Clear Sky Science · de
Ein lysinfreies REC-Tag-System für Anwendungen der Proximity-Biotinylierung
Warum winzige Tags an Proteinen wichtig sind
Im Inneren jeder Zelle arbeiten Proteine selten allein — sie gehen wechselnde Partnerschaften ein, die Gesundheit und Krankheit steuern. Um diese Partnerschaften zu untersuchen, bringen Wissenschaftler*innen häufig kleine „Namensschilder“ an Proteinen an, damit sie nachverfolgt, aus einem Gemisch herausgezogen oder unter dem Mikroskop sichtbar gemacht werden können. Eine verbreitete Methode, die Proximity-Biotinylierung, erlaubt es, zu kartieren, wer sich im Zellinneren neben wem aufhält, bringt aber ein verborgenes Problem mit sich: Viele dieser Tags werden chemisch modifiziert und verschwinden genau dann, wenn man sie am dringendsten braucht. Diese Studie stellt eine neue Art von Tag vor, das REC-Tag, das dafür entworfen wurde, unter diesen anspruchsvollen Bedingungen sichtbar zu bleiben.
Ein chemischer Textmarker für Protein-Nachbarn
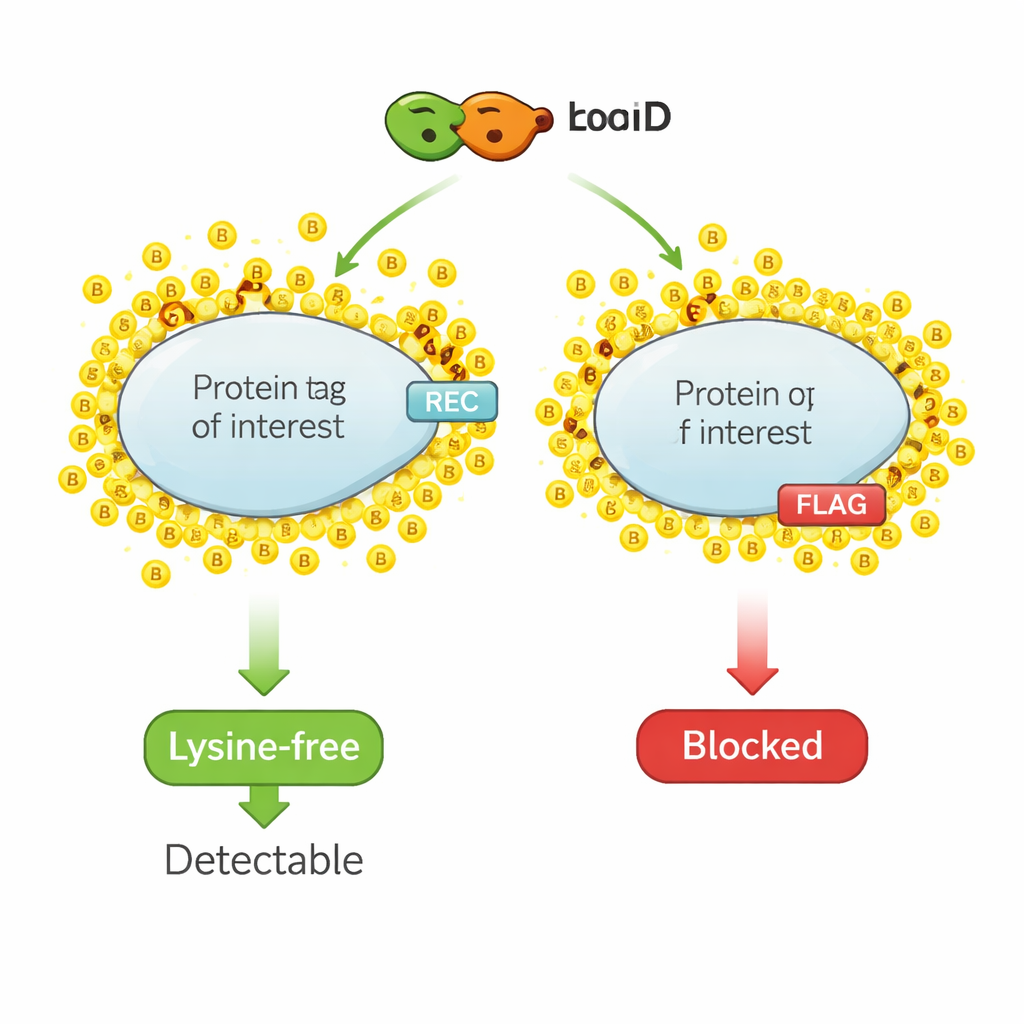
Proximity-Biotinylierung funktioniert wie ein molekularer Textmarker. Ein gentechnisch verändertes Enzym, etwa TurboID, wird an ein Interessensprotein fusioniert. Sobald Biotin — ein kleines Vitamin — zugegeben wird, heftet TurboID rasch Biotinmoleküle an nahegelegene Proteine. Anschließend fischen Forschende alle biotinylierten Proteine heraus und identifizieren sie, um einen Schnappschuss der lokalen Nachbarschaft des Proteins zu gewinnen. Doch dieselbe Chemie, die nahe Proteine markiert, trifft auch die kleinen Epitop-Tags, die üblicherweise zur Detektion genutzt werden, weil diese Tags oft Lysin enthalten — eine Aminosäure, die Hauptansatzstelle für Biotin. Wenn Lysin in dem Tag mit Biotin bedeckt ist, können Antikörper den Tag nicht mehr erkennen, und das Signal in Standardnachweismethoden nimmt ab oder verschwindet.
Entwurf eines Tags, das Modifikation verweigert
Um dieses Problem zu lösen, machten sich die Autor*innen daran, einen neuen Tag völlig ohne Lysin zu entwickeln. Sie begannen mit einem Fragment eines Malariaparasiten-Proteins namens PfRipr5, das nur geringe Ähnlichkeit zu menschlichen Proteinen aufweist und dadurch das Risiko unerwünschter Kreuzreaktionen reduziert. Mithilfe eines mikrochipbasierten Screening-Verfahrens in Kaninchen erzeugten sie 22 monoklonale Antikörper gegen PfRipr5 und identifizierten einen, bezeichnet Klon Nr. 6, mit besonders starker und spezifischer Bindung. Durch systematisches Kürzen und Mutieren des PfRipr5-Fragments schränkten sie die Zielsequenz des Antikörpers auf eine 11–Aminosäuren-Strecke ein. Diese minimale Sequenz enthielt nur ein Lysin, das sie durch eine ähnliche Aminosäure, Arginin, ersetzten. Bemerkenswerterweise blieb die Antikörperbindung unverändert stark. Diese optimierte, lysinfreie Sequenz nannten sie REC-Tag, und den passenden Antikörper den REC-Antikörper.
Das REC-Tag auf die Probe gestellt
Das Team prüfte dann, ob das REC-Tag gängige Tags wie FLAG in verbreiteten Laborverfahren ersetzen kann. Wenn es an fluoreszierende oder signalgebende Proteine fusioniert und in zellfreien Systemen sowie in Säugerzellen exprimiert wurde, ließen sich REC-getaggte Proteine problemlos durch Immunblotting, einen hochsensitiven lichtbasierten Plattenassay namens AlphaScreen und durch Immunfärbung in Zellen nachweisen. Die Nachweisstärke war ähnlich der des FLAG-Tags und eines anderen lysinfreien Tag-Systems (AGIA), und der REC-Antikörper zeigte über verschiedene human- und Affenzelllinien hinweg sehr geringe Hintergrundsignale. Wichtig ist, dass das Tag sowohl am N‑ als auch am C‑Termin eines Proteins funktionierte und bei Proteinen in unterschiedlichen zellulären Bereichen — einschließlich Zellkern, Mitochondrien, endoplasmatischem Retikulum und Zellmembran — nutzbar war.
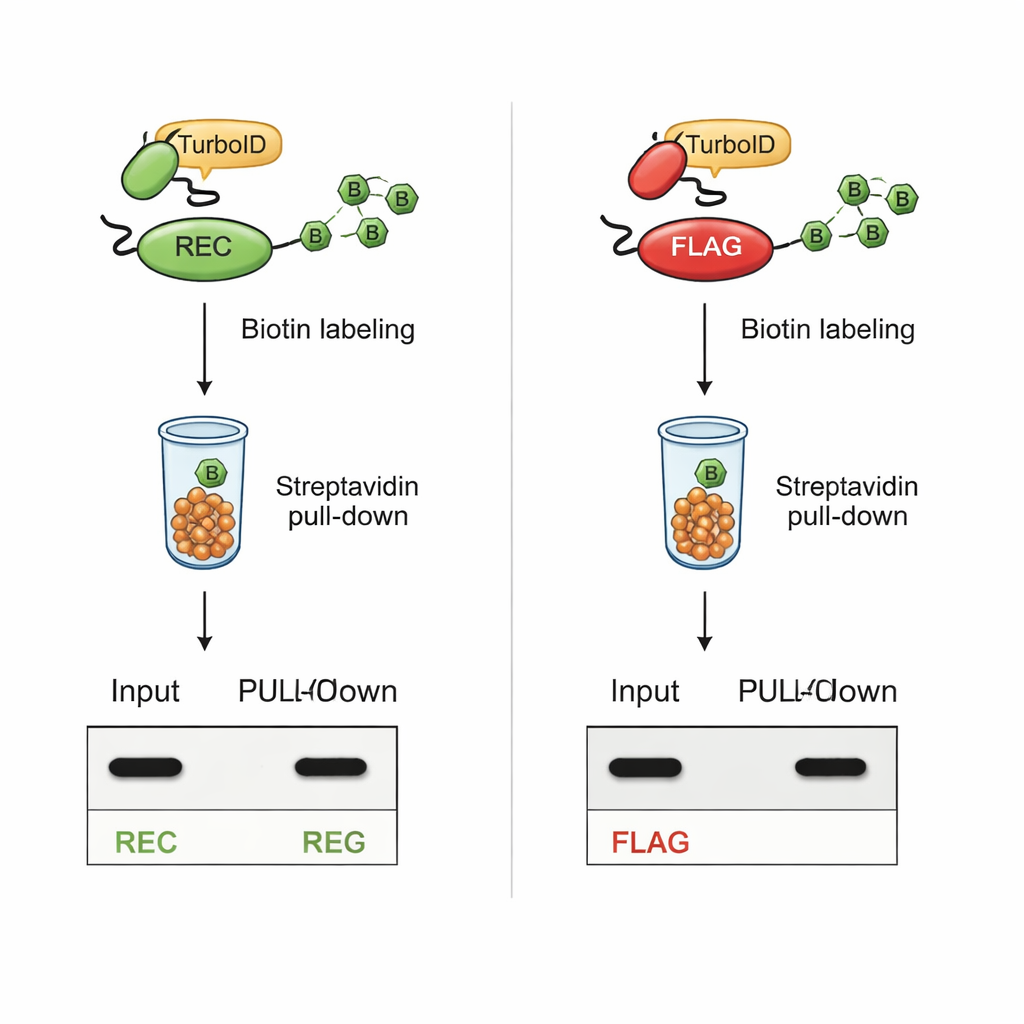
Sichtbar bleiben während intensiver Markierung
Der entscheidende Test war, ob REC nach TurboID-basierter Biotinylierung weiterhin detektierbar bleibt. In Zellen, in denen TurboID an bekannte Interaktionspartner fusioniert war, blieben Proteine mit dem REC-Tag sowohl in Gesamtzell-Extrakten als auch in der gereinigten, biotinylierten Fraktion deutlich sichtbar. Im Gegensatz dazu verloren Proteine mit dem klassischen FLAG-Tag ihr FLAG-Signal, sobald TurboID aktiv war, obwohl die Proteine selbst weiterhin vorhanden waren. Zusätzliche Experimente mit synthetischen Peptiden zeigten, dass TurboID die Lysinreste in der FLAG-Sequenz direkt biotinyliert und so physisch den Antikörperzugang blockiert. Das REC-Tag, dem Lysin vollständig fehlt, wurde von TurboID nicht verändert und blieb leicht nachweisbar.
Was das für künftige Experimente bedeutet
Für Forschende, die Proteinnetzwerke in lebenden Zellen untersuchen, bietet das REC-Tag ein praktisches neues Werkzeug: Es verhält sich in alltäglichen Assays wie vertraute Tags, funktioniert aber weiter, selbst wenn potente Proximity-Labeling-Enzyme aktiv sind. Das bedeutet, dass Wissenschaftler*innen zuverlässiger bestätigen können, dass ihre getaggten Proteine vorhanden und korrekt erfasst sind, und gleichzeitig andere lysinbasierte Modifikationen — wie Ubiquitinierung und Acetylierung — studieren können, ohne dass das Tag selbst stört. Kurz gesagt: REC ist eine kleine Designänderung mit großer Wirkung, die dazu beiträgt, komplexe Proteinkartierungs-Experimente klarer und vertrauenswürdiger zu machen.
Zitation: Tokunaga, S., Nagaoka, H., Ozawa, T. et al. A lysine-free REC tag system for proximity-biotinylation applications. Sci Rep 16, 4846 (2026). https://doi.org/10.1038/s41598-026-35323-w
Schlüsselwörter: Protein-Markierung, Proximity-Biotinylierung, TurboID, Protein-Interaktionen, Epitop-Tags