Clear Sky Science · de
EEG-basierte Klassifizierung von Alzheimer-Krankheit und frontotemporaler Demenz anhand funktionaler Konnektivität
Warum Hirnwellenmuster wichtig sind
Demenz betrifft Millionen von Familien, doch selbst Ärztinnen und Ärzte tun sich oft schwer, verschiedene Formen zu unterscheiden. Alzheimer-Krankheit und frontotemporale Demenz sehen in der Klinik häufig ähnlich aus, verlangen aber unterschiedliche Behandlungspläne und Studienansätze. Diese Studie stellt eine einfache, aber wirkungsvolle Frage: Können wir mit einem schnellen, nichtinvasiven Hirntest — der Elektroenzephalographie (EEG) — die Kommunikationsmuster des ruhenden Gehirns ablesen und damit diese Erkrankungen von gesundem Altern und voneinander unterscheiden?
Die Unterhaltungen des Gehirns betrachten, nicht nur seine Aktivität
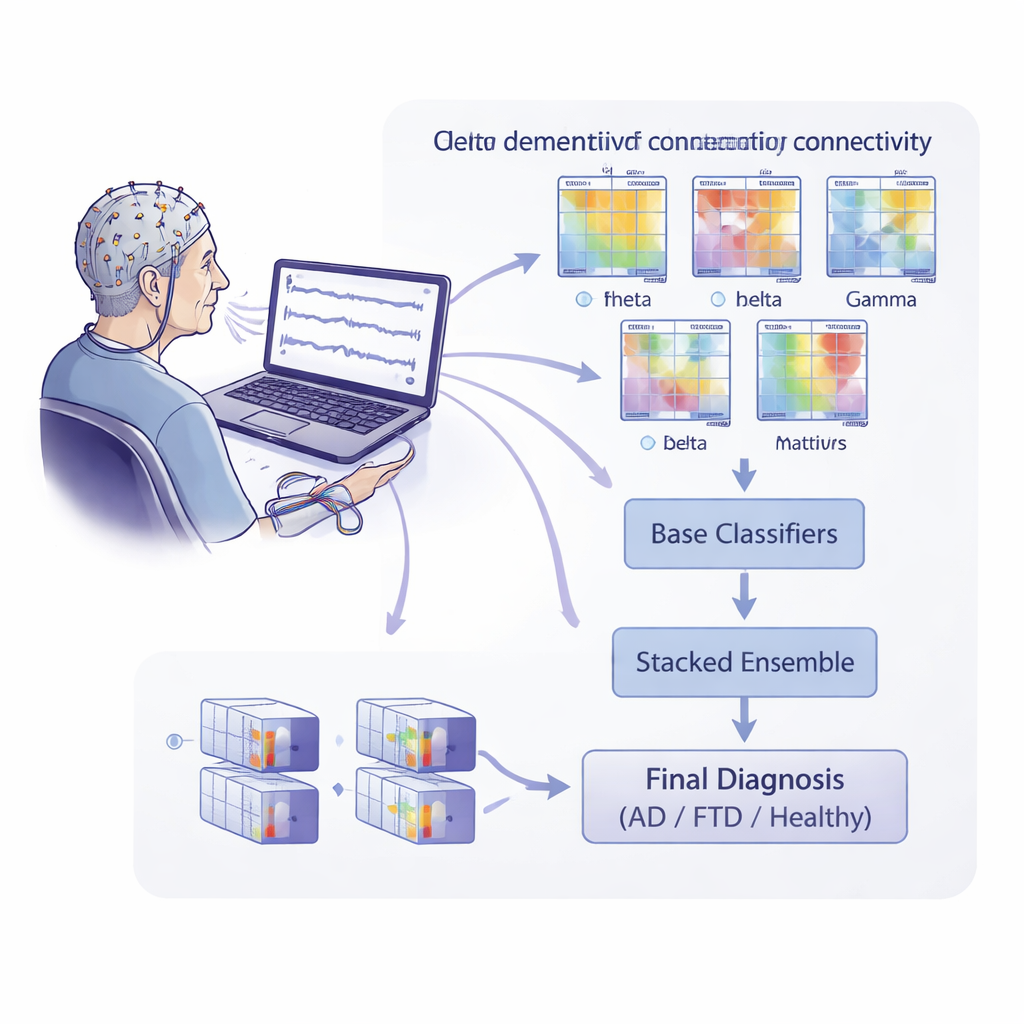
EEG misst üblicherweise, wie stark Hirnwellen in verschiedenen Frequenzbändern sind, etwa langsame Delta- oder schnellere Alpha-Wellen. Die Forscher gingen hier einen Schritt weiter und untersuchten, wie verschiedene Hirnregionen „miteinander sprechen“. Sie nutzten Aufnahmen von 88 Personen: 36 mit Alzheimer-Krankheit, 23 mit frontotemporaler Demenz und 29 gesunden älteren Erwachsenen. Mit 19 Skalp-Elektroden zeichneten sie die Hirnaktivität in Ruhe mit geschlossenen Augen auf und teilten jede Aufnahme in viele kurze Zeitsegmente. Für jedes Segment und mehrere Frequenzbänder berechneten sie eine Reihe von Konnektivitätsmaßen — mathematische Beschreibungen dafür, wie eng verschiedene EEG-Kanäle zeitlich, frequenzmäßig und phasenbezogen miteinander verbunden sind.
Algorithmen beibringen, Demenzmuster zu erkennen
Um diese Konnektivitätskarten in Vorhersagen zu überführen, trainierte das Team eine große Anzahl einfacher maschineller Lernmodelle, wobei sich jedes auf eine Kombination aus Frequenzband und Konnektivitätsmaß konzentrierte. Diese Basismodelle verwendeten spezialisierte mathematische Werkzeuge, um Konnektivitätsmuster zwischen Individuen zu vergleichen. Die Ausgaben aller Basismodelle wurden dann in ein höherstufiges „gestapeltes“ Modell eingespeist, das lernen sollte, welche Merkmal-Kombinationen am aussagekräftigsten sind. Entscheidend war, dass die Forschenden die Leistung auf der für die Klinik relevanten Ebene bewerteten: eine einzelne Diagnose pro Person. Sie nutzten ein strenges Testschema, bei dem die Daten einer Person stets vollständig vom Trainingsdatensatz getrennt blieben, um das Risiko überoptimistischer Ergebnisse durch subtile Datenleckagen zu verringern.
Was die Hirnwellen offenbarten — und was sie nicht taten
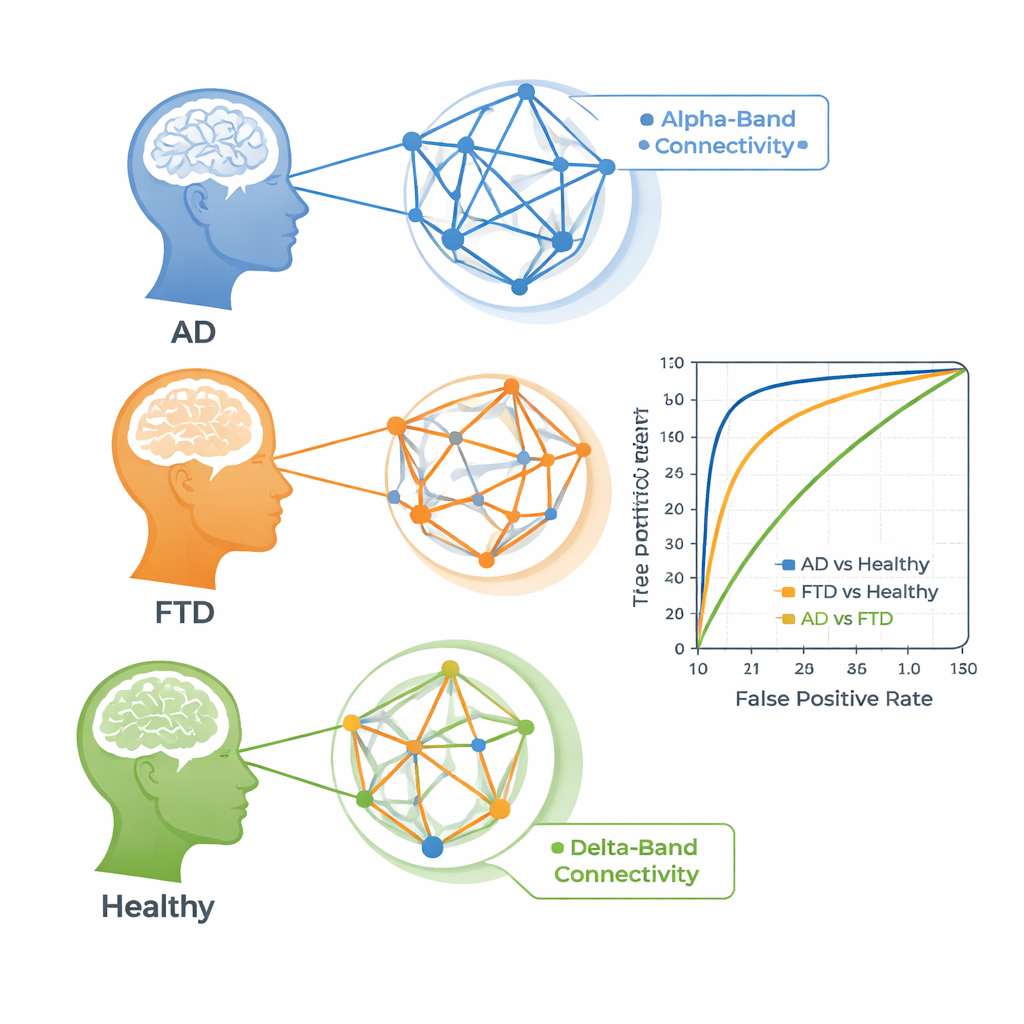
Die Konnektivitätsmuster halfen, Personen mit Demenz von gesunden Versuchspersonen zu unterscheiden. Bei Alzheimer gegenüber gesunden Kontrollen erreichten einige einzelne Konnektivitätsmerkmale AUC-Werte über 85 %, was bedeutet, dass sie recht gut darin waren, die Erkrankten zu ranken. Für frontotemporale Demenz gegenüber gesundem Altern galt Ähnliches, wenn auch etwas schwächer. Die informativsten Signale in beiden Fällen stammten aus dem Alpha-Band, einem Rhythmus, der mit entspannter Wachheit verbunden ist und bei Demenz oft gestört ist. Das Unterscheiden von Alzheimer und frontotemporaler Demenz war hingegen deutlich schwieriger. Die besten Maße für diese Aufgabe kamen aus dem langsamen Delta-Band und erreichten nur mäßige Genauigkeit, was darauf hindeutet, dass beide Krankheiten in diesen EEG-Aufnahmen viele derselben großräumigen Netzwerkstörungen teilen.
Wenn mehr Komplexität nicht bessere Antworten bringt
Eine Hoffnung bei Ensemble-Methoden ist, dass das Kombinieren vieler schwacher Prädiktoren ein stärkeres, verlässlicheres Modell ergibt. In dieser Studie übertraf das gestapelte Ensemble jedoch nicht die besten einzelnen Konnektivitätsmerkmale. Tatsächlich waren die besten Einzelmodelle oft leicht besser. Zusätzliche Analysen zeigten, dass viele Basismodelle ähnliche Fehler machten, sodass das Ensemble nur begrenzte wirklich neue Informationen zu nutzen hatte. Die Autorinnen und Autoren testeten auch verschiedene Wege, Abstände zwischen Konnektivitätsmatrizen zu messen, einschließlich fortgeschrittener „Mannigfaltigkeits“-Geometriemethoden, fanden jedoch wenig Vorteil gegenüber einfacheren Ansätzen für dieses Zwischen-Personen-Diagnoseproblem.
Was das für Patientinnen, Patienten und Kliniker bedeutet
Für Menschen mit Gedächtnis- oder Verhaltensveränderungen bieten diese Befunde vorsichtigen Optimismus. Ruhender Zustand-EEG, ein schneller, kostengünstiger und breit verfügbarer Test, erfasst sinnvolle Signaturen von Demenz in der Art, wie Hirnregionen miteinander verbunden sind. Gleichzeitig unterstreicht die Arbeit, dass clevere Mathematik allein enge Verwandtschaften zwischen Krankheiten nicht vollständig auflösen kann, wenn die Daten begrenzt sind und sich die Hirnveränderungen überschneiden. Die Autoren argumentieren, dass sorgfältig ausgewählte, interpretierbare EEG-Merkmale, bewertet mit strenger Subjekt-Level-Testung, verlässlicher sein könnten als hochkomplexe Modelle. Der künftige Fortschritt wird ihrer Ansicht nach wahrscheinlich daraus entstehen, EEG-Konnektivität mit anderen Biomarkern wie Hirnbildern, Bluttests und kognitiven Profilen zu kombinieren, um präzisere und vertrauenswürdigere Werkzeuge zur Diagnose verschiedener Demenzformen zu entwickeln.
Zitation: Mlinarič, T., Van Den Kerchove, A., Barinaga, Z.I. et al. EEG-based classification of alzheimer’s disease and frontotemporal dementia using functional connectivity. Sci Rep 16, 4903 (2026). https://doi.org/10.1038/s41598-026-35316-9
Schlüsselwörter: EEG, funktionale Konnektivität, Alzheimer-Krankheit, frontotemporale Demenz, maschinelles Lernen