Clear Sky Science · de
Wechselwirkung zwischen ELMO1-DNA-Methylierung und Med31 fördert H. pylori‑induziertes Magenkrebs‑EMT und intestinale Metaplasie über M2‑Polarisation
Warum Bakterien im Magen für das Krebsrisiko wichtig sind
Die meisten von uns tragen Milliarden Bakterien im Verdauungstrakt, und eines davon — Helicobacter pylori — kann Jahrzehnte lang still im Magen leben. Für manche Menschen verläuft diese Infektion unbemerkt und ohne Schaden, für andere ist sie jedoch der erste Schritt auf dem Weg zum Magenkrebs, einer der tödlichsten Krebsarten weltweit. Diese Studie untersucht, wie eine winzige chemische Veränderung an der DNA in Magenzellen dazu beiträgt, eine langanhaltende Infektion in vorKrebsschäden und schließlich in ein Umfeld zu verwandeln, in dem Krebs wachsen kann.
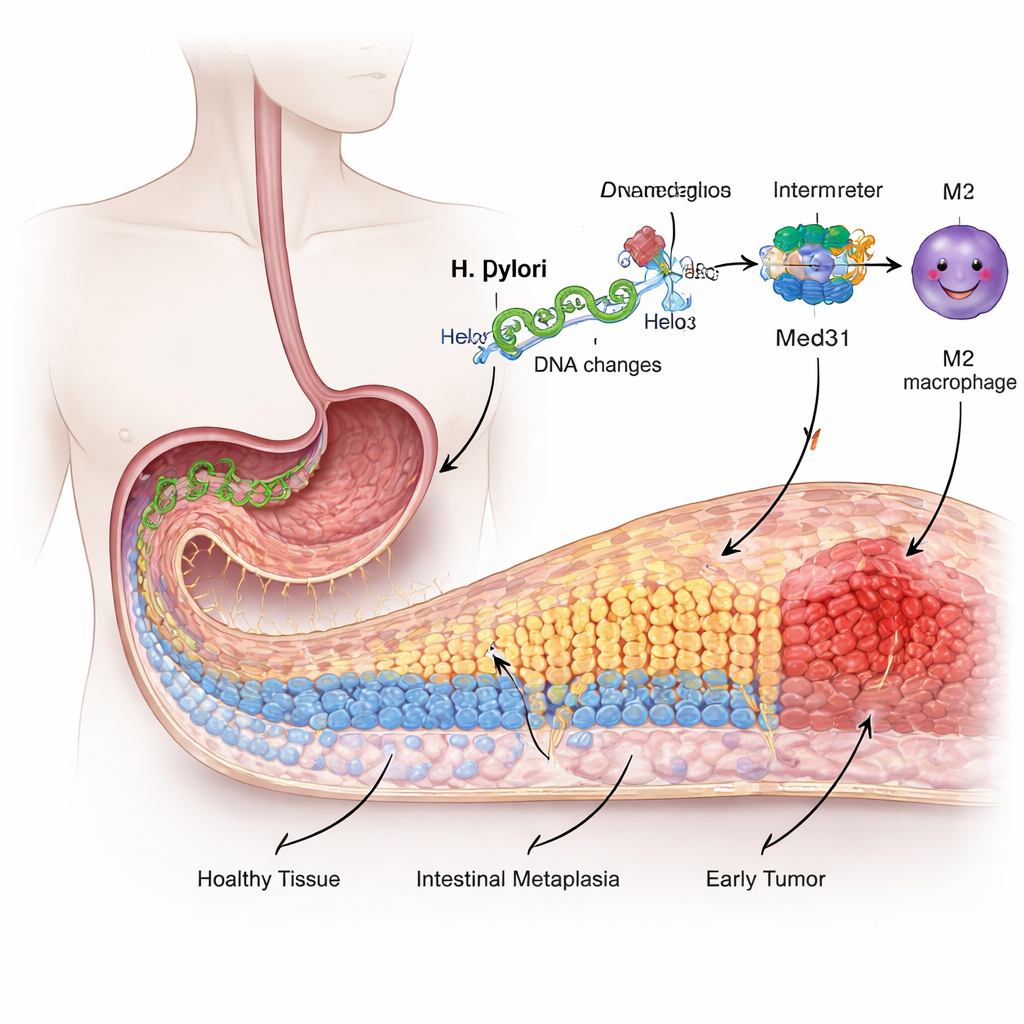
Von freundlicher Schleimhaut zur riskanten Umgestaltung
Die Innenseite des Magens ist mit spezialisierten Zellen ausgekleidet, die an den Umgang mit starker Säure angepasst sind, nicht an die Nahrungsverdauung wie im Darm. Nach Jahren von Reizung und Entzündung durch H. pylori beginnen einige dieser Magenzellen, sich „umzudekorieren“ und Merkmale intestinaler Zellen anzunehmen — ein Prozess, der als intestinale Metaplasie bezeichnet wird. Diese Veränderung gilt als präkanzeröse Stufe. Die Forschenden verwendeten eine humane Magenzelllinie, um die Infektion zu modellieren, und fanden heraus, dass die Exposition gegenüber H. pylori diese Zellen dazu brachte, schneller zu wachsen, sich leichter zu bewegen und intestinale Marker anzuschalten — alles Zeichen dafür, dass die Schleimhaut ihre normale Identität verliert.
Kleine chemische Anhänge mit großen Folgen
Unsere DNA kann mit winzigen chemischen Gruppen, sogenannten Methylgruppen, markiert werden, die wie Ein‑/Aus‑Schalter für Gene wirken, ohne den genetischen Code selbst zu verändern. Das Team konzentrierte sich auf ein Gen namens ELMO1, das bereits mit Zellbewegung und Tumorausbreitung in Verbindung gebracht wird. Sie zeigten, dass eine H. pylori-Infektion die Methylierung des ELMO1-Gens erhöhte und — etwas kontraintuitiv — dessen Aktivität und Proteinspiegel in Magenzellen steigerte. Als sie ein Medikament einsetzten, das diese Methylgruppen entfernt, verloren die Zellen viele der infektionsinduzierten Veränderungen: Sie teilten sich weniger, bewegten sich weniger und zeigten weniger Anzeichen intestinaler Metaplasie. Das deutet darauf hin, dass die ELMO1‑Methylierung ein entscheidender Schalter ist, den das Bakterium umlegt.
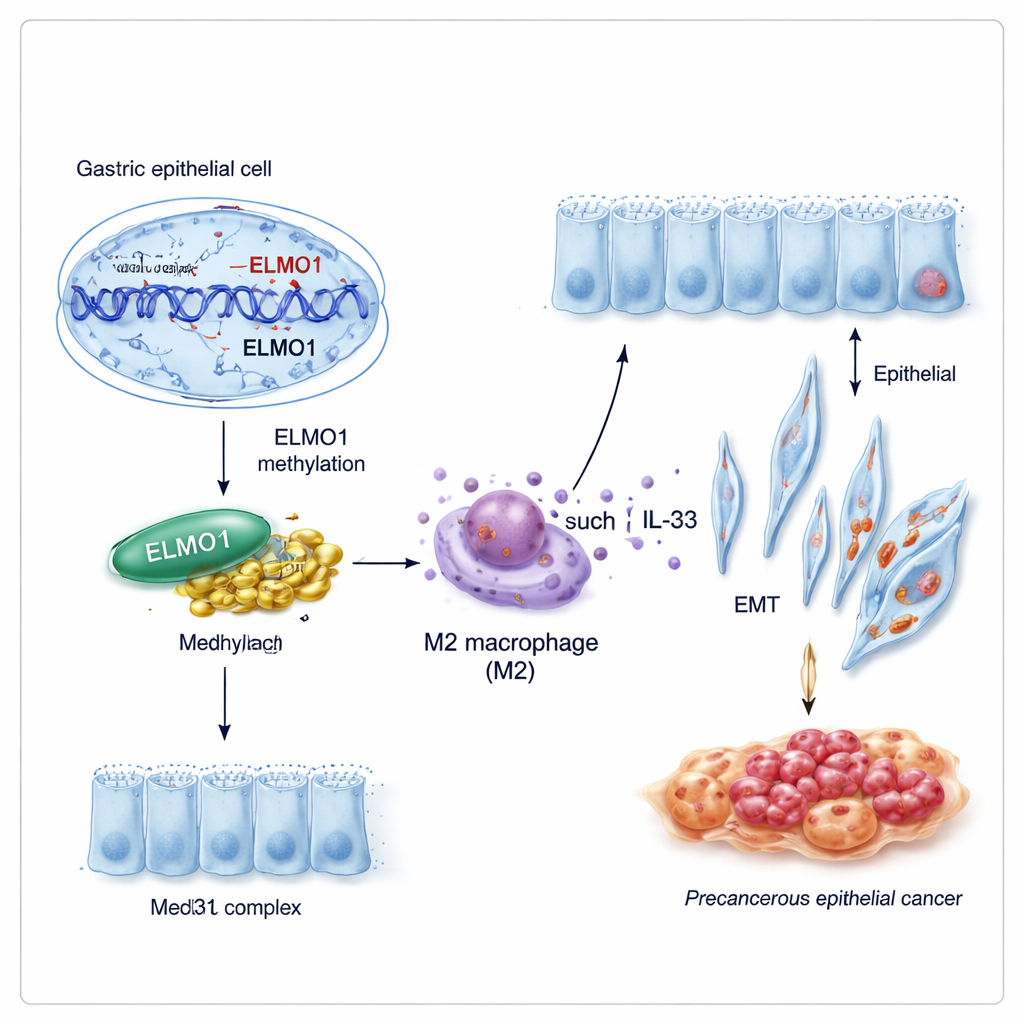
Eine neue Partnerschaft, die das Zellverhalten umprogrammiert
Gene wirken selten allein. Die Forschenden entdeckten, dass methyliertes ELMO1 eine Partnerschaft mit einem anderen Protein, Med31, begünstigt — einem Teil einer großen „Schaltzentrale“, die mitbestimmt, welche Gene eine Zelle ein- oder ausschaltet. Unter Bedingungen, die DNA‑Methylierung förderten, stiegen ELMO1‑ und Med31‑Spiegel an und die beiden banden sich physisch aneinander, während ein früher bekannter Partner von ELMO1, DOCK10, in den Hintergrund gedrängt wurde. Dieses neue ELMO1–Med31‑Team scheint das Genexpressionsprogramm der Magenzellen so zu verändern, dass sie eher intestinale Merkmale annehmen und aggressiver auftreten.
Wie Immunzellen dazu gedrängt werden, den Tumor zu unterstützen
Krebs entsteht nicht isoliert; er wächst innerhalb einer komplexen Nachbarschaft aus Immun‑ und Stützzellen. Die Studie zeigt, dass infizierte Magenzellen mit methyliertem ELMO1 höhere Mengen an IL‑33 freisetzen — ein Signal, das benachbarte Immunzellen, sogenannte Makrophagen, in einen tumorfördernden M2‑Zustand schiebt. In einem Ko‑Kultur‑System stellten die Autoren fest, dass Makrophagen, die diesen Signalen ausgesetzt waren, stark in Richtung M2‑Typ kippten und im Gegenzug Faktoren abgaben, die frische Magenzellen dazu brachten, mobiler, invasiver und darmähnlicher zu werden. Marker des epithelial‑mesenchymalen Übergangs — wenn stationäre Epithelzellen sich in wandernde, invasionsfähige Zellen verwandeln — stiegen unter dem Einfluss dieser M2‑Makrophagen deutlich an.
Was das für die Vorbeugung von Magenkrebs bedeutet
In der Zusammenfassung zeichnet die Arbeit eine Ereigniskette nach: H. pylori-Infektion verändert die DNA‑Methylierung von ELMO1, dieses modifizierte ELMO1 geht eine Verbindung mit Med31 ein, infizierte Zellen senden Signale aus, die benachbarte Immunzellen in M2‑Helfer verwandeln, und diese Helfer treiben sowohl intestinale Metaplasie als auch einen invasiveren Zellzustand voran. Für Nicht‑Spezialisten ist die zentrale Idee, dass ein verbreitetes Magenbakterium sowohl die Magenschleimhaut als auch die lokale Immunantwort durch reversible chemische Markierungen der DNA umformen kann. Das Verständnis dieses Wegs könnte neue Möglichkeiten eröffnen — etwa Bluttests, die riskante Methylierungsmuster früh erkennen, sowie Medikamente, die die ELMO1–Med31–M2‑Achse blockieren, bevor eine chronische Infektion sich zu Magenkrebs entwickelt.
Zitation: Lu, T., Yu, T., He, C. et al. Interaction between ELMO1 DNA methylation and Med31 promotes H. pylori-induced gastric cancer EMT and intestinal metaplasia via M2 polarization. Sci Rep 16, 5201 (2026). https://doi.org/10.1038/s41598-026-35314-x
Schlüsselwörter: Magenkrebs, Helicobacter pylori, DNA-Methylierung, intestinale Metaplasie, Tumormikromilieu