Clear Sky Science · de
Modellierung und experimentelle Verifikation der Ausfällung von Polycaprolacton-Nanopartikeln
Warum winzige Kunststoffkugeln für die Medizin wichtig sind
Stellen Sie sich vor, Sie verpacken ein starkes Medikament in einen so kleinen Partikel, dass er durch Blutgefäße schlüpfen und seine Ladung genau dort freisetzen kann, wo sie gebraucht wird. Solche Partikel, Polymernanopartikel genannt, stehen im Mittelpunkt vieler neuer Therapien und bildgebender Verfahren. Sie mit der richtigen und reproduzierbaren Größe herzustellen, ist jedoch überraschend schwierig. Diese Studie zeigt, wie ein einfaches, physikbasiertes Computermodell die Größe eines weit verbreiteten biologisch abbaubaren Nanopartikels vorhersagen und einstellen kann und damit potenziell Jahre an Versuch‑und‑Irrtum in der Entwicklung neuer Nanomedikamente einsparen könnte.
Vom Küchenrühren zur Laborpräzision
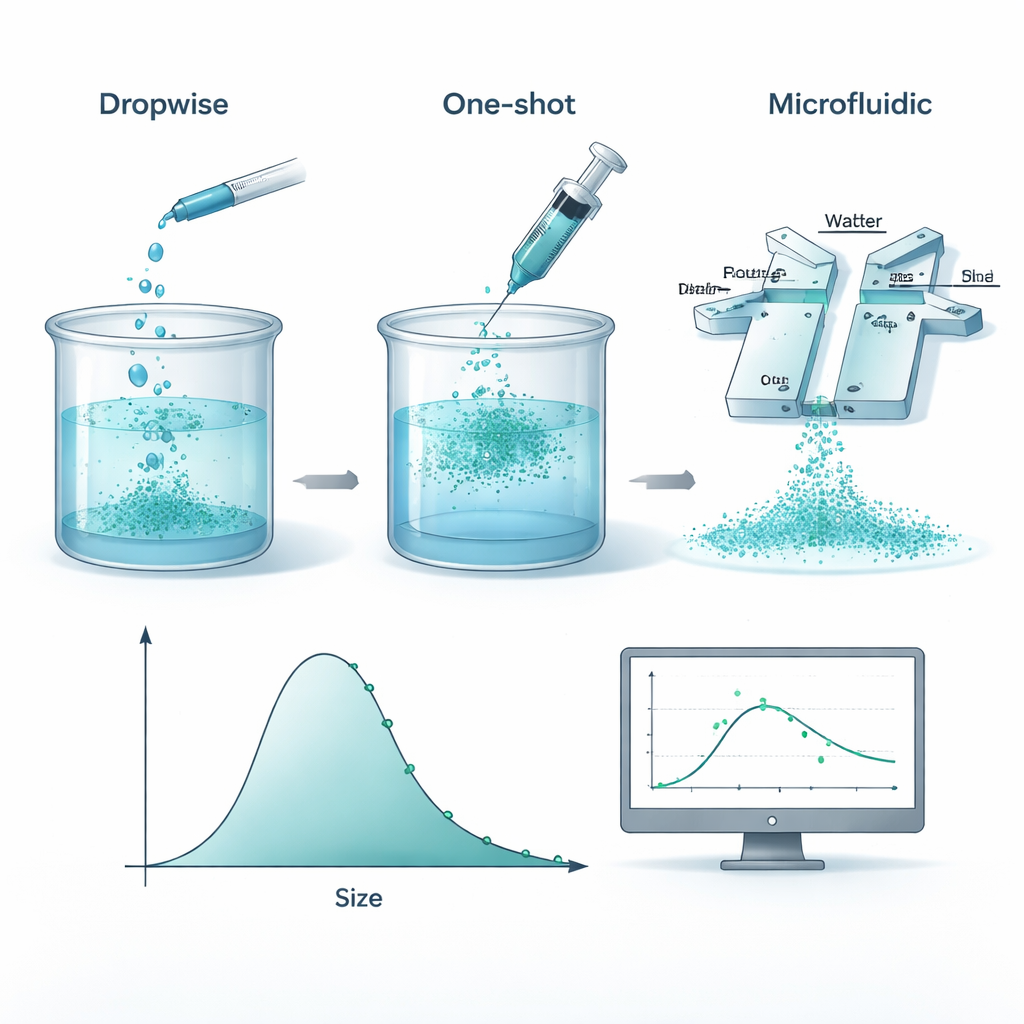
Um diese Nanopartikel herzustellen, lösen Forscher ein biologisch abbaubares Polymer namens Polycaprolacton (PCL) in einem organischen Lösungsmittel und mischen es dann mit Wasser, sodass das Polymer aus der Lösung „ausfällt“ und winzige Kugeln bildet. Das Team verglich drei praktische Verfahren: das langsame Tropfenlassen der Polymerlösung, das einmalige Einwerfen der Lösung und das Fördern beider Flüssigkeiten durch ein kleines mikrofluidisches Bauteil, in dem sie in engen Kanälen zusammentreffen. Unter sorgfältig kontrollierten Bedingungen ergaben alle drei Verfahren Partikel mit sehr ähnlichen mittleren Größen und Verteilungsbreiten. Das bedeutet, dass in den untersuchten Bereichen eher die eingesetzten Inhaltsstoffe — Mengen an Polymer und Stabilisator — als das genaue Mischverfahren entscheidend sind.
Wie Viskosität und Helfermoleküle die Partikel formen
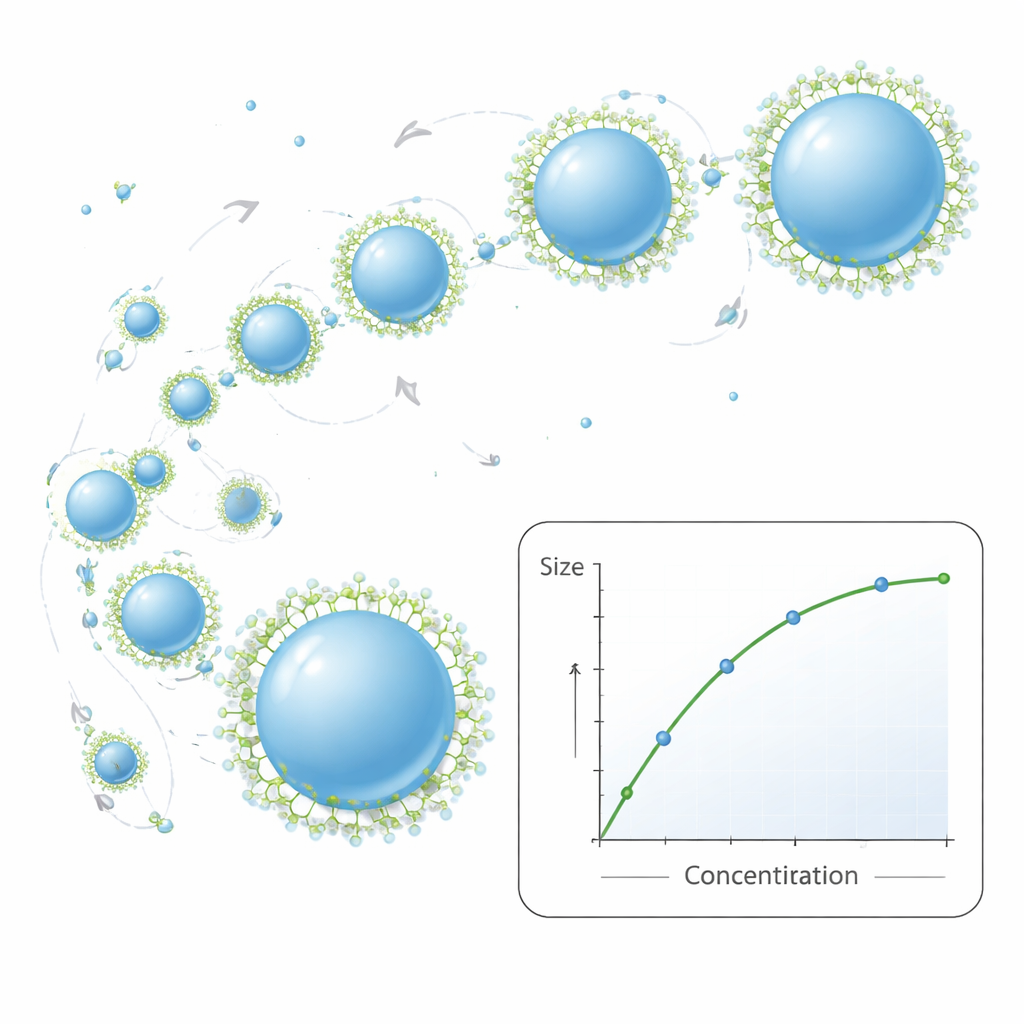
Die Forscher untersuchten anschließend, wie die Rezepturzutaten die endgültige Partikelgröße steuern. Eine Erhöhung der PCL‑Menge in der organischen Phase macht diese Flüssigkeit dicker bzw. viskoser. Denken Sie daran, Sirup in Wasser statt Saft zu mischen: Dickere Flüssigkeiten zerbrechen in größere Tropfen. Hier führten dichtere Polymerlösungen zu größeren Nanopartikeln und etwas breiteren Größendistributionen. Das Hinzufügen eines zweiten Lösungsmittels, Ethanol, stabilisierte den Prozess selbst bei sehr hohen Polymerkonzentrationen, hatte aber den Nachteil, dass die Partikel im oberen Konzentrationsbereich größer wurden. Ein weiterer Bestandteil, ein Tensid namens Pluronic F‑127, wirkt wie ein molekularer Anti‑Agglomerator. Bei niedrigen Tensidkonzentrationen neigen Partikel dazu, aneinander zu stoßen und zusammenzukleben, wodurch sie größer und ungleichmäßiger werden. Mit steigender Tensidkonzentration legen sich Moleküle auf die Partikeloberflächen, verhindern ein Verschmelzen und führen zu kleineren, stabileren Nanopartikeln — bis zu einem Punkt, an dem weitere Zufuhren nur noch geringe Verbesserungen bringen und die Größendisperion wieder heterogener werden kann.
Eine einfache Wachstumsregel, die der Realität entspricht
Kern der Arbeit ist ein kompaktes mathematisches Modell, das beschreibt, wie Nanopartikel wachsen, nachdem sie erstmals entstanden sind. Es behandelt ihre Bewegung als zufälliges Ruckeln in der Flüssigkeit, bei dem Kollisionen manchmal dazu führen, dass zwei Partikel zu einem größeren verschmelzen. Frühere Modelle gingen davon aus, dass Partikel bei Kontakt sofort verschmelzen und perfekte Kugeln bilden. Das neue Modell ergänzt zwei realistische Aspekte: Erstens erlaubt es eine endliche Zeit, in der zwei aneinandergrenzende Partikel von einer verlängerten Form zu einer einzigen Kugel entspannen; zweitens lässt es zu, dass Tensidmoleküle die Oberfläche schrittweise „blockieren“ und dadurch weiteres Verschmelzen verlangsamen oder verhindern. Mit nur wenigen messbaren Eingangsgrößen — wie Temperatur, Viskosität der Flüssigkeit und anfängliche Polymerkonzentration — sagt das Modell voraus, wie sich die durchschnittliche Partikelgröße mit den Rezepturbedingungen ändern sollte. Über viele Experimente hinweg stimmten die vorhergesagten Größen eng mit den mittels Lichtstreuung gemessenen Werten überein und erfassten zugleich allgemeine Trends in der Breite der Größendistribution.
Das Modell als Entwurfswerkzeug verwenden
Um zu prüfen, ob dieser Ansatz praktisch nützlich ist, kehrte das Team das Problem um: Statt das Modell nur zur Erklärung vergangener Daten zu verwenden, ließ es Rezepte vorschlagen, die drei spezifische Partikelgrößen und Gleichmäßigkeiten ergeben sollten. Diese „designten" Formulierungen wurden dann im Labor hergestellt. Die gemessenen Partikeldurchmesser wichen nur um 1–7 Prozent von den Zielwerten ab — also innerhalb typischer experimenteller Schwankungen — und zeigten, dass das Modell Formulierungsentscheidungen zuverlässig steuern kann. Vorhersagen zur Breite der Größendistribution waren weniger exakt, aber noch ausreichend, um relativ enge von weiter gestreuten Populationen zu unterscheiden. Im Vergleich zu aufwändigen Simulationsmethoden, die jedes Molekül oder jede Strömungseinstreuung verfolgen, läuft dieses vereinfachte Modell schnell auf durchschnittlicher Hardware und lässt sich leicht auf andere Polymere und Prozesskonfigurationen anpassen.
Was das für die Zukunft der Nanomedizin bedeutet
Für Nicht‑Spezialisten lautet die Hauptbotschaft: Die Herstellung brauchbarer Nanopartikel muss nicht länger ausschließlich auf mühsamem Versuch‑und‑Irrtum im Labor beruhen. Indem die wesentliche Physik beschrieben wird, wie kleine Kunststofftropfen sich bewegen, kollidieren und durch Tenside geschützt werden, liefert diese Arbeit eine praktische „Landkarte“ von Formulierungsentscheidungen — wie viel Polymer, welche Lösungsmittelmischung, wie viel Stabilisator — zur endgültigen Partikelgröße. Da PCL ein verbreitetes biologisch abbaubares Material in Wirkstofffreisetzung, Implantaten und Bildgebungsagentien ist, könnte dieses Modell Forschern helfen, sicherere und wirksamere Nanomedikamente schneller und mit weniger Materialverschwendung zu entwickeln. Dieselben Prinzipien lassen sich auf andere Polymere übertragen und bringen mehr Vorhersagbarkeit und Effizienz in die Welt nanoskaliger Therapien.
Zitation: Rybak, E., Trzciński, J., Gac, J. et al. Modeling and experimental verification of polycaprolactone nanoparticle precipitation. Sci Rep 16, 6613 (2026). https://doi.org/10.1038/s41598-026-35286-y
Schlüsselwörter: polymernanopartikel, Nanopräzipitation, Wirkstofffreisetzung, numerische Modellierung, Polycaprolacton