Clear Sky Science · de
Nicorandil lindert neuropathische und entzündliche Schmerzen über TNF-α-, IL6/MAPKERK1/2- und NO/cGMP-Signale
Warum die Linderung von Nervenschmerzen wichtig ist
Millionen von Menschen leben mit brennenden, stechenden oder kribbelnden Schmerzen, die lange nach Abheilung einer Verletzung anhalten. Dieser „neuropathische“ Schmerz kann hartnäckig gegen gängige Schmerzmittel resistent sein und geht häufig mit Nebenwirkungen bei langfristiger Medikation einher. Die hier zusammengefasste Studie untersucht, ob Nicorandil — ein Herzmedikament, das bereits bei Patienten mit Brustschmerzen eingesetzt wird — auch überaktive Schmerzwege im Nervensystem beruhigen kann und wie es dies auf zellulärer Ebene tut.
Ein Herzmedikament widmet sich der Schmerzforschung
Nicorandil wird routinemäßig zur Behandlung von Angina verschrieben, weil es die Blutgefäße entspannt. Es wirkt durch zwei Hauptmechanismen: Es spendet kleine Mengen Stickstoffmonoxid, ein Botenstoff, und öffnet bestimmte Kaliumkanäle in Zellen. Frühere Tierstudien deuteten an, dass Nicorandil Schmerzen reduzieren kann, indem es auf Nervenrezeptoren wirkt, die an Hitze- und Chili-Empfindungen beteiligt sind, und das körpereigene Opioidsystem einbezieht. In der vorliegenden Studie wollten die Forschenden kartieren, was nach diesen ersten Effekten passiert, mit Schwerpunkt auf Entzündung, oxidativem Stress (eine Art chemisches „Rosten“) und spezifischen Signalwegen innerhalb von Nervenzellen.
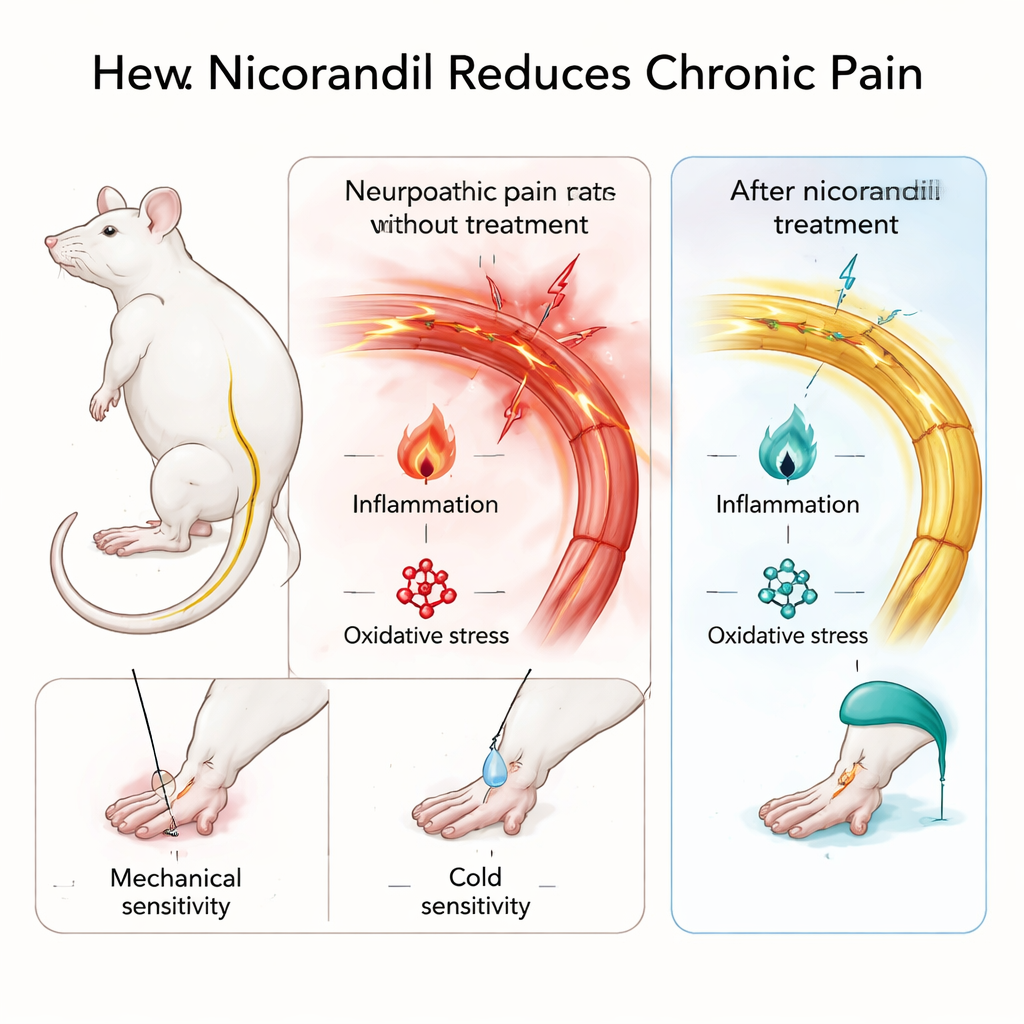
Test von Nicorandil in Modellen anhaltender Schmerzen
Um lang anhaltenden Nervenschmerz zu simulieren, banden die Forschenden den Ischiasnerv von Ratten lose zusammen, ein klassisches Verfahren, das Berührungs- und Kälteempfindlichkeit erzeugt, ähnlich wie beim Menschen mit neuropathischem Schmerz. Sie verwendeten außerdem den Formalin-Test, bei dem ein mildes chemisches Reizmittel in eine Pfote injiziert wird, um einen klar definierten, länger anhaltenden entzündlichen Schmerz zu erzeugen. Die Ratten erhielten Nicorandil oral in zwei Dosierungen, und die Wissenschaftler maßen, wie stark sie auf leichte Berührung und Kälte an der verletzten Pfote reagierten sowie wie oft und wie lange sie nach Formalin leckten oder zusammenzuckten. Wichtig ist: Nicorandil machte die Tiere im Freiland-Test nicht schläfrig oder wackelig, was darauf hindeutet, dass die Verringerung des Schmerzverhaltens nicht einfach auf Sedierung zurückzuführen war.
Absenken chemischer „Alarmstoffe“
Nicorandil reduzierte sowohl den durch Nervenschädigung ausgelösten Schmerz als auch den Formalin-evokierten Schmerz deutlich. Behandelte Ratten tolerierten Berührung und Kälte besser und zeigten weniger Zuckungen sowie kürzere Leckzeiten. Blutuntersuchungen zeigten, dass Nicorandil die Spiegel starker Entzündungsbotenstoffe — Tumornekrosefaktor alpha (TNF-α) und Interleukin-6 (IL‑6) — sowie Cyclooxygenase‑2, ein Enzym, das an der Produktion schmerzbezogener Prostaglandine beteiligt ist, senkte. Es verringerte außerdem Malondialdehyd, einen Marker für oxidativen Stress, was auf weniger chemische Schädigung der Zellmembranen hinweist. Unter dem Mikroskop wirkten Nerven von Nicorandil-behandelten Tieren gesünder: Es gab weniger strukturelle Schäden und Schwellungen im Ischiasnerv und im Ganglion der Hinterwurzel, dem Bündel sensorischer Nervenzellen.
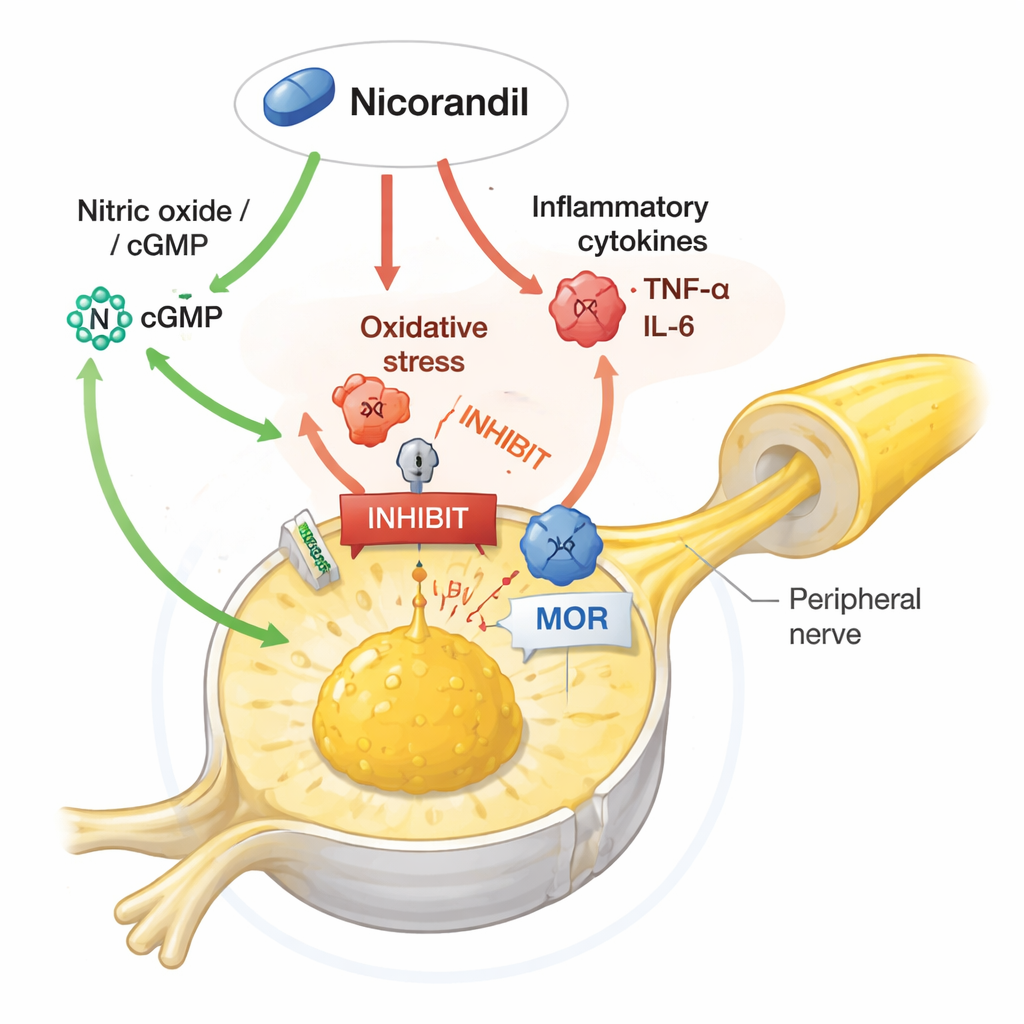
Das Signalknäuel in Schmerznerven entwirren
Die Studie ging weiter und untersuchte, welche molekularen Wege für die Wirkung von Nicorandil erforderlich sind. Als die Forschenden Arzneien verabreichten, die Stickstoffmonoxid stärkten oder den Spiegel von cyclischem GMP (einem mit NO verbundenen Botenstoff) erhöhten, schwächte sich Nicorandils Fähigkeit, Schmerzen zu lindern und Schlüsselproteine zu normalisieren, teilweise ab. Nicorandil verhinderte den typischen Anstieg von ERK1/2, einem Mitglied der MAP-Kinase-Familie, das Schmerzs Signale verstärkt, und dämpfte die Spiegel von TRPV1, einem Kanal, der Nerven gegenüber Hitze und chemischen Reizen empfindlicher macht. Die Verstärkung der NO-Signalgebung oder von cGMP kehrte diese schützenden Veränderungen um, während die Blockade von NO-bildenden Enzymen die Schmerzlinderung durch Nicorandil in manchen Fällen verstärkte. Überraschenderweise beseitigte die Blockade der Kaliumkanäle, die Nicorandil bekanntermaßen öffnet, nicht seine schmerzhemmenden Effekte, was darauf hindeutet, dass in diesem Kontext seine schmerzlindernde Wirkung stärker auf der Modulation von Stickstoffmonoxid, oxidativem Stress, Entzündung und opioider Signalgebung beruht als auf seiner klassischen gefäßwirksamen Funktion.
Was das für Menschen mit Schmerzen bedeuten könnte
Insgesamt zeichnen die Ergebnisse Nicorandil als einen Multitarget-Schmerzmodulator: Es beruhigt überaktive Nervenwege, indem es oxidative Schäden und entzündliche Botenstoffe reduziert, ERK1/2 und TRPV1 in sensorischen Neuronen dämpft und mit Stickstoffmonoxid sowie dem körpereigenen Opioidsystem interagiert. Obwohl diese Resultate aus Rattenmodellen und kurzfristiger Dosierung stammen, legen sie nahe, dass ein bereits klinisch eingesetztes Herzmedikament eines Tages umfunktioniert oder angepasst werden könnte, um schwer behandelbare neuropathische und entzündliche Schmerzkrankheiten zu unterstützen. Zukünftige Studien am Menschen sind nötig, um sichere Dosen, Langzeiteffekte und die Frage zu klären, ob dieselben Schutzmechanismen auch in menschlichen Nerven wirken.
Zitation: Badr, R.M., Abuiessa, S.A., Elblehi, S.S. et al. Nicorandil ameliorates neuropathic and inflammatory pain via TNF-α, IL6/MAPKERK1/2 and NO/cGMP signaling. Sci Rep 16, 4722 (2026). https://doi.org/10.1038/s41598-026-35272-4
Schlüsselwörter: neuropathischer Schmerz, Nicorandil, Entzündung, oxidativer Stress, Stickstoffmonoxid-Signalgebung