Clear Sky Science · de
Deubiquitinierungsbezogene Gene definieren Immunsubtypen von Darmkrebs und stehen in Zusammenhang mit Prognose und immuntherapiebezogenen Signaturen
Warum diese Studie für Betroffene wichtig ist
Darmkrebs gehört weltweit zu den häufigsten und tödlichsten Krebserkrankungen. Dennoch können Patientinnen und Patienten mit unter dem Mikroskop ähnlich aussehenden Tumoren sehr unterschiedliche Verläufe und Reaktionen auf moderne Therapien wie die Immuntherapie haben. Diese Studie stellt eine neue Frage: Lassen sich Darmkrebserkrankungen klarer in Gruppen einteilen, wenn man betrachtet, wie Tumorzellen mit dem „Recycling“ von Proteinen umgehen und wie das mit der Immunabwehr des Körpers verknüpft ist? Die Antwort könnte Ärzten künftig helfen, Prognosen genauer zu stellen und klügere Kombinationen von Therapien zu planen.
Proteinreinigung und Krebsverhalten
In jeder Zelle werden verschlissene oder beschädigte Proteine markiert und recycelt, damit sie sich nicht anreichern und Schaden anrichten. Ein Teil dieses Systems, die Deubiquitinierung, entfernt solche Markierungen und steuert fein, welche Proteine zerstört werden und welche erhalten bleiben. Die Autorinnen und Autoren sammelten große öffentliche Datensätze zu Darmtumoren und gesundem Gewebe und durchsuchten Tausende von Genen nach solchen, die sowohl mit diesem Proteinrecycling-System als auch mit dem Überleben der Patienten zusammenhängen. Sie schränkten die Liste auf 17 Schlüsselgene ein, die stark mit der Kontrolle der Zellteilung, der Reparatur von DNA-Schäden und der Struktur des das Gewebe umgebenden Gerüstes verbunden waren. Diese Gene bildeten das Rückgrat für eine neue Einteilung von Darmkrebserkrankungen.
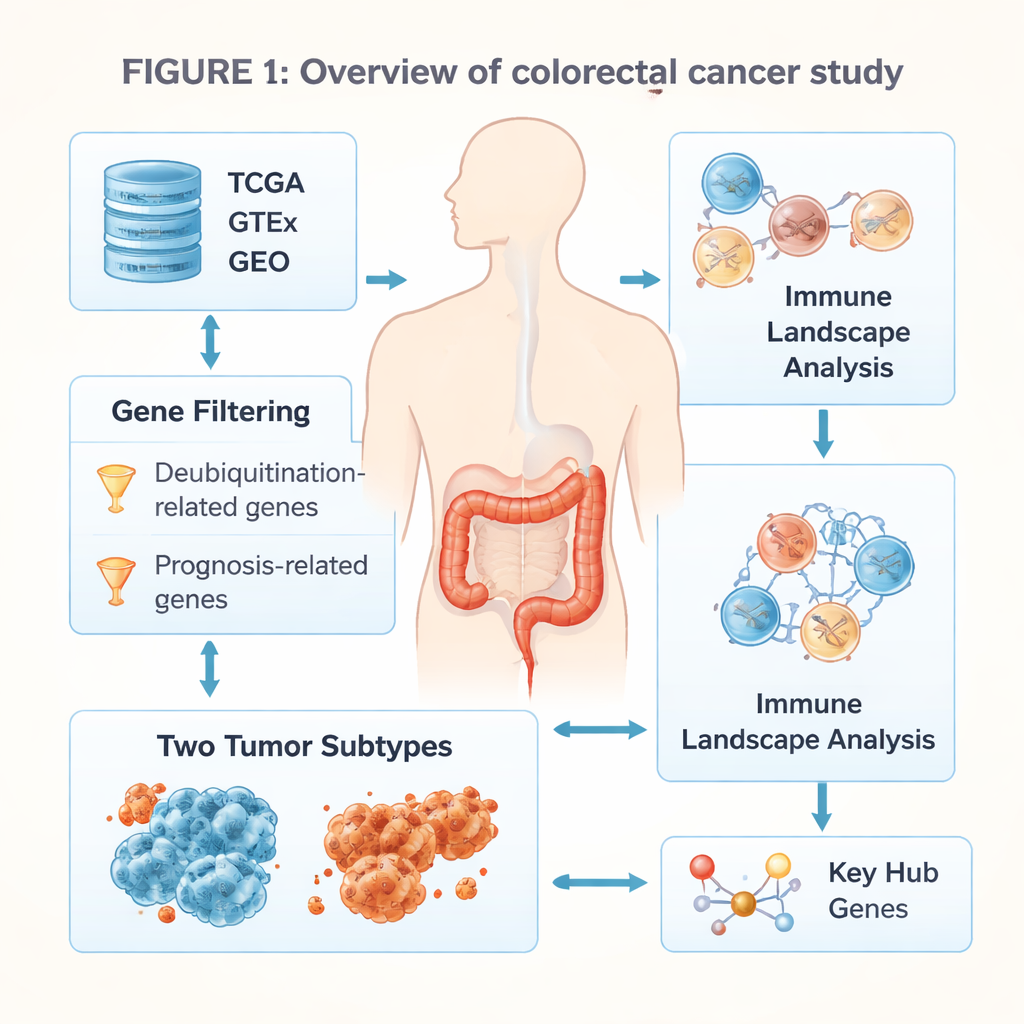
Es entstehen zwei Haupttumortypen
Anhand der Aktivitätsmuster dieser 17 Gene teilten die Forschenden die Tumoren in zwei Hauptsubtypen. Personen in einer Gruppe lebten tendenziell länger und wiesen frühere Erkrankungsstadien auf. Die andere Gruppe hatte eine schlechtere Prognose. Bei einer breiteren Betrachtung der in den Subtypen ein- oder ausgeschalteten Gene zeigte sich, dass die Gruppe mit ungünstiger Prognose starke Hinweise auf schnelle Zellproliferation, Stressreaktionen auf DNA-Schäden und intensive Umbauten des Gewebes um den Tumor herum aufwies. Im Gegensatz dazu zeigte die besser prognostizierte Gruppe weniger aggressiven Umbau und ein ausgewogeneres Muster von Zellwachstum und Reparatur.
Die Nachbarschaft des Tumors und die Immunantwort
Krebs wächst nicht isoliert; er lebt in einer Nachbarschaft aus Immunzellen, Stützszellen und narbenähnlichem Gewebe. Die Studie nutzte rechnerische Methoden, um abzuschätzen, welche Immunzellen in den einzelnen Tumoren vorhanden sind. Die beiden Subtypen zeigten auffällig unterschiedliche immunologische Landschaften. Der Subtyp mit schlechter Prognose war angereichert mit dichtem Kollagen und faserigem Gewebe, das eine physische und chemische Barriere bilden kann und Krebs bekämpfende T-Zellen fernhält. Er trug zudem Signale von Immunsuppression und höhere Werte bei Messgrößen, die auf Resistenz gegenüber Immuntherapie hinweisen. Der Subtyp mit besserer Prognose wies eine schwächere Matrixbildung, günstigere Zusammensetzungen von Immunzellen wie zytotoxischen und Helfer-T-Zellen sowie Werte auf, die auf eine größere potenzielle Empfindlichkeit gegenüber immunbasierten Behandlungen hindeuten.
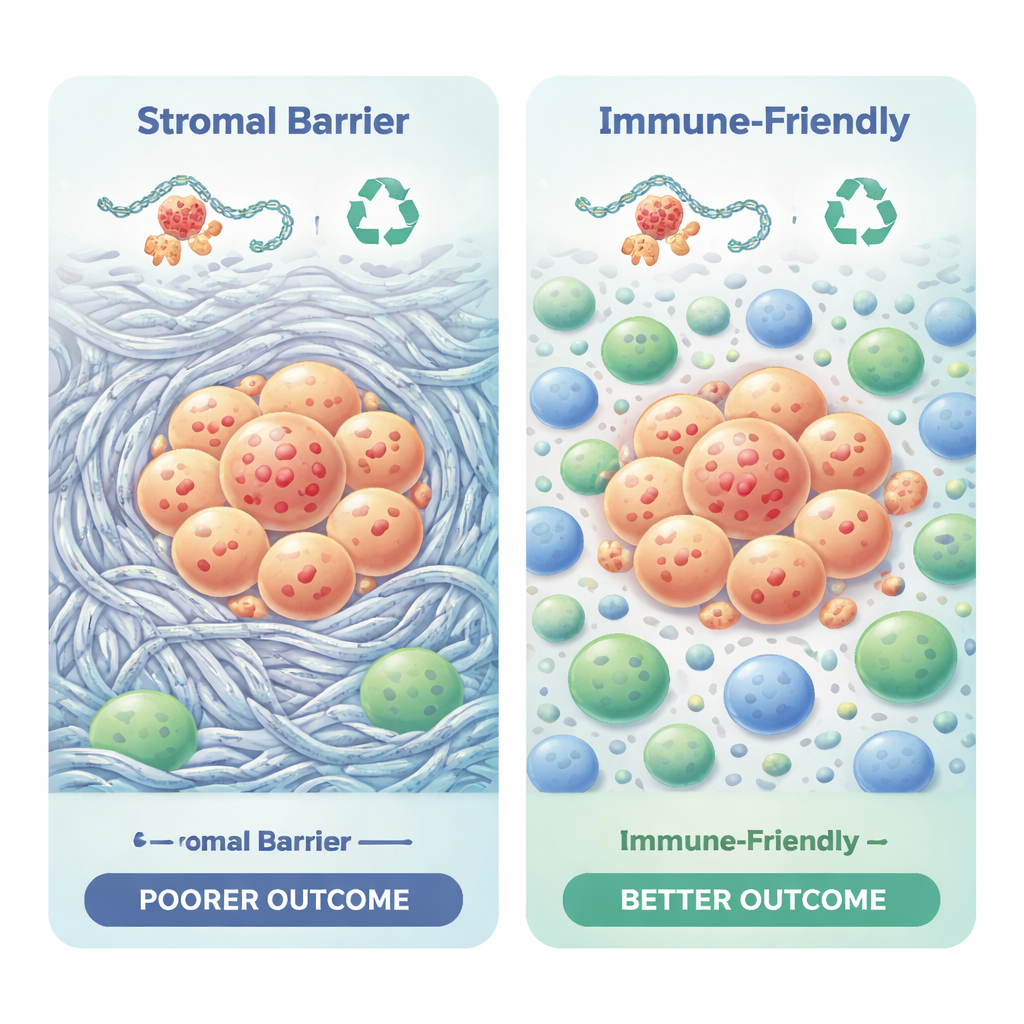
Wichtige Strukturgene als Warnsignale
Um von allgemeinen Mustern zu praxisnahen Markern zu gelangen, bauten die Autorinnen und Autoren Netzwerke interagierender Proteine auf und suchten nach zentralen „Hub“-Genen. Sie identifizierten neun Gene, die vor allem an Aufbau und Umbau des umgebenden Gewebegerüsts beteiligt sind, darunter mehrere Kollagene und Moleküle wie Fibronectin und Periostin. Eine hohe Aktivität einiger dieser Gene, insbesondere BGN, FN1 und POSTN, signalisierte in zwei unabhängigen Patientengruppen durchgängig ein schlechteres Überleben. Diese Hub-Gene stehen an der Schnittstelle von mechanischer Steifheit, chemischer Signalgebung und Anlockung von Immunzellen und sind daher vielversprechende Kandidaten für künftige Tests, die helfen könnten, das Risiko vorherzusagen oder Therapieentscheidungen zu leiten.
Was das für die Zukunft bedeutet
Diese Arbeit ändert die Behandlung von Patientinnen und Patienten noch nicht, da sie auf computergestützten Analysen vorhandener Daten und nicht auf neuen klinischen Studien beruht. Dennoch liefert sie eine klare Kernaussage für Nicht-Spezialisten: Wie ein Darmtumor sein Proteinrecycling handhabt und seine lokale Umgebung umgestaltet, scheint mitzuentscheiden, ob das Immunsystem Zugang findet und den Tumor angreifen kann. Tumoren mit stark gestörtem Proteinkontrollsystem und einer dicken, faserigen Hülle halten Immunzellen eher ab und sind mit schlechteren Ergebnissen verbunden, während Tumoren mit weniger Vernarbung und offenerem Zugang für Immunzellen besser abschneiden. Künftig könnten Kombinationen aus Wirkstoffen, die DNA-Reparatur oder die fibröse Matrix gezielt angreifen, zusammen mit Immuntherapie besonders hilfreich für die in dieser Studie definierte Hochrisikogruppe sein.
Zitation: Xu, Y., Mo, Z., Jiang, Q. et al. Deubiquitination-related genes define immune subtypes of colorectal cancer and are associated with prognosis and immunotherapy-related signatures. Sci Rep 16, 4862 (2026). https://doi.org/10.1038/s41598-026-35271-5
Schlüsselwörter: Darmkrebs, tumormikroumgebung, Immunsubtypen, Proteinabbau, Immuntherapie