Clear Sky Science · de
Störung der Zink‑Homöostase reduziert Histon‑Acetylierungsniveaus in normalen und Tumorzellen
Wenn ein nützliches Metall schädlich wird
Zink ist vor allem als Nährstoff in Multivitaminpräparaten bekannt, der unser Immunsystem und die Wundheilung unterstützt. Innerhalb unserer Zellen muss Zink jedoch in einem sehr engen „gerade richtig“-Bereich gehalten werden. Diese Studie zeigt, dass zu hohe Zinkspiegel in Zellen wichtige Gene stillschweigend abschalten können, indem sie die DNA‑Verpackung straffer machen, und sogar Zellen in einen Selbstreinigungsprozess namens Autophagie treiben können. Da Zinkpräparate, gegen Schuppen eingesetzte Inhaltsstoffe und experimentelle Krebsmedikamente alle den Zinkhaushalt verändern können, ist das Verständnis dieses verborgenen Kontrollsystems sowohl für die alltägliche Gesundheit als auch für künftige Therapien bedeutsam.
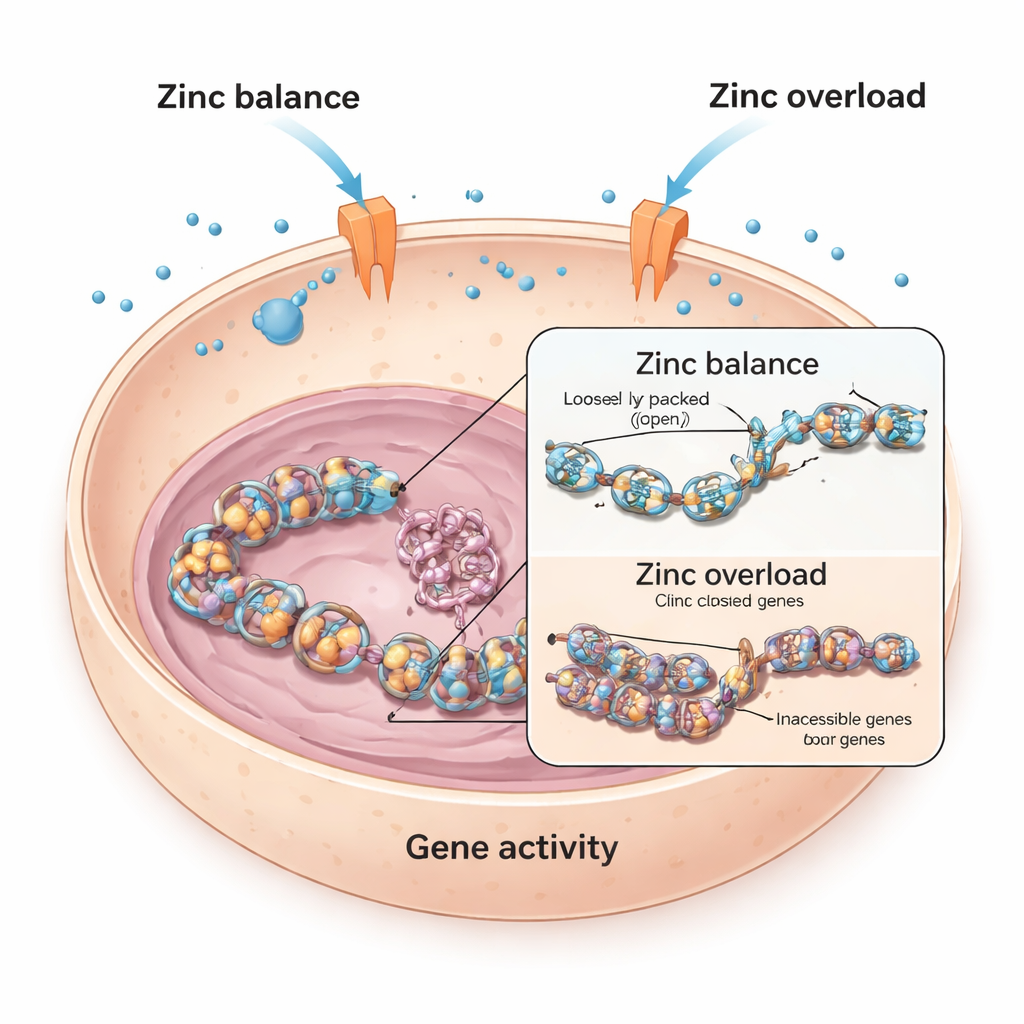
Zink innerhalb lebender Zellen ausbalancieren
Jede Zelle ist auf Zink angewiesen, das tausenden Proteinen hilft, ihre Aufgabe zu erfüllen. Um sowohl Mangel als auch Überladung zu vermeiden, nutzen Zellen spezielle „Tore“ in ihren Membranen, sogenannte Zinktransporter, um Zink hinein und heraus zu bewegen. Die Forschenden begannen mit Herzmuskelzellen von Maus und Mensch und untersuchten, was passiert, wenn diese Zellen zusätzlichem Zink ausgesetzt werden. Sie fanden, dass bei Maus‑Herzmuskelzellen hohe Zinkspiegel die Aktivität eines wichtigen herzbezogenen Gens namens Bmp4 stark reduzierten, das die Herzentwicklung und -funktion mitsteuert. Im Gegensatz dazu waren menschliche Herzzellen deutlich weniger betroffen, was darauf hindeutet, dass verschiedene Zelltypen sich auf unterschiedliche Weise gegen Zinküberladung schützen.
Wie Zink die DNA‑Verpackung strafft
Um aufzudecken, wie Zink Gene wie Bmp4 stilllegt, untersuchte das Team Histone, die spulartigen Proteine, um die DNA gewickelt ist. Wenn kleine chemische Gruppen, sogenannte Acetylgruppen, an Histone angeheftet werden, wird die DNA lockerer und leichter lesbar; werden diese Gruppen entfernt, verpackt sich die DNA enger und Gene lassen sich schwerer aktivieren. Die Studie zeigte, dass überschüssiges Zink in Maus‑Herzmuskelzellen zu einem Rückgang der Histonacetylierung an einer spezifischen Stelle (bekannt als H3K9) führte, was eng mit dem Absinken der Bmp4‑Aktivität korrespondierte. Wirkstoffe, die Histon‑Deacetylasen blockieren, konnten den Zinkeffekt rückgängig machen und Bmp4 wiederherstellen, was darauf hindeutet, dass Zink das Gleichgewicht dieses chemischen Markierungssystems verschiebt.
Zu viel Zink im Inneren, nicht nur außen
Der entscheidende Schritt erwies sich als Zink im wässrigen Zytoplasma der Zelle, nicht nur in der umgebenden Flüssigkeit. Mit einer fluoreszenten Sonde, die in Anwesenheit von freiem Zink aufleuchtet, beobachteten die Forschenden nach Behandlung einen Zinkanstieg innerhalb der Maus‑Herzmuskelzellen. Setzten sie ein Zinktransportsystem ein, das Zink direkt in die Zellen schleust, zeigten sich derselbe Rückgang der Histonacetylierung und der Genaktivität, selbst bei deutlich niedrigerem Zinkgehalt im Außenmedium. Bei menschlichen Herzzellen hingegen passten sich die Membrantransporter rasch an: Einige Zinkeimporteure schalteten ab und Exporteure wurden hochgefahren, wodurch ein starker Anstieg des intrazellulären Zinks verhindert und die Histonacetylierung geschützt wurde. Maus‑Herzmuskelzellen zeigten eine eher „fehlverdrahtete“ Transportantwort, die mehr Zink eindringen ließ und die Genregulation störte.
Von Genkontrolle zur Selbstreinigung in normalen und Tumorzellen
Die Forschenden fragten dann, ob diese zinkgetriebene Straffung der DNA‑Verpackung auf Herzzellen beschränkt ist. Sie testeten mehrere normale menschliche Zelltypen und Krebszelllinien aus Magen, Gebärmutter und Eierstock. Wenn Zink mit Hilfe eines shuttles intrazellulär angereichert wurde, zeigten nahezu alle diese Zellen einen klaren Abfall der Histonacetylierung. In einigen Tumorzellen, etwa Magenkrebszellen, trat dies bereits bei besonders niedrigen Zinkdosen auf, was darauf hindeutet, dass bestimmte Krebsarten ungewöhnlich empfindlich gegenüber Zinkungleichgewicht sind. Das Team verband die verringerte Acetylierung auch mit Autophagie, einem Prozess, bei dem Zellen abgenutzte Bestandteile recyceln. Moderate Anstiege des intrazellulären Zinks förderten die Autophagie, sehr hohe Zinkmengen schwächten sie jedoch schließlich ab, was auf ein enges Fenster hindeutet, in dem Zink zur Feinabstimmung dieses Selbstreinigungswegs genutzt werden könnte.
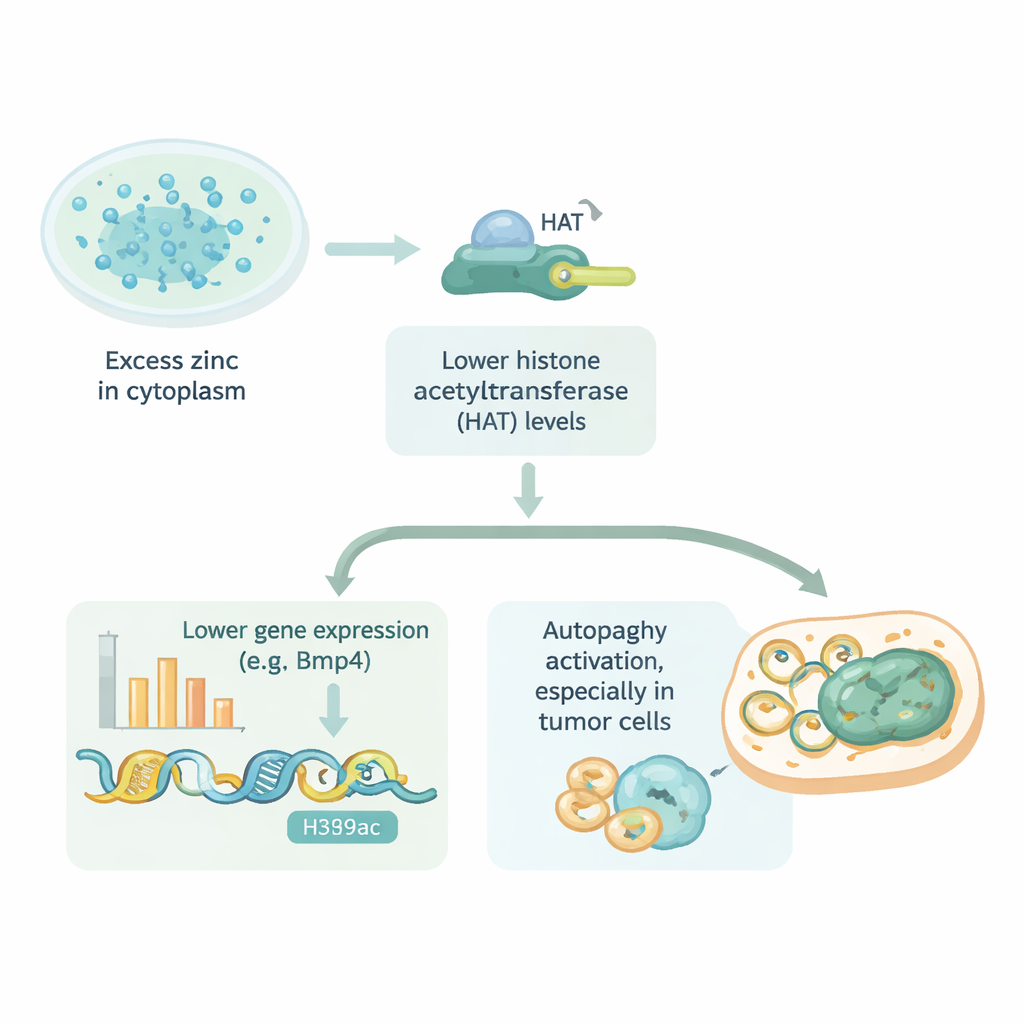
Was das für Gesundheit und Therapie bedeutet
Kurz gesagt zeigt diese Arbeit, dass zu viel Zink innerhalb von Zellen Gene herunterregeln kann, indem es den Zugang zur DNA erschwert, und dass derselbe Weg beeinflusst, wie aktiv Zellen sich selbst säubern. Der Effekt beschränkt sich nicht auf Herzzellen; er scheint in verschiedenen normalen und Krebszellen aufzutreten, obwohl einige besser gegen Zinküberladung schützen als andere. Diese Erkenntnisse deuten darauf hin, dass die winzigen Zinktransporter‑„Tore“ in Zellmembranen vielversprechende Arzneizielkandidaten sein könnten — entweder um gesundes Gewebe vor zinkbedingten Schäden zu bewahren oder um empfindliche Tumorzellen in Richtung Zelltod zu treiben. Zwar stammen die Befunde aus Zellkulturexperimenten, dennoch bieten sie eine neue Perspektive darauf, wie ein alltäglicher Nährstoff die Genaktivität und Krankheit beeinflussen kann, wenn sein empfindliches Gleichgewicht gestört ist.
Zitation: Xu, S., Hu, Y., Tang, C. et al. Disruption of zinc homeostasis reduces histone acetylation levels in normal and tumor cells. Sci Rep 16, 4983 (2026). https://doi.org/10.1038/s41598-026-35270-6
Schlüsselwörter: Zink‑Homöostase, Genregulation, Histonacetylierung, Autophagie, Krebszellen