Clear Sky Science · de
Verschiedene Verteilung von BMPs in verschiedenen periostalen Schichten als Ursache für die inkonsistente osteoinduktive Wirkung von DBM-basierten Produkten
Warum Knochenreparaturmaterialien nicht immer gleich wirken
Wenn Chirurgen ein gebrochenes oder fehlendes Knochenstück auffüllen, greifen sie häufig auf demineralisierte Knochenmatrix (DBM) zurück — aufbereitetes Spenderknochenmaterial, das neues Knochenwachstum anstoßen soll. In der Praxis verhalten sich diese Produkte jedoch sehr unterschiedlich, selbst wenn sie auf dem Etikett ähnlich erscheinen. Diese Studie stellt eine einfache, aber wichtige Frage: Könnten diese Unterschiede daher rühren, dass die heilenden Proteine im Knochen in verschiedenen Schichten ungleich verteilt sind und dass die Messmethoden im Labor dies noch verzerren?
Das Potenzial der körpereigenen Heilproteine
DBM wirkt, weil es natürliche knochenbildende Moleküle trägt, die sogenannten bone morphogenetic proteins (BMPs). Diese Proteine signalisieren benachbarten Stammzellen, sich in Knorpel- und Knochenzellen zu differenzieren und so beschädigte Bereiche wieder aufzubauen. Frühere Arbeiten zeigten, dass DBM-Präparate mit höheren BMP-Gehalten tendenziell mehr Knochen bilden, offenbarten aber auch enorme Schwankungen zwischen Handelsprodukten und sogar zwischen Chargen desselben Produkts. Die Autorinnen und Autoren dieser Studie vermuteten, dass eine bislang wenig beachtete Quelle dieser Variation darin besteht, aus welcher Region eines langen Knochens wie dem Femur das Ausgangsmaterial entnommen wird und wie die BMPs extrahiert und gemessen werden.
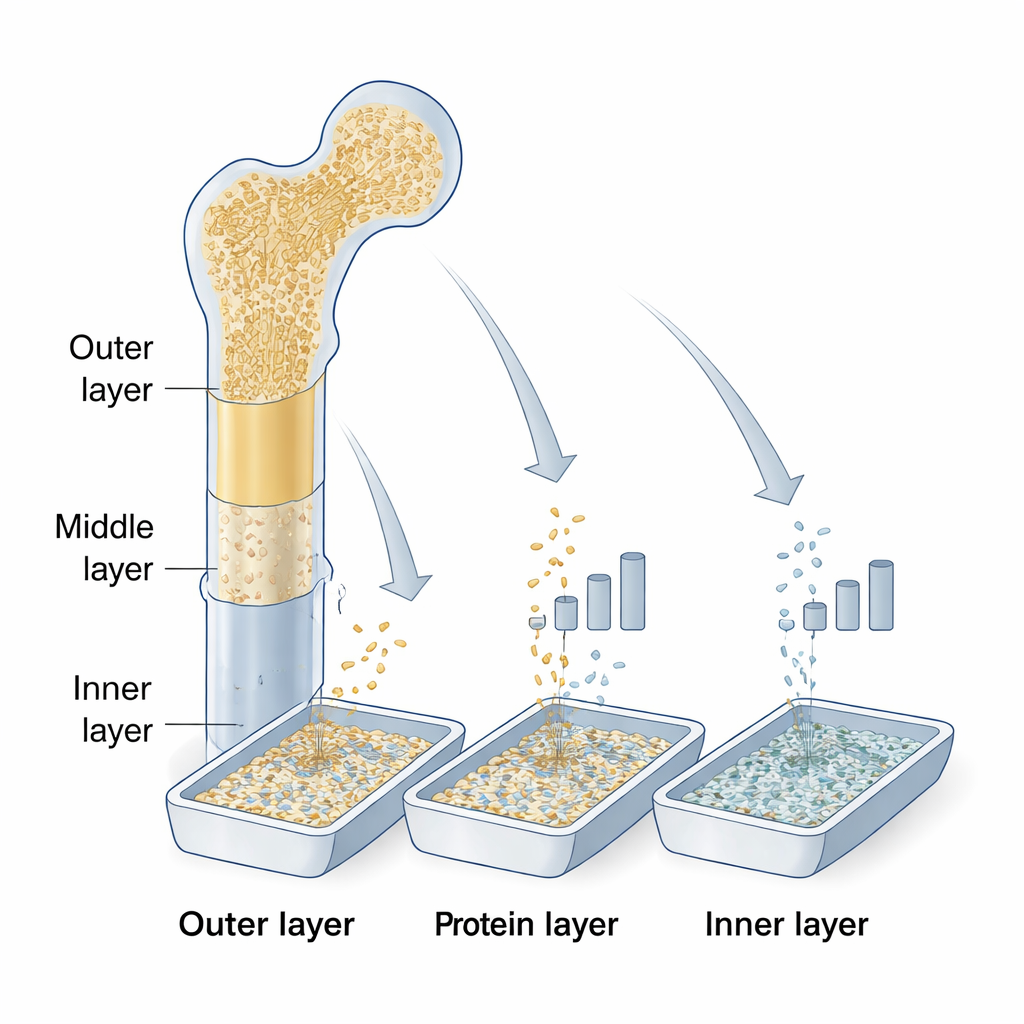
Einen Knochen schichtweise aufschneiden
Anhand eines einzelnen menschlichen Femurs eines Spenders schnitt das Team den harten äußeren Schaft in drei gleich große Schichten: eine äußere Schicht nahe dem Periost (der faserigen Ummantelung des Knochens), eine mittlere Schicht und eine innere Schicht nahe dem Endost sowie dem Markraum. Sie mahlten jede Schicht zu kleinen Partikeln. Einige Partikel aus der äußeren und mittleren Schicht blieben mineralisiert wie gewöhnlicher kortikaler Knochen, während andere — sowie alle Partikel der inneren Schicht — in Säure demineralisiert wurden, um DBM herzustellen. Dieser Prozess entfernt den größten Teil des Calciums, belässt aber die organische Matrix, die BMPs und andere Wachstumsfaktoren hält.
Messung knochenbildender Signale im Labor
Um zu bestimmen, wie viel BMP-2 und BMP-7 jede Probe enthielt, verglichen die Wissenschaftler zwei gängige Extraktionsmethoden. Die eine verwendete Guanidiniumhydrochlorid (GuHCl), eine starke Chemikalie, die Proteine aus der Knochenmatrix löst. Die andere verwendete Kollagenase, ein Enzym, das Kollagen — das Hauptstrukturprotein des Knochens — verdaut. Nach der Extraktion bestimmten sie sowohl die Gesamtproteinmenge als auch spezifische BMP-Level mit Standard-Protein-Assays und hochempfindlichen Antikörpertests (ELISAs) und verglichen die Ergebnisse zwischen den Schichten und Methoden.
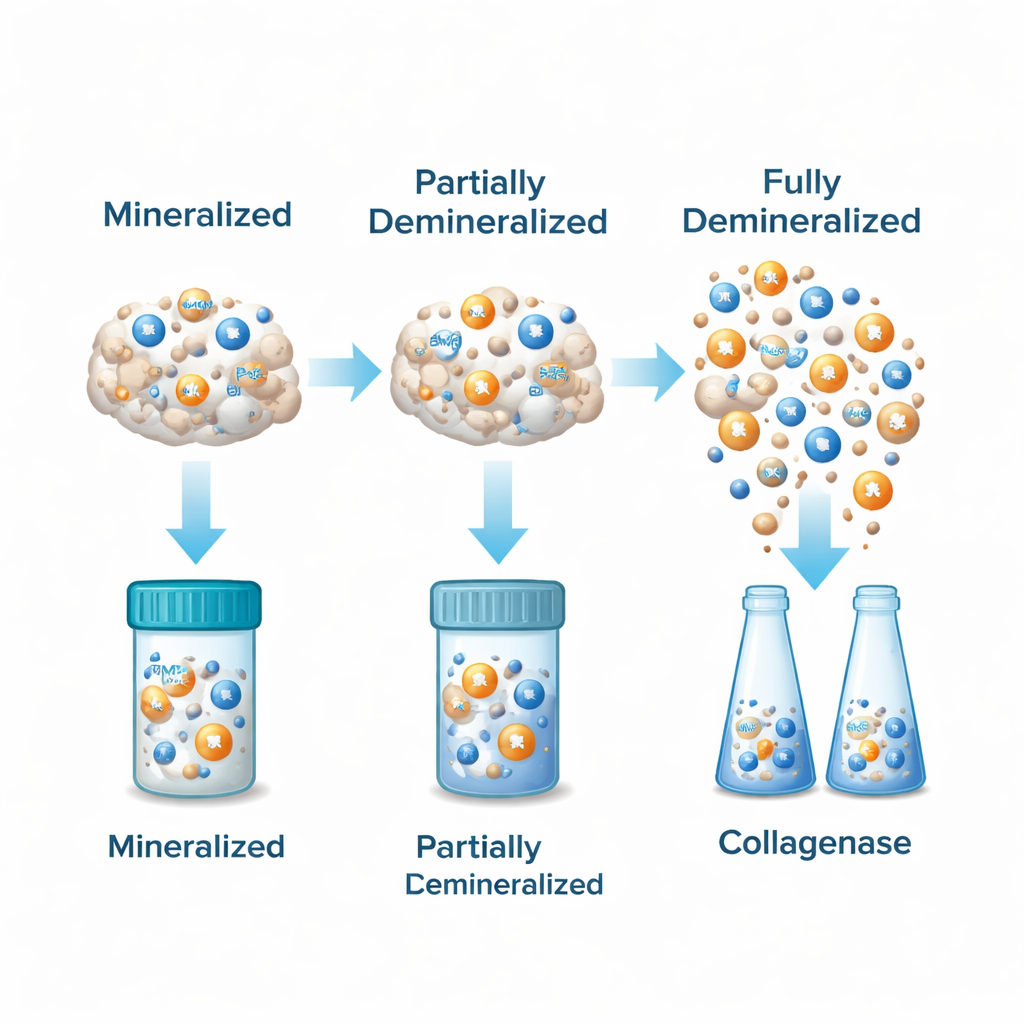
Unregelmäßige Proteinlandkarten innerhalb eines einzelnen Knochens
Die Demineralisierung zeigte einen deutlichen Unterschied: Für jede betrachtete Schicht enthielten die DBM-Proben deutlich mehr nachweisbares BMP-2 und BMP-7 als die entsprechenden mineralisierten Knochenpartikel. Innerhalb der DBM-Gruppe wies die äußere Schicht durchgängig die höchsten Werte beider BMPs auf, die mittlere Schicht hatte etwas weniger und die innere Schicht die geringsten Mengen. Dieses Muster blieb bestehen, unabhängig davon, ob GuHCl oder Kollagenase verwendet wurde. Die beiden BMPs schwankten stark linear miteinander — Proben, die reich an BMP‑2 waren, enthielten fast immer auch mehr BMP‑7 — was zeigt, dass diese wichtigen Wachstumss ignale im Knochen tendenziell gemeinsam variieren.
Wenn die Testmethode die Antwort verändert
Auch die Extraktionsmethode beeinflusste die Ergebnisse. GuHCl gewann dramatisch mehr BMP-2 und BMP-7 als Kollagenase, in einigen Fällen mehr als zehn- bis hundertfach, obwohl Kollagenase gelegentlich mehr Gesamtprotein ergab. Das bedeutet, dass routinemäßige Labortests die knochenbildende Potenz eines DBM-Produkts unterschätzen oder falsch einschätzen können, wenn sie eine weniger effiziente Extraktionsmethode verwenden. Da klinische Produkte aus Mischungen von Knochen unterschiedlicher Schichten und Spender hergestellt werden, kann eine solche verborgene Variabilität im BMP-Gehalt unmittelbar in unvorhersehbare Leistungsfähigkeit beim Einbau in Patienten übersetzen.
Was das für Patientinnen, Patienten und Chirurgen bedeutet
Für Nicht‑Fachleute ist die Schlussfolgerung klar: Nicht alle Knochenersatzstoffe sind gleichwertig, selbst wenn sie aus derselben Knochenart stammen. Die äußeren Bereiche langer Knochen enthalten natürlicherweise mehr der Proteine, die neues Knochenwachstum auslösen, und starke chemische Extraktion macht deutlich mehr dieser Signale sichtbar als schonendere Enzymmethoden. Diese eingebauten Unterschiede helfen zu erklären, warum DBM-Produkte manchmal Knochendefekte gut heilen und manchmal versagen. Bessere Kontrolle darüber, aus welchen Regionen Spenderknochen entnommen werden und wie deren Proteingehalt getestet wird, könnte zukünftige Knochenersatzmaterialien verlässlicher und wirksamer machen.
Zitation: Zhao, Yj., Xue, Y., Sun, S. et al. Various distribution of BMPs in different periosteal layers contributing to inconsistent osteoinductivity of DBM-based products. Sci Rep 16, 5279 (2026). https://doi.org/10.1038/s41598-026-35269-z
Schlüsselwörter: Knochenersatz, demineralisierte Knochenmatrix, knochenmorphogenetisches Protein, Knochenheilung, Orthopädie