Clear Sky Science · de
Stoffwechselumschaltung verbessert die Resistenz gegen oxidativen Stress in differenzierenden Kardiomyozyten
Warum der Kampf der Herzzellen mit Sauerstoff wichtig ist
Jeder Herzschlag beruht auf spezialisierten Muskelzellen, den Kardiomyozyten. Während des Wachstums durchlaufen diese Zellen einen dramatischen Wandel: Sie wechseln von einer sauerstoffarmen, zuckerbasierten Umgebung im Mutterleib in eine sauerstoffreiche Welt nach der Geburt. Sauerstoff ist lebenswichtig, erzeugt aber auch schädliche Nebenprodukte, die DNA beschädigen und Zellen töten können. Diese Studie untersucht, wie sich reifende Herzzellen metabolisch umstellen, damit sie mehr Sauerstoff verarbeiten, mehr Energie erzeugen und sich gleichzeitig vor oxidativer Schädigung schützen können — Erkenntnisse, die künftige Behandlungen von Herzerkrankungen und Regenerationsansätze informieren könnten.
Von einfachen Bautrupps zu Energieathleten
Unreife Herzzellen, sogenannte Kardiomyoblasten, sind kleine, sich teilende Zellen, die hauptsächlich auf den Abbau von Glukose zur Energiegewinnung angewiesen sind. Wenn sie sich zu reifen Kardiomyozyten differenzieren, stellen sie die Teilung ein und vergrößern sich, wobei sie oft zu mehrkernigen, länglichen Zellen fusionieren, die besser für kraftvolle Kontraktionen geeignet sind. Mit hochauflösender Mikroskopie beobachteten die Forschenden diese Umwandlung über zehn Tage in einem Zellmodell im Labor. Marker für Zellproliferation sanken, während sich die Zellen streckten und sich zu faserigen, herzähnlichen Strukturen umorganisierten — ein Hinweis darauf, dass sie in einen erwachseneren, kontraktilen Zustand übergingen. 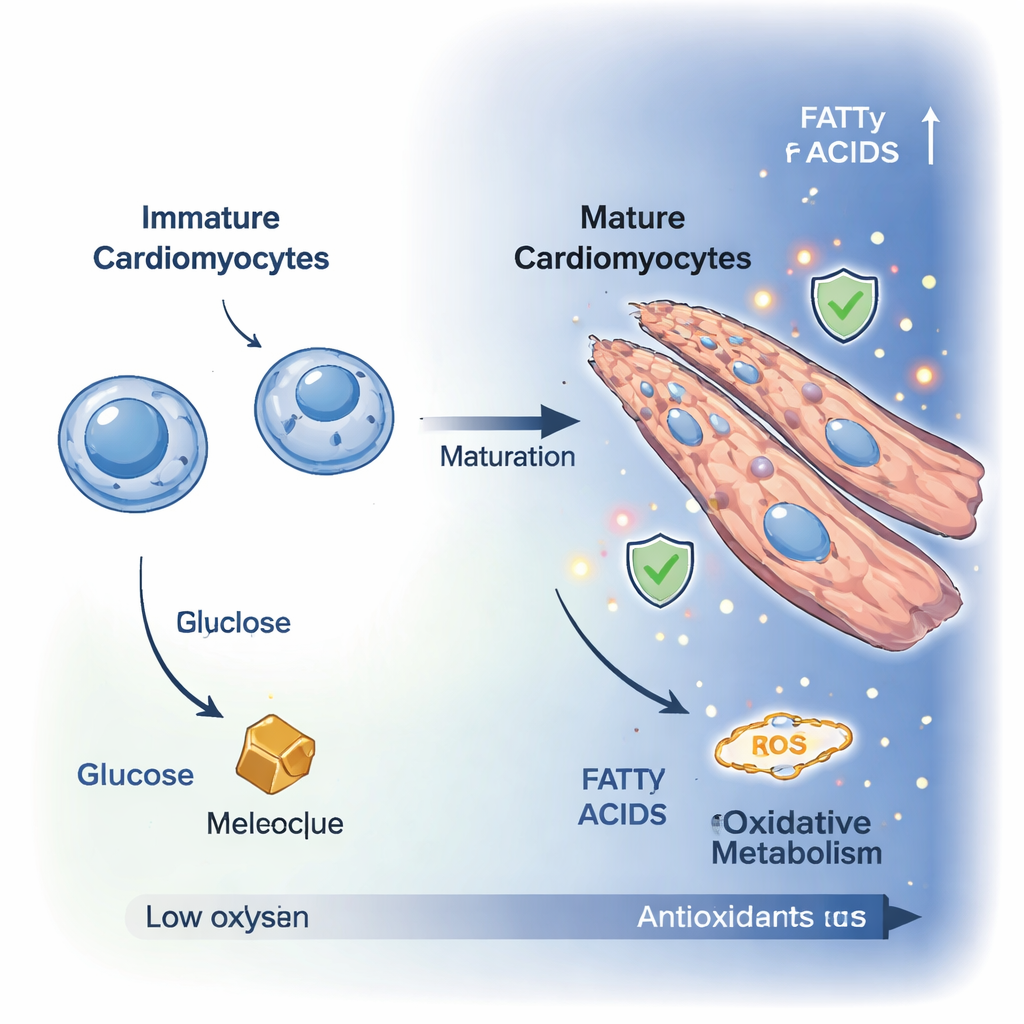
Andere Brennstoffe und neue Energiewege
Um zu verstehen, was unter der Haube geschieht, maßen die Forschenden hunderte kleiner Moleküle in den Zellen und nutzten fortgeschrittene Bildgebung der natürlichen Zellfluoreszenz, um den Energieverbrauch in Echtzeit zu verfolgen. Zusammen zeigten diese Techniken einen klaren Wandel von einem glykolytischen Zustand, in dem die Zellen überwiegend Glukose verbrennen, hin zu einem oxidativen Zustand, der von mitochondrialer Atmung dominiert wird. Die Spiegel von Glukose und Fruktose fielen, während Zwischenprodukte des Tricarbonsäure-(TCA-)Zyklus — wie Zitronensäure, Malat und Oxoglutarat — zunahmen. Die Pfadanalyse zeigte stärkere Aktivität in Strecken, die Brennstoff in die Mitochondrien einspeisen, einschließlich der Malat–Aspartat-Shuttle und des Aminosäureabbaus, was darauf hindeutet, dass reife Kardiomyozyten ihre Brennstoffoptionen erweitern und Energie effizienter zu ihren Kraftwerken leiten.
Mit mehr Sauerstoff leben — und mehr Stress
Effizienteres Verbrennen von Brennstoff in den Mitochondrien hat seinen Preis: eine höhere Produktion reaktiver Sauerstoffspezies (ROS), chemisch aggressive Moleküle, die Lipide, Proteine und DNA schädigen können. Die Forschenden stellten fest, dass die Mitochondrien mit der Reifung der Kardiomyozyten größer und verlängerter wurden und Marker für oxidativen Stress zunahmen. Fluoreszenzbasierte Bildgebung zeigte mehr lipofuszinähnliche Granulate, ein Kennzeichen oxidierter Lipide, und ein nukleärer Sensor ergab höhere ROS-Werte in differenzierten Zellen. Die Metabolomik wies auf Veränderungen im Glutathionstoffwechsel hin, einem zentralen Antioxidationssystem, das das Molekül Glutathion — aufgebaut aus Aminosäuren wie Glutamat und Glycin — nutzt, um ROS zu neutralisieren. Diese Befunde deuten darauf hin, dass Herzzellen mit gesteigerter oxidativer Energiegewinnung zugleich ihre antioxidativen Wege anpassen, um Schäden in Schach zu halten. 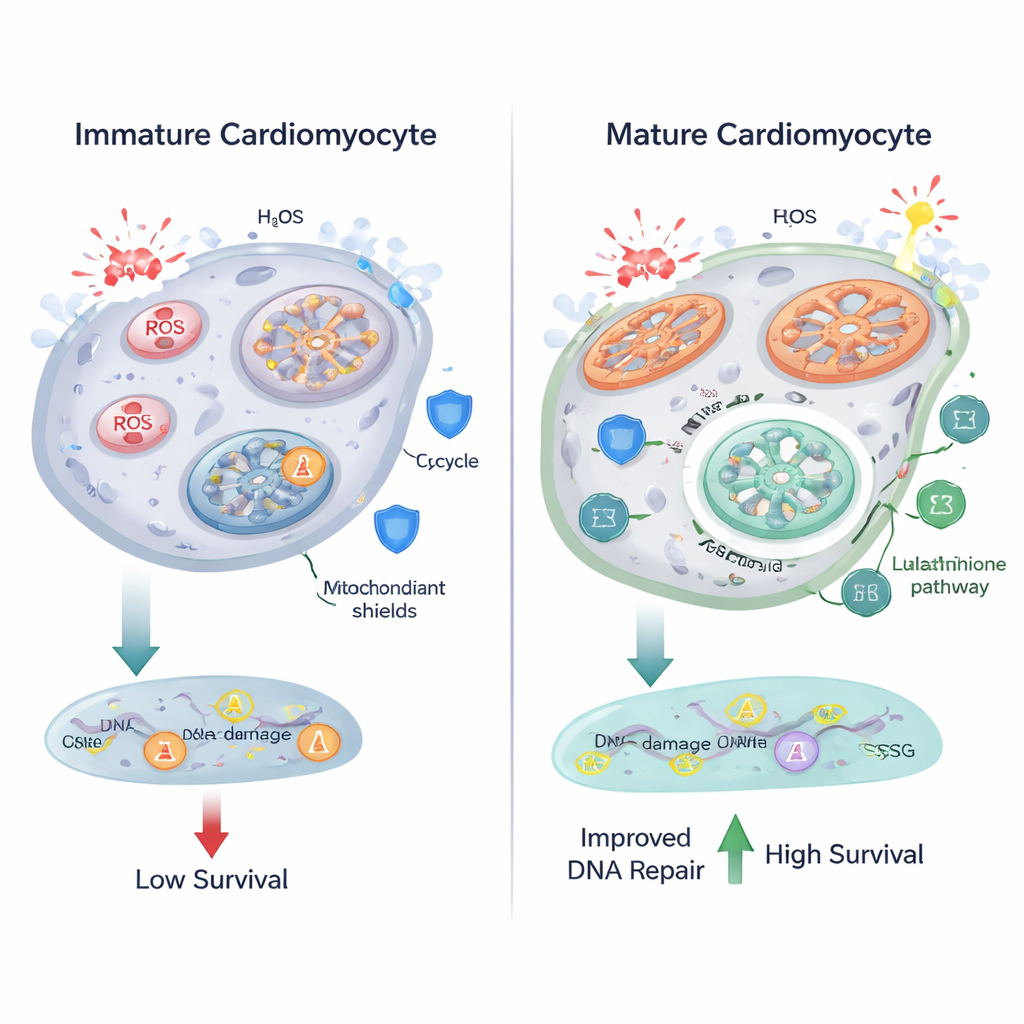
Schäden begrenzt, Abwehrkräfte gestärkt
Überraschenderweise zeigten differenzierte Kardiomyozyten trotz höherer ROS-Werte nicht mehr DNA-Brüche als ihre unreifen Gegenstücke, gemessen anhand von γ-H2AX-Foci, einem sensitiven Marker für DNA-Schäden. Als die Forschenden die Zellen mit Wasserstoffperoxid, einem starken Oxidationsmittel, herausforderten, akkumulierten sowohl unreife als auch reife Zellen ROS und DNA-Brüche — doch die reifen Zellen schnitten besser ab. Im Verhältnis zu ihren höheren ROS-Werten zeigten sie anteilig weniger DNA-Läsionen, waren weniger geneigt, zelltodverknüpfte Signalwege wie PUMA zu aktivieren, und wiesen deutlich höhere Überlebensraten auf. Diese Ergebnisse deuten darauf hin, dass sich maturing Kardiomyozyten nicht nur metabolisch anpassen, sondern auch ihre DNA-Reparatur- und Überlebensmechanismen aufrüsten, sodass sie härtere oxidative Bedingungen aushalten können.
Was das für den Schutz des Herzens bedeutet
Einfach gesagt zeigt diese Studie, dass Herzzellen beim Erwachsenwerden lernen, heißer zu laufen, ohne zu verbrennen. Sie wechseln von einem zuckerlastigen, sauerstoffarmen Lebensstil zu einem sauerstoffintensiven, von Mitochondrien getragenen Stoffwechsel und bauen gleichzeitig bessere Schutzschilde und Reparaturmechanismen auf, um mit oxidativem Stress fertigzuwerden. Das Verständnis dieses fein austarierten Gleichgewichts zwischen Energieproduktion und Selbsterhalt könnte Wissenschaftlern helfen, Strategien zu entwickeln, um geschädigtes erwachsenes Herzgewebe widerstandsfähiger zu machen oder Stammzellen in sicherere, dauerhaftere Kardiomyozyten für regenerative Therapien zu lenken.
Zitation: Novais, L.B., Rodrigues, B.R.I., Pereira, F.O.B. et al. Metabolic reprogramming enhances oxidative stress resistance in differentiating cardiomyocytes. Sci Rep 16, 5534 (2026). https://doi.org/10.1038/s41598-026-35263-5
Schlüsselwörter: Kardiomyozytendifferenzierung, oxidativer Stress, Mitochondrien, Zellstoffwechsel, Herzerkrankung