Clear Sky Science · de
Alzheimer-Vorhersage mittels Deep Learning und XAI-basierter interpretierbarer Merkmalsauswahl aus Blut-Genexpressionsdaten
Warum diese Forschung wichtig ist
Die Alzheimer-Krankheit raubt Menschen schrittweise Erinnerung und Unabhängigkeit, doch die heute genauesten Tests erfordern oft Hirnscans oder Lumbalpunktionen, die teuer, invasiv und schwer wiederholbar sind. Diese Studie untersucht eine weniger belastende Alternative: eine einfache Blutentnahme kombiniert mit fortschrittlicher Computeranalyse, um Muster in der Genaktivität zu erkennen, die auf Alzheimer hinweisen könnten, und so womöglich frühere und leichter zugängliche Diagnosen zu ermöglichen.
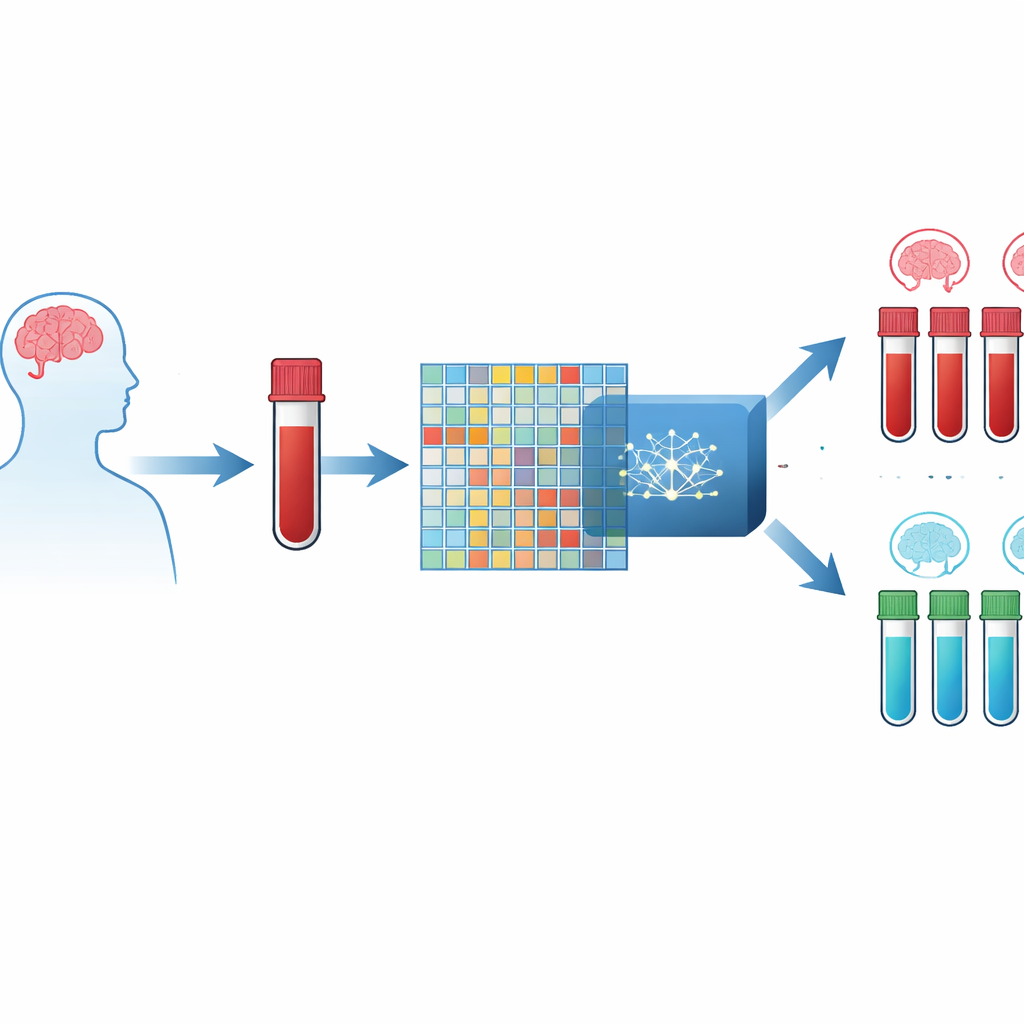
Ein Bluttest statt eines Hirnscans
Die Autoren konzentrieren sich auf geringe Änderungen darin, wie Gene in Blutzellen ein- oder ausgeschaltet werden. Moderne Laborchips können die Aktivität von Tausenden Genen gleichzeitig messen und erzeugen so für jede Person eine umfangreiche Zahlentabelle. Die Herausforderung besteht darin, dass es deutlich mehr Genmessungen als Patienten gibt, was Computermodelle leicht fehlleiten kann. Um das zu umgehen, kombinierten die Forschenden drei große öffentliche Datensätze mit Blutproben von Alzheimer-Patienten und gesunden Freiwilligen und schufen so eine integrierte Ressource mit über zwölftausend gemeinsamen Genen, die an Hunderten von Personen gemessen wurden.
Computern beibringen, wichtige Warnsignale zu erkennen
Anstatt einen Algorithmus alle zwölftausend Gene verarbeiten zu lassen, brachten die Forschenden ihm zunächst bei, eine deutlich kleinere Menge besonders informativer Gene auszuwählen. Sie verglichen mehrere Verfahren, darunter einfache statistische Tests, schrittweise Verfahren, die weniger nützliche Gene entfernen, und Ansätze, die die Auswahl direkt in das Modell integrieren. Diese „Feature-Selection“-Werkzeuge reduzierten die Liste auf einige Hundert bis etwas über tausend Gene, die Patienten am besten von gesunden Kontrollen unterschieden. Die verkleinerten Gen-Sets halfen, das Überanpassen an Rauschen zu vermeiden, und verbesserten die Leistung auf bisher ungesehenen Daten.
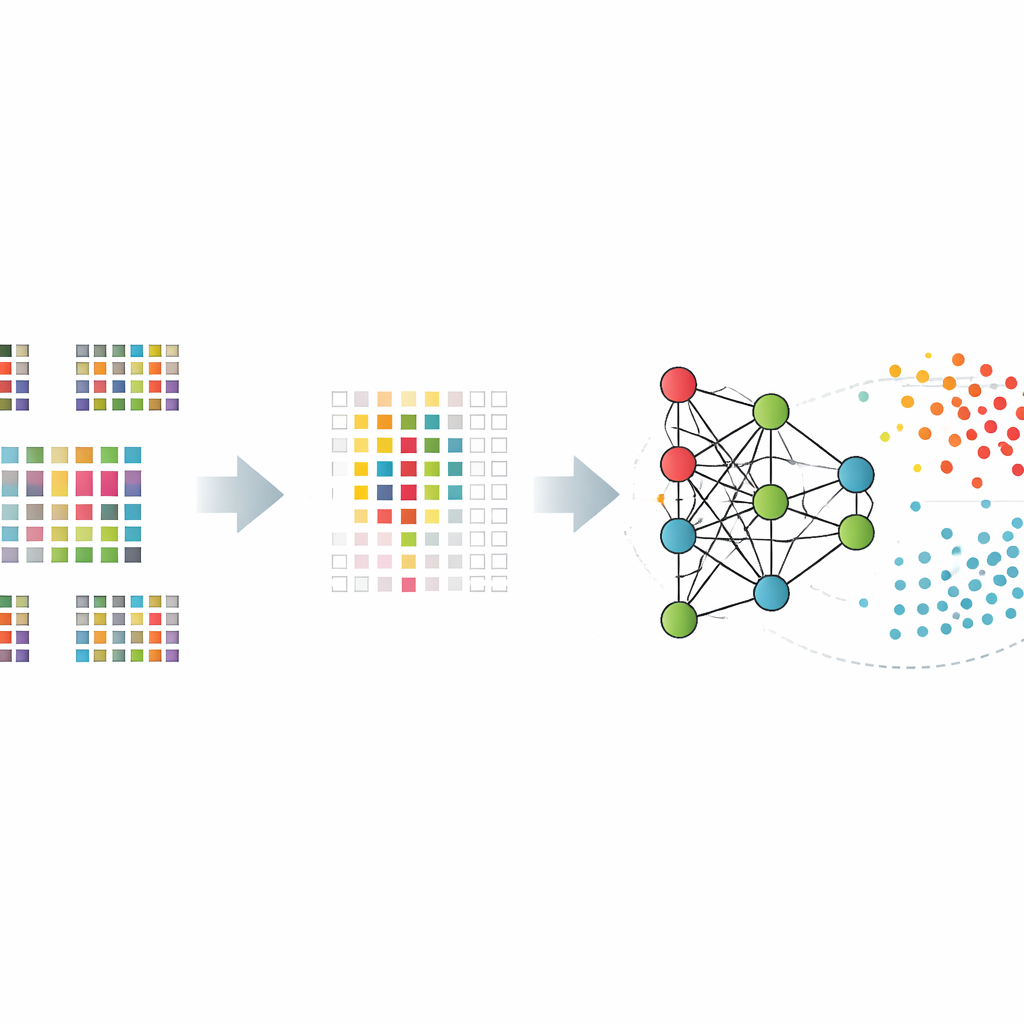
Den Black Box verstehen
Um blindes Vertrauen in eine Black-Box-Vorhersage zu vermeiden, nutzten die Forschenden Techniken der erklärbaren künstlichen Intelligenz, um zu verstehen, welche Gene am wichtigsten waren und wie sie jede Entscheidung beeinflussten. Eine Methode namens SHAP, entlehnt der Spieltheorie, bewertet den Beitrag jedes Gens zum Endergebnis für jede Person. Durch Anwendung auf ihre bestperformenden Modelle hoben die Autorinnen und Autoren eine Kerngruppe von Genen hervor, deren Aktivitätsmuster zuverlässig in Richtung Alzheimer- oder gesund-Klassifikation wogen. Viele dieser Gene wurden bereits mit Gehirngesundheit oder Immunfunktion in Verbindung gebracht, was der inneren Logik des Modells biologische Glaubwürdigkeit verleiht.
Mehr Aussagekraft durch synthetische Patienten
Selbst nach dem Zusammenführen der Datensätze blieb die Zahl echter Blutproben moderat. Um ihre Modelle zu stärken, trainierten die Autorinnen und Autoren einen spezialisierten Typ neuronaler Netze, genannt generative adversariale Netzwerke, um realistische synthetische Genprofile zu erzeugen, die denen tatsächlicher Patienten ähneln. Diese künstlichen Proben wurden nur zum Trainingsdatensatz hinzugefügt, niemals zum Testdatensatz, sodass die Leistungsüberprüfungen unverfälscht blieben. Mit diesem erweiterten Trainingspool und sorgfältig ausgewählten Genen konnte ein tiefes neuronales Netzwerk Alzheimer-Fälle mit rund 91 % Gesamttrefferquote und 95 % Präzision identifizieren, was bedeutet, dass sehr wenige gesunde Personen fälschlich als krank markiert wurden.
Was die Ergebnisse für Patientinnen und Patienten bedeuten
Die Arbeit deutet darauf hin, dass ein künftiger blutbasierter Test auf Alzheimer, angetrieben von intelligenten Algorithmen, die sowohl Schlüsselgenen auswählen als auch deren Bedeutung erklären, ergänzend wirken oder die Abhängigkeit von teuren Scans und invasiven Verfahren verringern könnte. Während weitere Validierungen an unabhängigen Patientengruppen nötig sind und Unterschiede zwischen Laborverfahren besser kontrolliert werden müssen, zeigt die Studie, dass das Zusammenführen mehrerer Datensätze, das Entfernen unwirksamer Information und das Öffnen der „Black Box“ der KI uns einem praxisnahen, interpretierbaren Bluttest für eine frühere und angenehmere Alzheimer-Erkennung näherbringen kann.
Zitation: Hariharan, J., Jothi, R. Alzheimer’s disease prediction using deep learning and XAI based interpretable feature selection from blood gene expression data. Sci Rep 16, 8022 (2026). https://doi.org/10.1038/s41598-026-35260-8
Schlüsselwörter: Alzheimer-Diagnose, Blut-Biomarker, Genexpression, Deep Learning, erklärbare KI