Clear Sky Science · de
Einfache und effiziente Kotsynthese von Goldnanopartikeln und -nanoclustern zum Nachweis von HPV‑16
Warum es wichtig ist, ein verborgenes Virus zu erkennen
Gebärmutterhalskrebs gehört zu den wenigen Krebsarten, die wir weitgehend verhindern können, wenn Warnsignale früh erkannt werden. Ein Hauptverursacher ist das humane Papillomavirus Typ 16 (HPV‑16), ein häufig sexuell übertragbares Virus, das Zellen über Jahre hinweg unbemerkt schädigen kann, bevor Symptome auftreten. Impfungen helfen, doch viele Frauen weltweit sind nicht geimpft oder haben keinen regelmäßigen Zugang zu Untersuchungen. Diese Studie beschreibt eine einfache Labor‑Methode, die winzige Goldpartikel in einen kostengünstigen Sensor verwandelt, der das genetische Material von HPV‑16 schnell und ohne sperrige Geräte nachweist.
Gold als Krankheitsdetektor
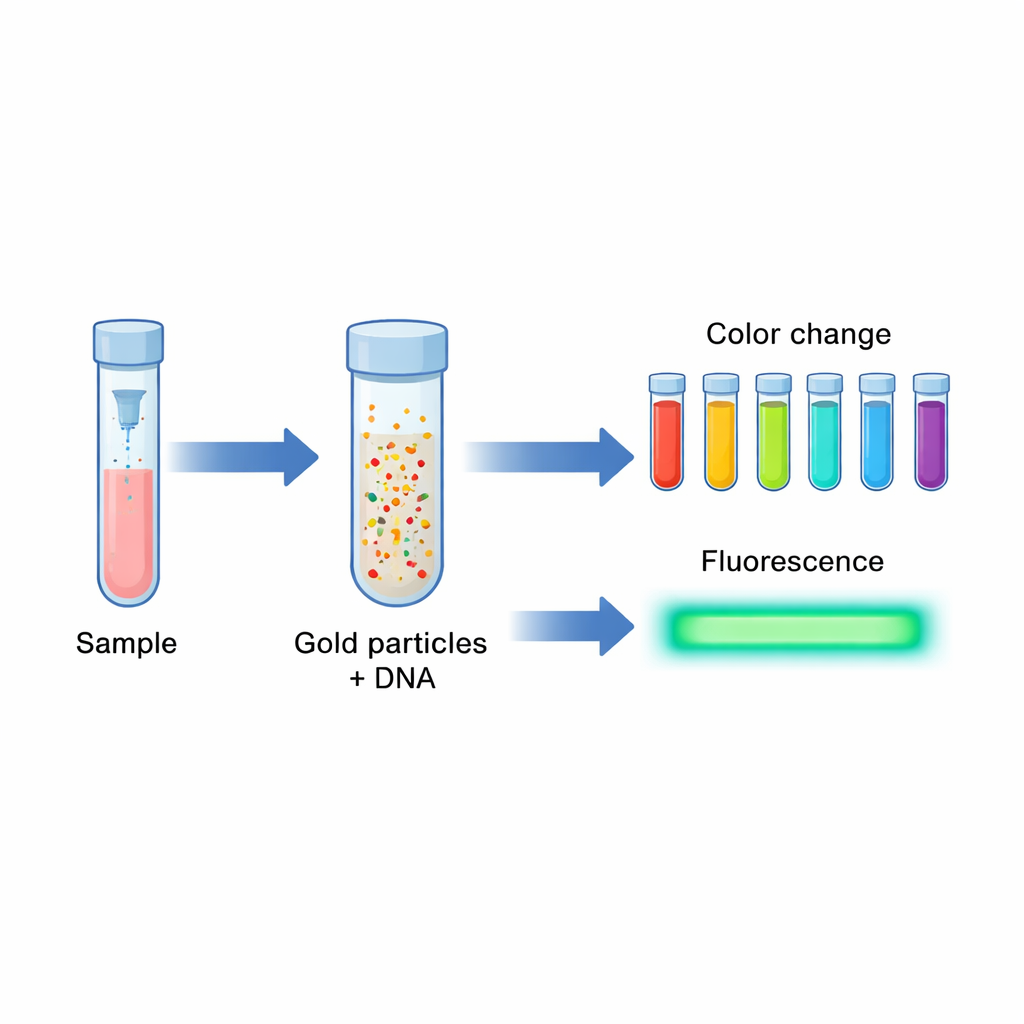
Die Forschenden wollten einen Test entwickeln, der sowohl erschwinglich als auch empfindlich genug ist, um geringe Mengen an HPV‑16‑DNA, dem genetischen Material des Virus, nachzuweisen. Statt auf komplexe Apparate zu setzen, verwendeten sie Gold im Nanobereich — Partikel so klein, dass sie sich anders verhalten als gewöhnliches Metall. Diese Goldnanopartikel und noch kleinere „Nanocluster“ verändern die Farbe und leuchten unter Licht auf sehr spezifische Weise. Indem sie an eine kurze DNA‑Sequenz gekoppelt werden, die einen Teil des HPV‑16‑Genoms erkennt, entstand ein System, bei dem das Vorhandensein des Virus eine sichtbare Farbänderung und ein starkes Lichts Signal auslöst. Diese doppelte Reaktion erleichtert es, positive von negativen Proben zu unterscheiden, selbst für Nicht‑Expertinnen und Nicht‑Experten.
Ein einfaches Rezept, zwei Goldformen
Eine zentrale Neuerung der Arbeit ist, dass sowohl die größeren Goldnanopartikel als auch die ultrasmallen Nanocluster in einem einzigen Schritt hergestellt werden. Das Team nutzte einen kurzen DNA‑Strang, reich an der Base Adenin — im Wesentlichen ein Schwanz aus 20 „A“‑Basen —, gemischt mit einer Goldsalzlösung und einer milden Chemikalie namens HEPES. Der Adenin‑Schwanz bindet natürlicherweise an Goldionen und fördert deren Zusammenlagerung zu etwas größeren Partikeln, die ein kräftiges Rot erzeugen, oder zu sehr winzigen Clustern, die blau‑violett fluoreszieren. Da derselbe DNA‑Strang auch eine Sequenz enthält, die spezifisch an das L1‑Gen von HPV‑16 bindet, wird jedes Goldpartikel mit vielen Kopien einer solchen Sonde beschichtet, die bei Vorhandensein der Virus‑DNA an diese andocken kann.
Den Erreger in Farbe und Licht ablesen
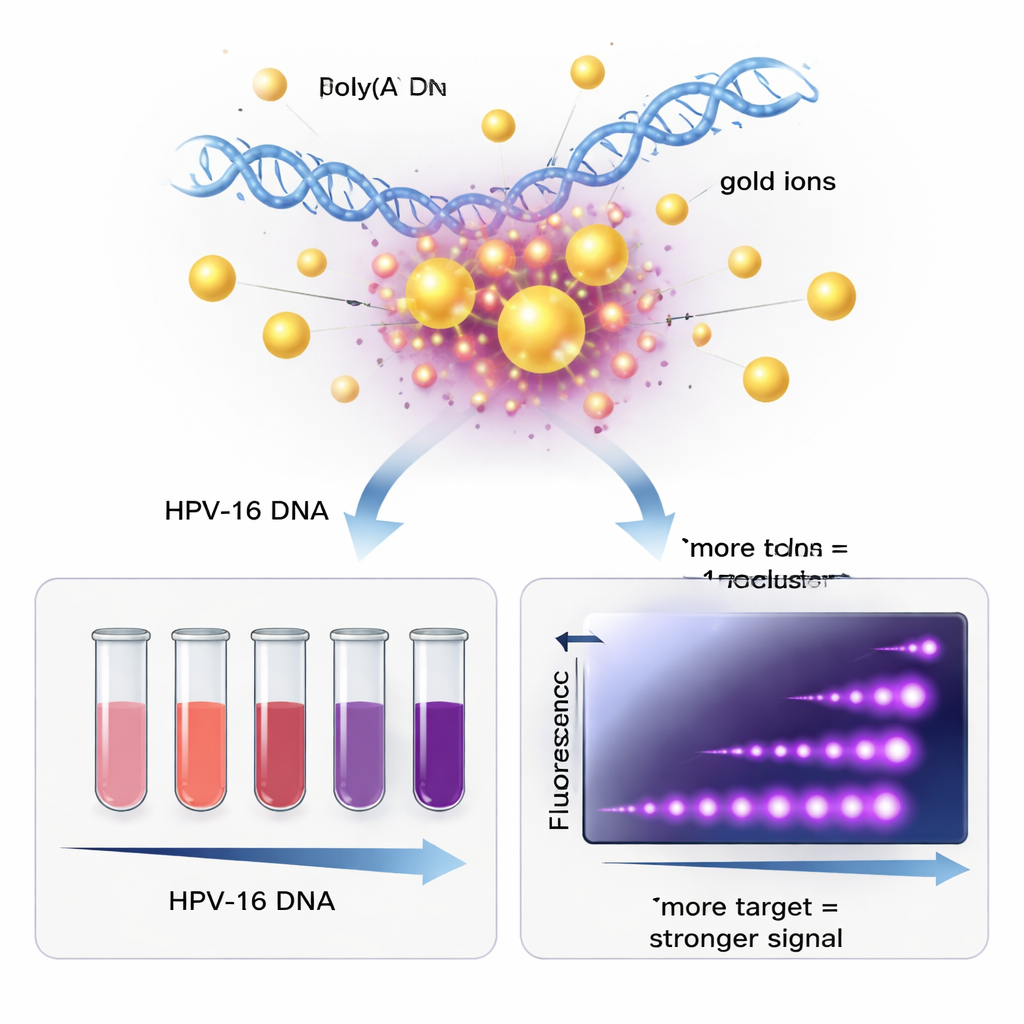
Um den Sensor zu testen, verwendeten die Forschenden ein ringförmiges DNA‑Molekül (ein Plasmid), das das L1‑Gen von HPV‑16 trägt, sowie DNA, die aus echten Patientenproben gewonnen wurde. Sie erhitzten die virale DNA kurz, sodass die Doppelhelix aufging, und kühlten sie dann mit den Gold‑DNA‑Sonden in der Lösung ab. Wenn die Sonde ihre passende HPV‑16‑Sequenz fand, bildete sich eine stabile Doppelstrangstruktur, die an das Gold gebunden blieb. In Probenröhrchen mit dem korrekten Ziel blieb die Lösung klar rot und erzeugte ein starkes Fluoreszenzsignal. In Kontrollen ohne die passende HPV‑16‑Sequenz verklumpten die Goldpartikel, die Farbe verschob sich ins Purpur, und das Lichts Signal blieb schwach. Durch Messung der Veränderung von Farbe und Fluoreszenz konnte das Team abschätzen, wie viel virale DNA in einem praktischen Konzentrationsbereich vorhanden war.
Zusätzlicher Trick: Gold mit enzymähnlichem Verhalten
Die Goldnanopartikel in diesem Sensor ahmen zudem die Aktivität bestimmter natürlicher Enzyme nach. Als die Forschenden einen gebräuchlichen Laborfarbstoff (TMB) und Wasserstoffperoxid hinzufügten, halfen die nicht verklumpten Goldnanopartikel, den Farbstoff in eine tiefblaue Form umzuwandeln. Je mehr HPV‑16‑DNA an die Sonden gebunden war, desto stabiler und stärker voneinander getrennt blieben die Goldpartikel, und desto kräftiger wurde dieses Blau. Das ergab eine zweite, unabhängige Farbablesung — eine, die nicht nur auf der natürlichen Farbe der Partikel beruhte, sondern auf ihrem enzymähnlichen Verhalten. Mithilfe dieses Effekts konnte das Team HPV‑16‑DNA auf ähnlich niedrigen Niveaus nachweisen und bestätigte so, dass beide Farbwege dasselbe Ergebnis liefern.
Was das für künftige Screenings bedeuten könnte
Insgesamt zeigt die Studie, dass eine einfache Mischung aus Gold, Puffer und kurzen DNA‑Strängen in einen zuverlässigen Sensor für ein Hochrisiko‑Krebsvirus verwandelt werden kann. Die Methode detektiert HPV‑16 ohne zusätzliche Markierungen, komplexe Amplifikationsschritte oder teure Instrumente, erreicht dennoch niedrige Nachweisgrenzen und trennt positive von negativen Proben klar. Zwar sind weitere Validierungen in größeren Patientengruppen und in realen klinischen Umgebungen nötig, doch dieser duale Gold‑Sensor weist in Richtung künftiger Screening‑Tools, die in einfachen Laboren — oder möglicherweise in der Nähe des Patienten — eingesetzt werden könnten und dazu beitragen, die Früherkennung von Gebärmutterhalskrebs für mehr Frauen weltweit erreichbar zu machen.
Zitation: Saleh, M.A., Hosseinkhani, S., Nikkhah, M. et al. Simple and efficient co-synthesis of gold nanoparticles and nanoclusters for HPV-16 detection. Sci Rep 16, 4854 (2026). https://doi.org/10.1038/s41598-026-35246-6
Schlüsselwörter: HPV-16, Gebärmutterhalskrebs-Screening, Goldnanopartikel, Biosensor, Nanodiagnostik