Clear Sky Science · de
Föderierte Segmentierung von Lungenknoten mit einer hybriden Transformer–U-Net‑Architektur
Warum das Erkennen winziger Lungentupfer wichtig ist
Lungenkrebs ist weltweit die tödlichste Krebsart, und seine frühesten Warnzeichen – winzige Flecken, sogenannte Knoten, in CT-Aufnahmen – werden leicht übersehen. Radiologen müssen Tausende detaillierter Bilder durchsieben, und das Teilen von Patientendaten zwischen Krankenhäusern, um intelligentere Computer zu trainieren, wird häufig durch strenge Datenschutzvorschriften blockiert. Diese Studie stellt einen Weg vor, wie Krankenhäuser zusammenarbeiten können, um ein System der künstlichen Intelligenz (KI) zu trainieren, das Lungenknoten zuverlässig erkennt, ohne jemals rohe Patientenscans auszutauschen.
Wissen teilen, ohne Scans zu teilen
Moderne CT-Scanner erfassen Lungenstrukturen bis in Bruchteile eines Millimeters, doch diese Präzision erzeugt eine Flut von Bildern, die kein Mensch allein durchsehen kann. Computerunterstützte Werkzeuge können helfen, benötigen aber große, vielfältige Datensätze, um ungewöhnliche Knoten nicht zu übersehen. Gesetze wie HIPAA und DSGVO verhindern, dass Krankenhäuser Patientendaten einfach an einem Ort zusammenlegen. Die Autor:innen nutzen eine Strategie namens föderiertes Lernen, um dieses Dilemma zu lösen. Jedes Krankenhaus trainiert lokal eine Kopie desselben Modells an seinen eigenen CT-Aufnahmen und sendet danach nur die gelernten Modellparameter, nicht die Bilder selbst, an einen zentralen Server. Der Server mittelt diese Parameter zu einem verbesserten „globalen“ Modell und schickt es zurück, sodass alle Standorte voneinander profitieren, während die Patientendaten im Haus bleiben. 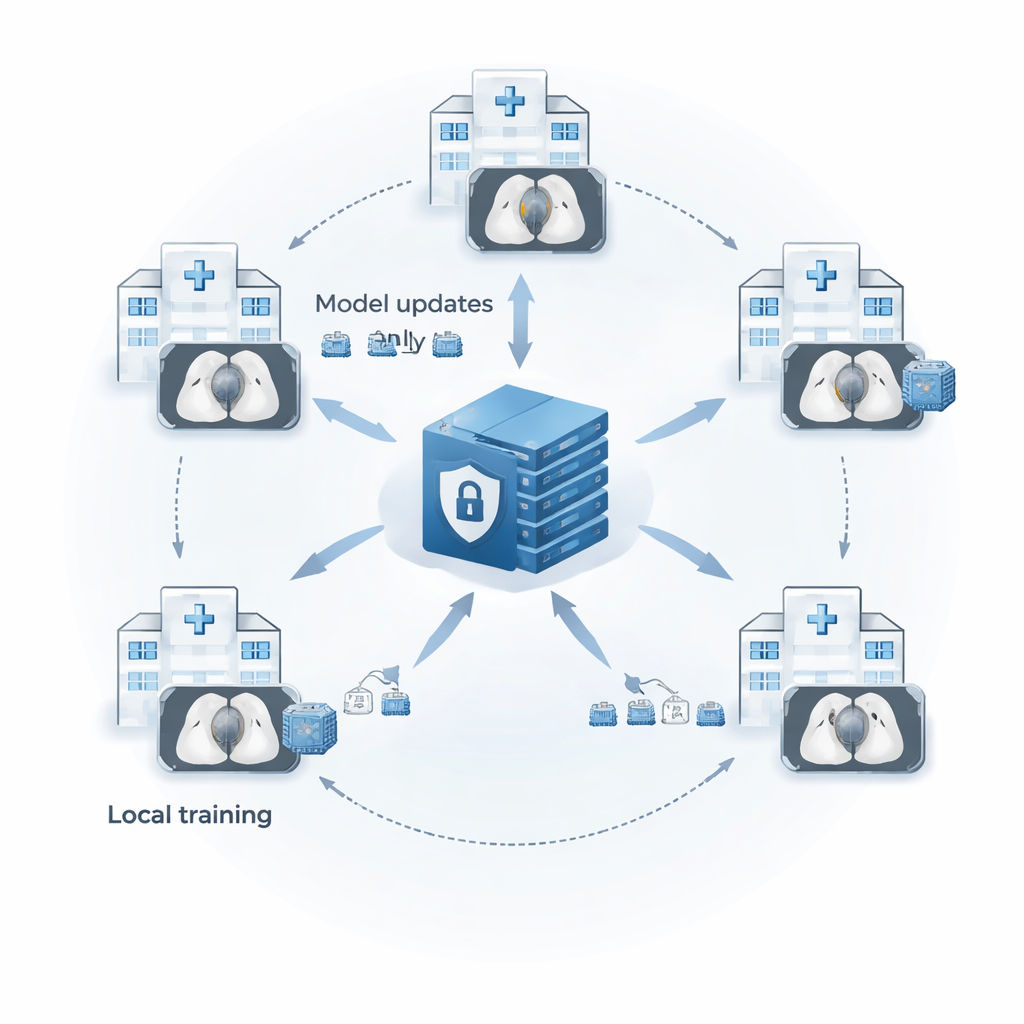
Die Bilder vor dem KI‑Training bereinigen
Die Forschung konzentriert sich auf „solide“ Lungenknoten zwischen 15 und 25 Millimetern, die klinisch relevant sind, in jeder CT-Schicht aber nur wenige Pixel einnehmen und daher leicht übersehen werden können. Bevor etwas gelernt wird, durchläuft jede CT‑Schicht einen zweistufigen Bereinigungsprozess. Zuerst hellt eine Kontrastverbesserungsmethode namens CLAHE schwache Knoten auf, ohne Rauschen zu verstärken, sodass subtile Flecken deutlicher hervortreten. Danach werden die Bilder so skaliert, dass alle Pixelwerte zwischen 0 und 1 liegen, wodurch das Modell eine einheitliche Helligkeitsskala über Scans von verschiedenen Geräten und Krankenhäusern hinweg erhält. Diese standardisierte Vorverarbeitung hilft der KI, auf winzige, kontrastarme Knoten zu achten, statt sich von Scannerartefakten verwirren zu lassen.
Zwei Sichtweisen kombinieren: Detailnähe und Gesamtzusammenhang
Im Kern des Systems steht ein hybrides Netzwerk, das zwei leistungsfähige Konzepte moderner KI verbindet: das U-Net, das bei der Markierung von Objekten in Bildern brilliert, und den Transformer, ursprünglich für Sprache entwickelt und inzwischen breit im Bereich Vision eingesetzt. Der U-förmige Teil des Modells komprimiert das Bild zunächst durch Schichten kleiner Filter, die lokal Texturen – Kanten, Punkte und feine Begrenzungen – erfassen, und rekonstruiert dann eine Maske in voller Größe, die anzeigt, welche Pixel zu einem Knoten gehören. Residualverbindungen und Skip‑Links transportieren feine Details durch das Netzwerk, damit sie nicht verloren gehen. In der Mitte dieses U sitzt ein Transformer‑„Flaschenhals“, der Bildpatches wie Token in einem Satz behandelt und mittels Self‑Attention entfernte Regionen zueinander in Beziehung setzt. So kann das Modell sowohl den winzigen Knoten als auch dessen größere anatomische Umgebung erfassen, was wichtig ist, wenn Knoten mit benachbarten Gefäßen oder Bruststrukturen verschmelzen. 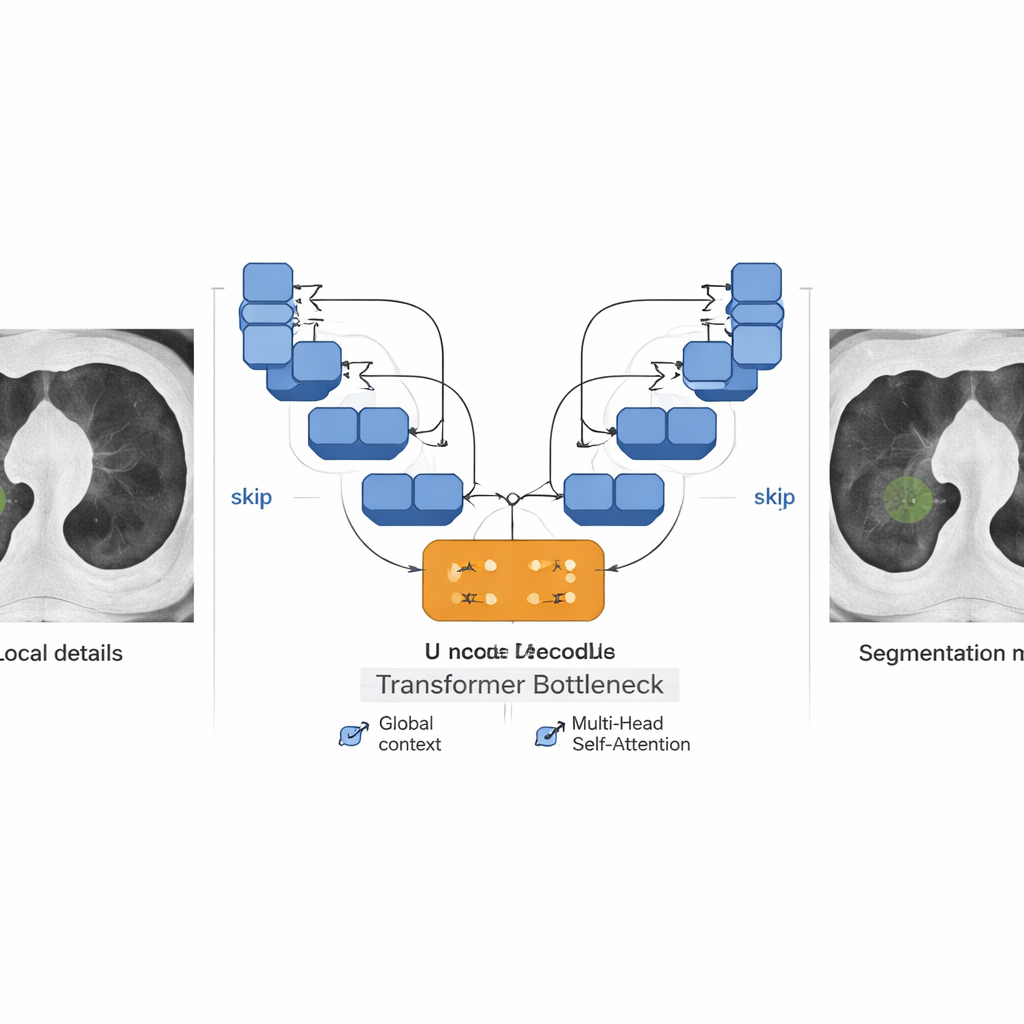
Umgang mit seltenen Zielen und ungleich verteilten Daten
Die Autor:innen gehen auch ein großes Problem der medizinischen Bildgebung an: Klassenungleichgewicht. In Lungen‑CTs ist fast jedes Pixel Hintergrund; Knotenpixel sind selten. Standardmäßiges Training belohnt Modelle, die einfach alles als Hintergrund markieren. Um dem entgegenzuwirken, kombiniert das Team zwei Verlustfunktionen – Dice‑Loss, die direkt die Überlappung zwischen vorhergesagten und echten Knoten belohnt, und Focal‑Loss, die schwer zu klassifizierende Pixel stärker gewichtet. Diese Dice–Focal‑Kombination ermutigt das Modell, auf kleine, schwierige Knoten und scharfe Begrenzungen zu achten. In ihrem föderierten Aufbau mit fünf simulierten Krankenhaus‑„Clients“, die am öffentlichen LUNA16‑Datensatz trainierten, erreichte das System Dice‑Werte bis zu 0,93 für solide Knoten und zeigte niedrige Raten sowohl für übersehene Knoten als auch für Fehlalarme. Die Leistung blieb über die meisten Clients hinweg stabil, trotz Unterschieden in Bildqualität und Knotenerscheinung; Knoten mit unscharfer oder gemischter Dichte blieben jedoch herausfordernd.
Was das für die zukünftige Lungenvorsorge bedeutet
Kurz gesagt: Diese Arbeit zeigt, dass Krankenhäuser gemeinsam eine hochwertige, knotenfindende KI trainieren können, ohne Patientenscans über Netzwerke zu verschicken. Durch die Kombination sorgfältiger Bildbereinigung, eines Modells, das sowohl Details als auch Kontext erfasst, und einer Trainingsstrategie, die auf seltene Ziele abgestimmt ist, umreißt das Framework zuverlässig solide Lungenknoten in einem realistischen Multi‑Hospital‑Setting. Zwar ist weitere Arbeit nötig, um sehr schwache oder teilweise solide Knoten besser zu behandeln, doch die Studie weist in Richtung Lungenkrebsscreening‑Werkzeuge, die sowohl genau als auch datenschutzschonend sind – und so die Vorteile großer KI‑Datensätze für Patient:innen bringen, ohne die Vertraulichkeit ihrer medizinischen Bilder zu gefährden.
Zitation: Turjya, S.M., Fawakherji, M. Federated lung nodule segmentation using a hybrid transformer–U-Net architecture. Sci Rep 16, 5228 (2026). https://doi.org/10.1038/s41598-026-35243-9
Schlüsselwörter: Lungenkrebsvorsorge, Segmentierung medizinischer Bilder, föderiertes Lernen, CT-Lungenknoten, datenschutzfreundliche KI