Clear Sky Science · de
Deglykosylierung induziert eine neuartige distale Konformation beim Mannose-Rezeptor CD206
Warum Zuckerüberzüge auf Immunsensoren wichtig sind
Unsere Immunzellen verlassen sich auf molekulare „Antenne“, um Bedrohungen wie Mikroben und Krebszellen zu erkennen. Eine dieser Antennen, der Mannose-Rezeptor CD206, hilft Immunzellen, zuckerverzierte Moleküle zu erfassen und sogar Tumoren anzuzielen. Wie viele Proteine ist auch CD206 selbst mit kurzen Zuckerketten bedeckt. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Was passiert mit Form und Funktion von CD206, wenn diese Zucker entfernt werden?
Ein flexibler Arm, der zuckerhaltige Signale liest
CD206 sitzt auf der Oberfläche bestimmter Immunzellen, besonders von Makrophagen, die Gewebe und Tumoren durchstreifen. Es besitzt eine lange, gelenkartige Struktur, die von der Zellmembran ausgreift und in mehreren „Lektin“-Segmenten endet, die Zucker auf vorbeiziehenden Molekülen erkennen. CD206 kann außerdem ins Blut freigesetzt werden; seine Konzentration korreliert mit Entzündungs- und Fibroseerkrankungen und macht es zu einem potenziellen Marker für Erkrankungen. Das Protein ist stark mit N-gebundenen Zuckerketten verziert; frühere Arbeiten zeigten, dass diese beeinflussen können, wie gut verschiedene Rezeptorsegmente Zucker erkennen. Viele dieser Zuckerstellen liegen weit von den Hauptbindungsstellen entfernt, was darauf hindeutet, dass sie eher als entfernte Schalter denn als einfache Blocker wirken könnten.
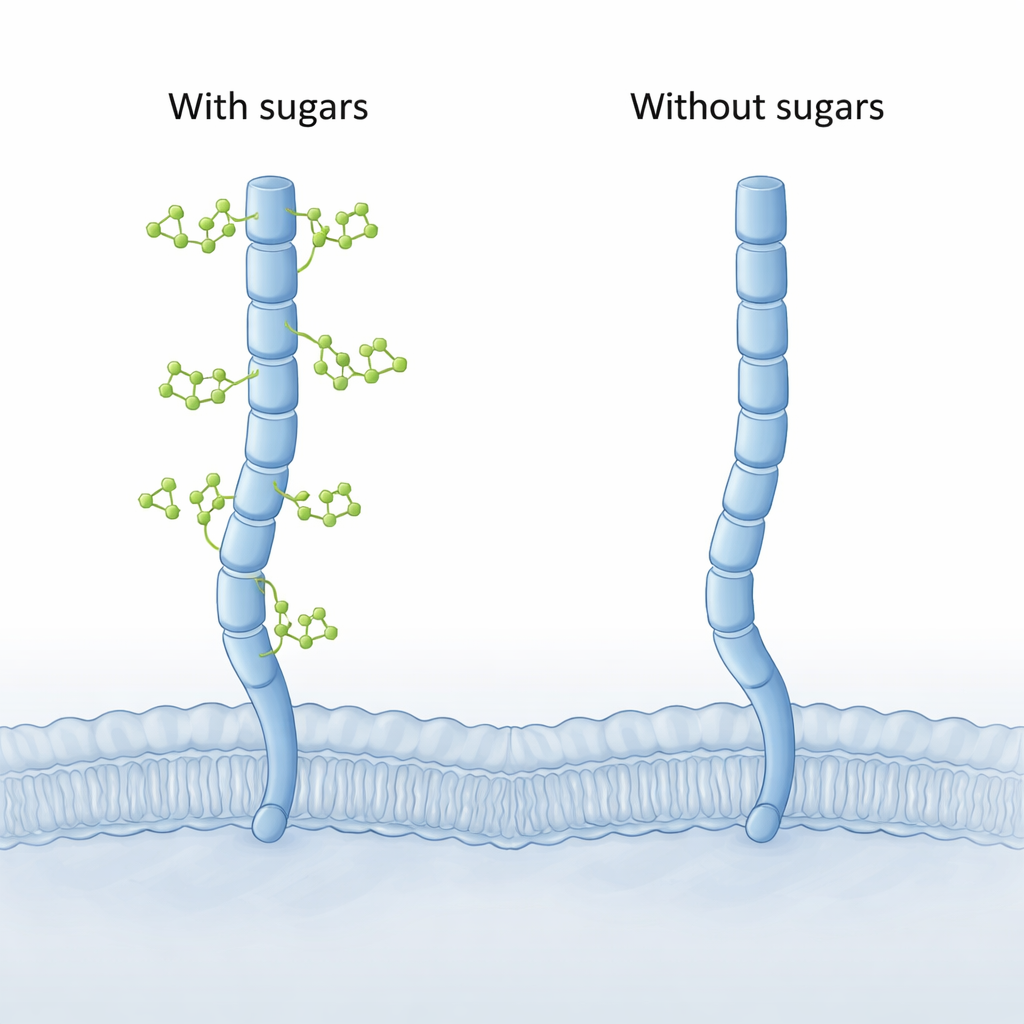
Computermodelle enthüllen eine verborgene Biegung
Da die vollständige 3D-Struktur von CD206 experimentell noch nicht erfasst wurde, nutzten die Autorinnen und Autoren moderne Rechenwerkzeuge. Zunächst verwendeten sie AlphaFold, um Vollmodellstrukturen des Rezeptors zu erstellen, und führten dann lange, detaillierte Molekulardynamik-Simulationen von CD206 mit und ohne seine angehefteten Zucker durch. Beide Versionen verhielten sich wie ein ausgreifender molekularer Arm, doch die „zuckerfreie“ Form zeigte eine auffällige neue Bewegung an ihrem äußersten Ende. Die letzten beiden Lektin-Segmente (CTLD7 und CTLD8 genannt) konnten nach innen schwingen und eine konkave, nach innen gebogene Spitze bilden — eine Form, die in der zuckerverzierten Version nie beobachtet wurde; diese verblieb eher in einer nach außen gebogenen, konvexen Gestalt.
Wie eine kleine Veränderung die Bewegung umformt
Um diesen Unterschied zu verstehen, analysierte das Team die dominanten Bewegungen in ihren Simulationen. Sie fanden heraus, dass die Hauptbewegung, die die beiden Formen unterscheidet, genau diese Biegung der distalen Spitze ist und dass sie nur auftritt, wenn die Zucker fehlen. Allgemein machte das Entfernen der Zucker den Rezeptor flexibler, insbesondere in den distalen Lektin-Segmenten und in geringerem Maße am N-terminalen Ende. Korrelationskarten, die zeigen, wie verschiedene Teile des Proteins gemeinsam bewegten, ergaben, dass ohne Zucker die letzten beiden Lektin-Segmente stärker konzertiert bewegen und enger mit anderen Regionen gekoppelt sind. Im Wesentlichen sitzen die Zucker nicht nur auf der Oberfläche; sie stimmen die Art und Weise ab, wie sich der gesamte Arm biegt und entlang seiner Länge kommuniziert.
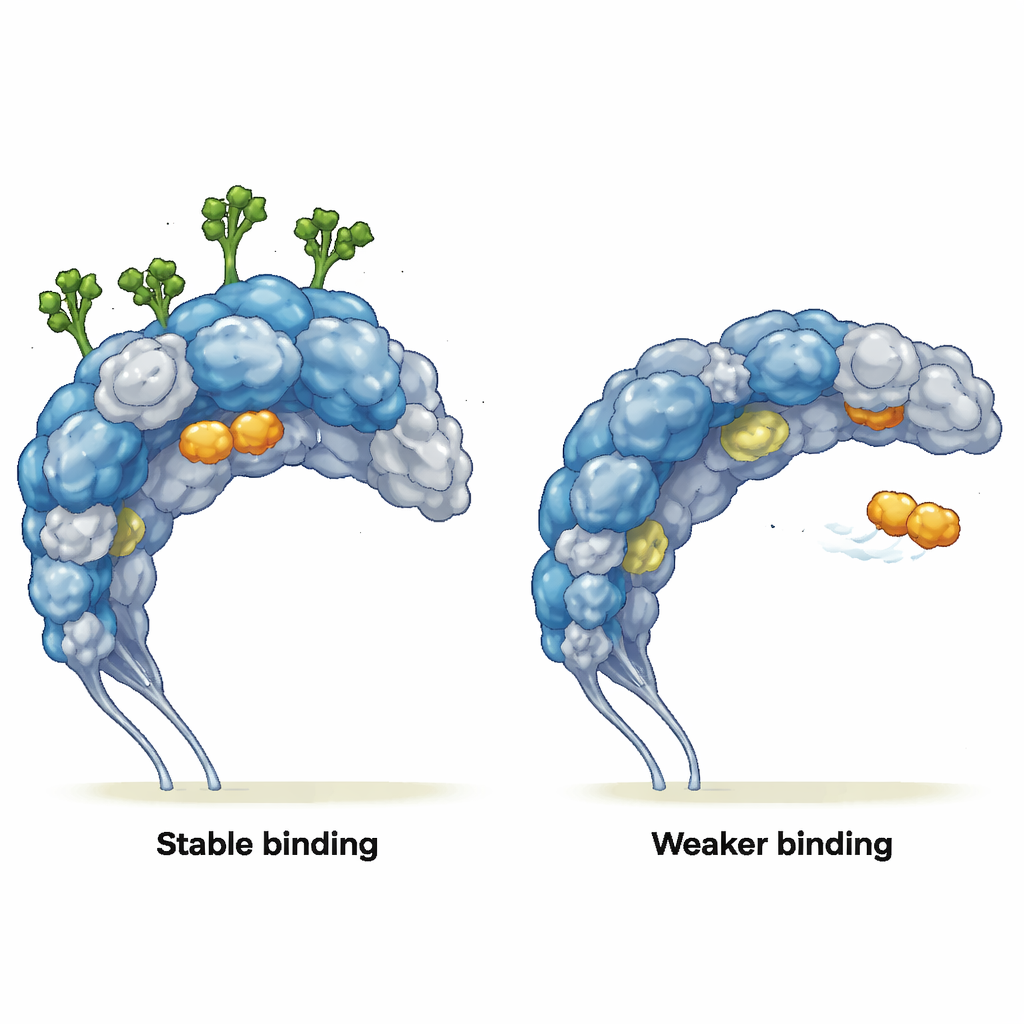
Veränderung der Art, wie Partner binden
Die Autorinnen und Autoren untersuchten anschließend, wie sich diese veränderte Bewegung auf reale Bindungspartner auswirkt. Sie simulierten Wechselwirkungen mit zwei Liganden: einem einfachen mannoseähnlichen Zucker (MMA), der in eine gut definierte Tasche passt, und einem tumoranvisierenden Peptid namens mUNO, das CD206-positive, tumorassoziierte Makrophagen anvisiert. In Gegenwart der Zucker blieb MMA während der gesamten Simulation fest in seiner Bindungsstelle und hielt wichtige Kontakte, obwohl die benachbarte Proteinstruktur kaum verändert war. Ohne Zucker entkam MMA der Tasche, glitt über die Proteinoberfläche und bildete nur kurze, oberflächliche Kontakte. Für mUNO zeigte der glykosylierte Rezeptor mehrere stabile Bindungsposen mit häufigen, langanhaltenden Kontakten. Im de-glykosylierten Rezeptor war die Bindung von mUNO schwächer und verstreuter; es begann zudem, Regionen zu erkunden, die normalerweise von Zuckerketten blockiert sind, und offenbarte so neue, zuvor verborgene Interaktionsstellen.
Was das für Krankheit und Therapie bedeutet
Insgesamt zeigen diese Ergebnisse, dass die an CD206 gebundenen Zucker als entfernte Regulatoren seiner Form und Haftung fungieren. Indem sie bestimmte Biegungen einschränken und die gemeinsame Bewegung der Segmente organisieren, helfen die Glykane dem Rezeptor, einige Liganden fester zu halten und andere zu bevorzugten Andockstellen zu lenken, während sie gleichzeitig Teile seiner Oberfläche abschirmen. Bei Erkrankungen wie Krebs, in denen die generellen Zuckerprofile von Proteinen häufig verändert sind, könnte CD206 andere Formen und Bindungsverhalten annehmen und damit die Art verändern, wie Immunzellen ihre Umgebung wahrnehmen. Das Verständnis dieses zuckerabhängigen „Konformationsschalters“ klärt nicht nur die Funktionsweise von CD206, sondern legt auch neue Ansatzpunkte nahe, um Arzneimittel oder Bildgebungsagentien zu entwickeln, die seine veränderliche Landschaft in Tumoren und anderen krankhaften Zuständen ausnutzen.
Zitation: Alvarez, G., Di Lella, S., Pickholz, M. et al. Deglycosylation induces a novel distal conformation in the mannose receptor CD206. Sci Rep 16, 5239 (2026). https://doi.org/10.1038/s41598-026-35240-y
Schlüsselwörter: Mannose-Rezeptor, Protein-Glykosylierung, Immunerkennung, tumorassoziierte Makrophagen, Molekulardynamik