Clear Sky Science · de
Verlust von Snhg5 stört die Zellzyklusregulation, verändert aber die Zystogenese in einem Mausmodell der polyzystischen Nierenerkrankung nicht
Warum ein Nierengen mit einem seltsamen Namen wichtig ist
Die polyzystische Nierenerkrankung (PKD) ist eine häufige erbliche Erkrankung, bei der unzählige mit Flüssigkeit gefüllte Hohlräume die Nieren allmählich überwuchern und häufig zur Niereninsuffizienz führen. Wissenschaftler wissen, dass Defekte in zwei Genen, PKD1 und PKD2, die Krankheit antreiben, doch viele weitere genetische Faktoren können beeinflussen, wie schnell sie fortschreitet. Diese Studie konzentriert sich auf einen ungewöhnlichen Gentypp, eine lange nicht-kodierende RNA namens Snhg5, und stellt eine einfache, aber wichtige Frage: Beeinflusst dieses Molekül den Verlauf der PKD maßgeblich, oder ist es überwiegend ein Nebenakteur?
Ein genauerer Blick auf einen obskuren genetischen Boten
Anders als typische Gene, die Baupläne für Proteine liefern, wirken lange nicht-kodierende RNAs eher wie molekulare Organisatoren oder Schalter in der Zelle. Frühere Arbeiten zeigten, dass Snhg5 in Mausmodellen der PKD stark hochreguliert ist und mit mehreren Krebsarten sowie Nierenschäden in Verbindung gebracht wurde, was darauf hindeutet, dass es schädliches Wachstum antreiben könnte. Die Forschenden kartierten zunächst, wo und wann Snhg5 in normalen Mäusen aktiv ist. Sie fanden heraus, dass es in vielen Organen eingeschaltet ist, mit besonders hohen Werten im Darm, und dass seine Aktivität in der Niere nach der Geburt stark abfällt, wenn das Organ vom raschen Wachstum in einen stabileren, ausgereiften Zustand übergeht. Innerhalb von Nierenzellen befindet sich nahezu die gesamte Snhg5-Menge im Zellkern, dem Kommandozentrum, das die DNA beherbergt, was darauf hindeutet, dass Snhg5 eher die Genaktivität steuert, statt direkt Proteine zu produzieren.
Mustern in kranken Nieren fehlt der ganze Kontext
Das Team verglich anschließend die Snhg5-Spiegel in verschiedenen Mausmodellen der PKD. In schnell verlaufenden Modellen, in denen Zysten rasch entstehen, war Snhg5 in kranken Nieren um das Zwei- bis Dreifache erhöht, und Einzelzellbildgebung zeigte starke nukleare Signale in Zysten auskleidenden Zellen und dem umliegenden Gewebe. Überraschenderweise stieg Snhg5 in einem langsameren, milderen Mausmodell, das den langen Verlauf der menschlichen PKD besser nachahmt, nicht an. Noch auffälliger war, dass das menschliche Gegenstück des Gens, SNHG5, in Nierengewebe von Menschen mit fortgeschrittener autosomal-dominanter PKD tatsächlich um mehr als 90 Prozent reduziert war. Zusammengenommen deuten diese Ergebnisse darauf hin, dass Veränderungen dieser RNA mit der Zystenbildung einhergehen, die Richtung und das Timing der Veränderung jedoch zwischen Arten und Krankheitsstadien variieren, was Zweifel daran aufkommen lässt, dass Snhg5 allein ein eindeutiger Treiber des Zystenwachstums ist.
Was passiert, wenn das Gen entfernt wird
Um über Korrelationen hinauszugehen, nutzten die Forschenden CRISPR-Geneditierung, um das Snhg5-Gen bei Mäusen vollständig zu löschen und eine globale „Knockout“-Linie zu erzeugen. Entgegen der Sorge, dass das Entfernen eines so stark veränderten Moleküls schädlich sein könnte, wurden Mäuse ohne Snhg5 in normalen Verhältnissen geboren, hatten eine normale Lebensdauer und Nieren, die wie die ihrer gesunden Wurfgeschwister aussahen und funktionierten. Mikroskopische Untersuchungen zeigten eine normale Nierenstruktur ohne Vernarbung oder Entzündung, und Bluttests wiesen keine Hinweise auf eine eingeschränkte Nierenfilterfunktion auf. Auf molekularer Ebene traten jedoch subtilere Veränderungen zutage: Sowohl in Nieren von Mäusen als auch in kultivierten Nierentubuluszellen ohne Snhg5 zeigten sich konsistente Verschiebungen in der Aktivität von Genen, die mit Zellteilung und DNA-Replikation verbunden sind. In Zellkultur stockten mehr Zellen in späten Phasen des Zellzyklus und in einem geschädigten Sub-G1-Zustand. Ein Protein im Besonderen, ARPC5, Teil eines Komplexes, der Zellen durch Umstrukturierung ihres internen Gerüsts bei der Teilung unterstützt, war reduziert, wenn Snhg5 fehlte, was auf eine mögliche Kausalkette hindeutet.
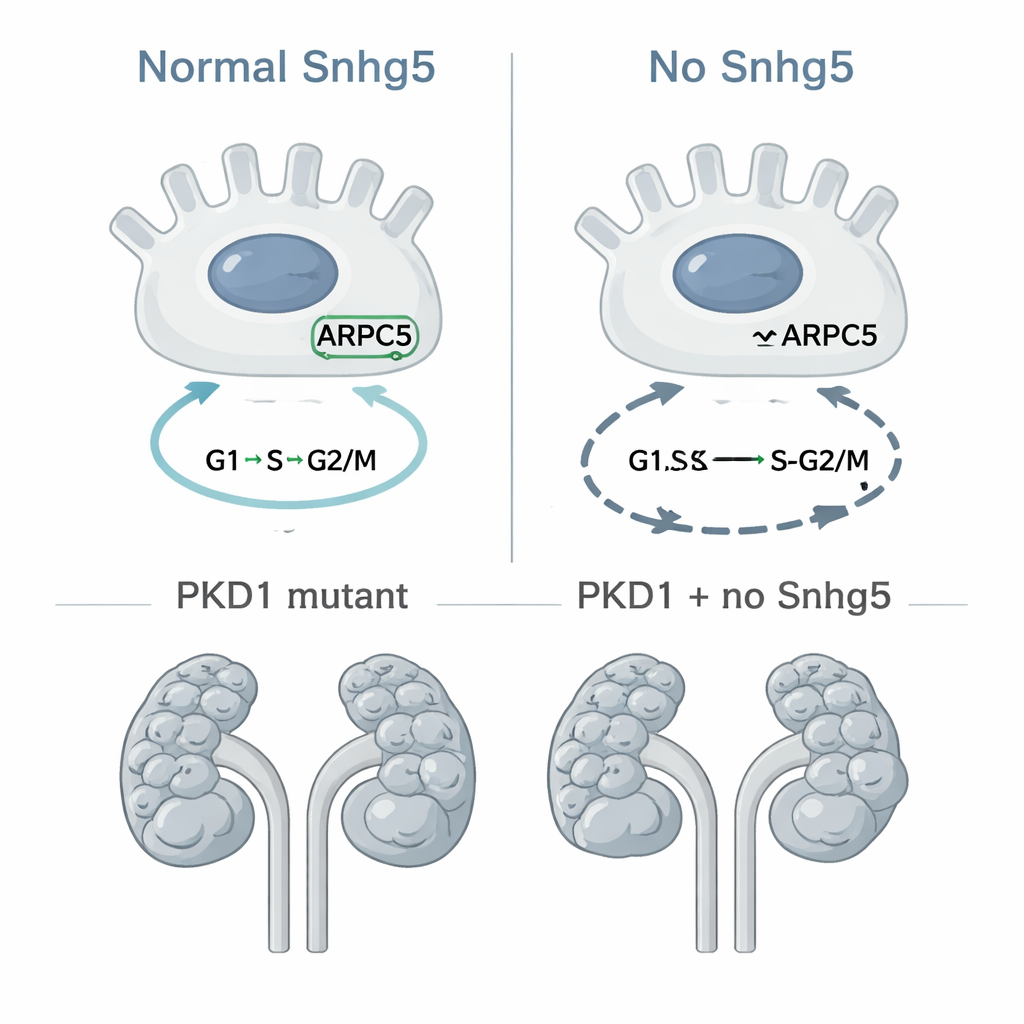
Direkter Test seiner Rolle beim Zystenwachstum
Da unkontrollierte Zellteilung ein zentrales Merkmal der PKD ist, untersuchte das Team als Nächstes, ob das Entfernen von Snhg5 die Zystenbildung in einem etablierten Mausmodell verlangsamte, in dem das PKD1-Gen spezifisch in Sammelrohrzellen deaktiviert ist, der Quelle vieler Zysten. Sie kreuzten Mäuse so, dass einige nur die PKD1-Mutation trugen, während andere sowohl PKD1 als auch Snhg5 fehlten. Bei Untersuchung der Tiere im Alter von 10 Tagen zeigten beide Gruppen stark zystische Nieren, und sorgfältige Messungen von Nierengröße, Zystenfläche und Zystenzahl ergaben keinen bedeutsamen Schutz durch das Löschen von Snhg5. Wenn überhaupt, neigten die Doppelmutanten zu einer leicht höheren Zystenlast, obwohl der Unterschied gering und statistisch nicht überzeugend war. Mit anderen Worten: Obwohl Snhg5 die Zellzyklusgene in Nierenzellen beeinflusst, verändert sein Fehlen in diesem speziellen PKD-Modell die Geschwindigkeit, mit der Zysten auftreten oder wachsen, nicht merklich.
Was das für künftige Therapien bedeutet
Für Patienten und Arzneimittelentwickler lautet die wichtigste Schlussfolgerung: Snhg5 ist – obwohl eines der stärksten veränderten genetischen Signale in der Maus-PKD – kein Dreh- und Angelpunkt der Zystenbildung, zumindest nicht in der frühen, schnell wachsenden Phase der aus Sammelrohren stammenden Erkrankung. Das Gen scheint die Art und Weise, wie Nierenzellen den Teilungszyklus durchlaufen, fein abzustimmen, wahrscheinlich über seinen Einfluss auf Faktoren wie ARPC5, doch ist dieser Einfluss so subtil, dass sein vollständiges Fehlen die Nierenentwicklung und den frühen PKD-Verlauf weitgehend unberührt lässt. Diese Ergebnisse unterstreichen eine allgemeinere Lehre: Nicht jede auffällige molekulare Veränderung im erkrankten Gewebe ist ein vielversprechendes therapeutisches Ziel. Die Trennung von Ursache und Wirkung erfordert das Testen langer nicht-kodierender RNAs wie Snhg5 in mehreren Krankheitsmodellen und Zeitpunkten, bevor sie als Wirkstoffkandidaten mit Zuversicht verfolgt werden können.
Zitation: D’Amico, S., Dar, U., Eckberg, K. et al. Loss of Snhg5 disrupts cell-cycle regulation without altering cystogenesis in a mouse model of polycystic kidney disease. Sci Rep 16, 4869 (2026). https://doi.org/10.1038/s41598-026-35234-w
Schlüsselwörter: polyzystische Nierenerkrankung, lange nicht-kodierende RNA, Snhg5, Zellzyklus, Nierenzysten