Clear Sky Science · de
Chitosan‑Dextransulfat‑Nanokapseln zur Verbesserung der Wirksamkeit von Tigecyclin gegen nicht‑typhoidale Salmonella enterica
Warum das für Lebensmittelsicherheit wichtig ist
Die meisten Menschen kennen Salmonella als lästigen Auslöser von Lebensmittelvergiftungen, oft im Zusammenhang mit nicht ausreichend gegartem Geflügel. Weniger bekannt ist, dass einige Stämme so resistent gegen Antibiotika geworden sind, dass selbst potente „letzte Rettungs“-Medikamente versagen können. Diese Studie untersucht einen nanotechnologischen Ansatz, um ein solches Medikament, Tigecyclin, zu retten, indem es in winzige, zuckerbasierte Kapseln verpackt wird, die ihm helfen, in infizierte Zellen zu gelangen und wesentliche Resistenzmechanismen von Salmonella auszuschalten.
Die wachsende Bedrohung durch resistente Salmonella
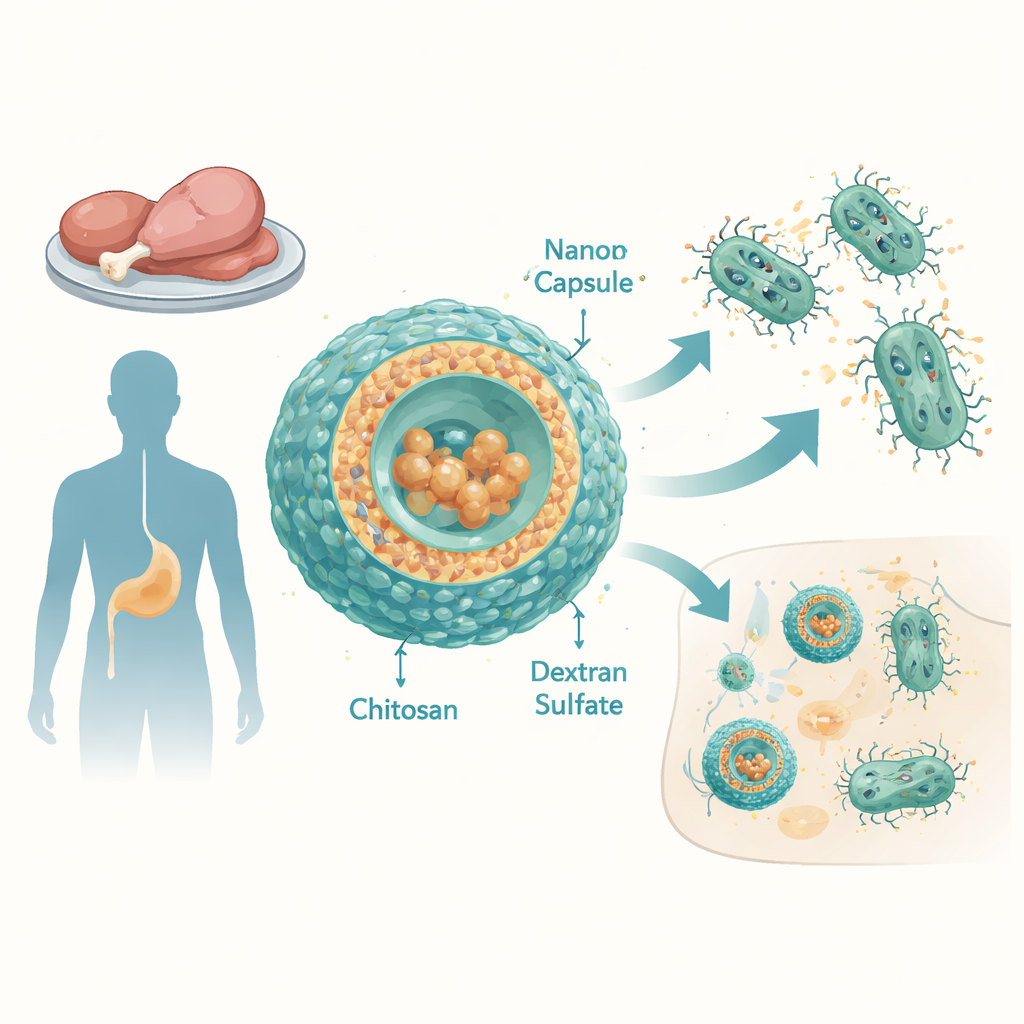
Nicht‑typhoidale Salmonella‑Serovare (NTS) sind weltweit eine Hauptursache für Durchfallerkrankungen und Blutstrominfektionen, besonders in Ländern mit niedrigem und mittlerem Einkommen. Die Forschenden untersuchten 12 Salmonella enterica‑Stämme, die aus Hühner‑ und Entenfleisch in Ägypten isoliert wurden. Diese Stämme waren gegen viele gebräuchliche Antibiotika resistent, darunter Penicilline, Cephalosporine, Tetracycline und weitere, und zeigten hohe Multiresistenz‑Werte. Selbst Tigecyclin, ein breit wirksames Mittel, das für schwere Fälle vorbehalten ist, zeigte geringe Wirkung: Die Bakterien tolerierten sehr hohe Konzentrationen. Ein wesentlicher Grund waren überaktive Efflux‑Pumpen — molekulare Maschinen in der bakteriellen Membran, die Antibiotika kontinuierlich wieder aus der Zelle herausschwemmen.
Aufbau einer intelligenteren Arzneimittelkapsel
Um dies zu überwinden, entwarf das Team nanoskalige Kapseln aus zwei natürlich gewonnenen Polymeren: Chitosan, gewonnen aus Chitin (dem Material in Schalentieren), und Dextransulfat, einem verzweigten Zuckermolekül. Durch sorgfältiges Abstimmen der Mischungsverhältnisse erzeugten sie stabile Partikel von etwa 100–150 Nanometern Durchmesser mit einer positiven Oberflächenladung, die ihre Wechselwirkung mit bakteriellen und Wirtszellmembranen fördert. Tigecyclin wurde mit bemerkenswert hoher Effizienz in diese Partikel geladen — praktisch das gesamte Medikament gelangte in die Kapseln. In Laborversuchen, die Blutbahn‑ähnliche Bedingungen nachbildeten, setzten die Kapseln den Großteil ihres Tigecyclins innerhalb weniger Stunden frei, was darauf hindeutet, dass sie an Infektionsherden eine starke Wirkstofffreisetzung bewirken könnten.
Herunterfahren bakterieller Abwehrmechanismen
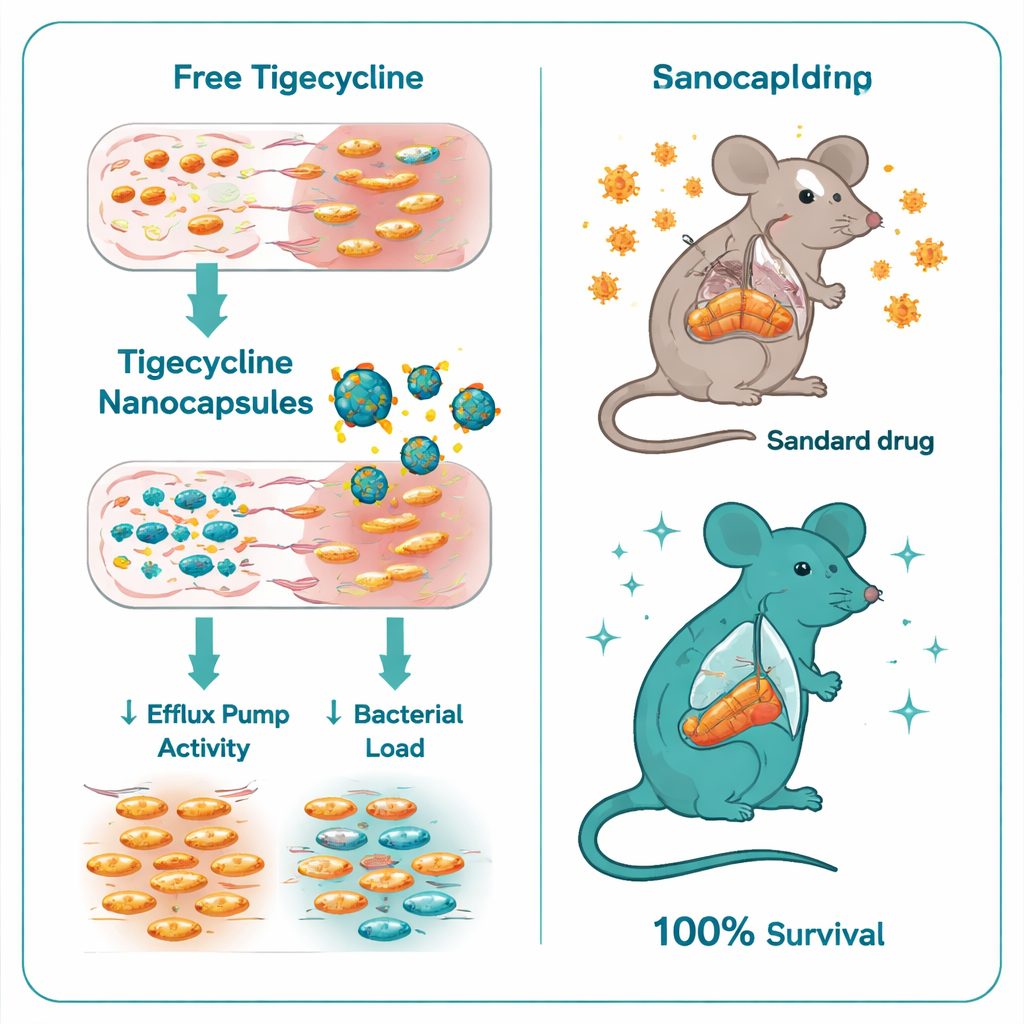
Beim Vergleich von freiem Tigecyclin mit Tigecyclin‑beladenen Chitosan‑Dextransulfat‑Nanokapseln war der Unterschied deutlich. Die minimale Wirkstoffkonzentration, die das Bakterienwachstum hemmte, sank von 32–128 Mikrogramm pro Milliliter für freies Tigecyclin auf nur 0,5–1 Mikrogramm pro Milliliter mit den Nanokapseln — eine sechs‑ bis siebenfache Verbesserung. Zeit‑Kill‑Experimente zeigten, dass die einkapselte Form Salmonella deutlich schneller und gründlicher abtötete. Auf genetischer Ebene dämpften die Nanokapseln zudem wichtige Resistenzregulatoren: Die Expression der ramA‑ und acrB‑Gene, die die Bildung und Steuerung großer Efflux‑Pumpen unterstützen, nahm in behandelten Bakterien um ein Vielfaches ab. Mit anderen Worten: Die Kapseln lieferten nicht nur mehr Wirkstoff; sie halfen auch, einen der wichtigsten Fluchtwege der Bakterien abzuschalten.
Schutz infizierter Mäuse vor tödlicher Erkrankung
Das Team prüfte die neue Formulierung anschließend in einem Mäusemodell schwerer Salmonella Typhimurium‑Infektion. Unbehandelte infizierte Mäuse starben alle innerhalb von acht Tagen. Mäuse, die Standard‑Tigecyclin erhielten, schnitten besser ab, zeigten aber weiterhin hohe Sterblichkeit mit nur 40 % Überlebenden. Im krassen Gegensatz dazu überlebte jede Maus, die mit Tigecyclin‑beladenen Nanokapseln behandelt wurde. Diese Tiere wiesen deutlich weniger Bakterien in Leber und Darm auf, Blutwerte, die näher an normale Leber‑ und Nierenfunktionen herankamen, und deutlich mildere Gewebeschäden bei mikroskopischer Untersuchung. Selbst die „leeren“ Chitosan‑Dextransulfat‑Kapseln ohne Antibiotikum boten einen gewissen Schutz, vermutlich weil Chitosan selbst moderate antimikrobielle und entzündungshemmende Effekte hat, doch die Kombination mit Tigecyclin war klar überlegen.
Was das für künftige Behandlungen bedeuten könnte
Für Nicht‑Spezialisten lautet die zentrale Botschaft: Die Verpackung eines vorhandenen Antibiotikums in eine intelligente, biokompatible Nanokapsel kann seine Wirkung gegen hochresistente Salmonella wiederherstellen. Indem das System dem Wirkstoff hilft, Bakterien zu erreichen, die in Zellen verborgen sind, und gleichzeitig die Pumpen abschwächt, die das Medikament normalerweise hinausschwemmen, verwandelte das Chitosan‑Dextransulfat‑System ein kämpfendes Reserveantibiotikum in eine hochwirksame Behandlung bei Mäusen mit 100 % Überleben. Obwohl vor einer Anwendung beim Menschen oder in Nutztieren noch weitere Arbeiten nötig sind, bietet dieser Ansatz einen vielversprechenden Weg, die Nutzungsdauer wichtiger Antibiotika zu verlängern und die Sicherheit unserer Lebensmittelversorgung zu verbessern, ohne völlig neue Wirkstoffe entwickeln zu müssen.
Zitation: Omar, M.R., Saeed, A.A., Malhat, S.M. et al. Chitosan-dextran sulfate nanocapsules for enhanced tigecycline efficacy against non-typhoidal Salmonella enterica. Sci Rep 16, 5016 (2026). https://doi.org/10.1038/s41598-026-35229-7
Schlüsselwörter: Salmonella, Antibiotikaresistenz, Nanopartikel, Arzneimittel‑Freisetzung, Tigecyclin