Clear Sky Science · de
Genetische Polymorphismen im DNA-Reparaturgen XRCC1 und das Risiko für diabetische Polyneuropathie
Warum winzige DNA-Veränderungen für Menschen mit Diabetes wichtig sind
Bei vielen Menschen mit Typ‑2‑Diabetes ist das erste Warnzeichen nicht ein hoher Blutzucker im Labor, sondern Kribbeln, Brennen oder Taubheitsgefühle in Füßen und Händen. Dieser Zustand, diabetische Polyneuropathie genannt, kann zu Schmerzen, Gleichgewichtsverlust und sogar Amputationen führen. Dennoch entwickeln nicht alle Menschen mit Diabetes diese Komplikation, selbst wenn ihre Blutzuckerwerte ähnlich sind. Diese Studie stellte eine einfache, aber folgenreiche Frage: Können kleine vererbte Unterschiede in einem DNA‑Reparaturgen erklären, wer besonders gefährdet ist, und kann moderne Datenwissenschaft Ärzten helfen, diese Personen früher zu erkennen?
Ein genauerer Blick auf Nervenschäden bei Diabetes
Diabetische Polyneuropathie entsteht, wenn lange Nerven, besonders in Beinen und Füßen, über Jahre durch hohen Blutzucker, schlechte Durchblutung und chronisches „Rosten“ der Zellen durch reaktive Sauerstoffmoleküle langsam geschädigt werden. Diese Moleküle können wichtige Zellbestandteile, einschließlich DNA, angreifen. Unsere Zellen sind nicht wehrlos: Sie verfügen über Reparaturmechanismen, die solche Schäden ständig ausbessern. Ein solcher Mechanismus beruht auf einem Protein, das vom Gen XRCC1 kodiert wird und bei der Reparatur von Einzelstrangbrüchen in der DNA hilft. Funktioniert dieses Reparatursystem schlecht, sind Nervenzellen möglicherweise weniger in der Lage, dem dauerhaften Stress des Diabetes zu trotzen, wodurch Nervenschäden wahrscheinlicher und schwerer werden.
Was die Forscher an ägyptischen Patienten untersuchten
Das Team untersuchte 732 Erwachsene in Ägypten: 503 mit Typ‑2‑Diabetes und 229 gesunde Freiwillige. Unter den Diabetikern hatten etwa die Hälfte bereits Nervenschäden, die andere Hälfte nicht. Die Wissenschaftler konzentrierten sich auf zwei häufige „Buchstabendifferenzen“ im XRCC1‑Gen, bekannt als Arg399Gln und Arg194Trp. Diese winzigen Veränderungen, Single‑Nucleotide‑Polymorphismen genannt, tauschen einen Baustein des XRCC1‑Proteins gegen einen anderen aus und können die Effizienz der DNA‑Reparatur verändern. Mithilfe standardmäßiger Gentests an Blutproben bestimmten die Forscher, welche Varianten an diesen beiden Positionen jede Person trug, und verglichen diese Muster anschließend mit dem Vorhandensein und der Schwere der Nervenschäden.
Genetische Muster, die mit erhöhtem Nervenkontakt verbunden sind
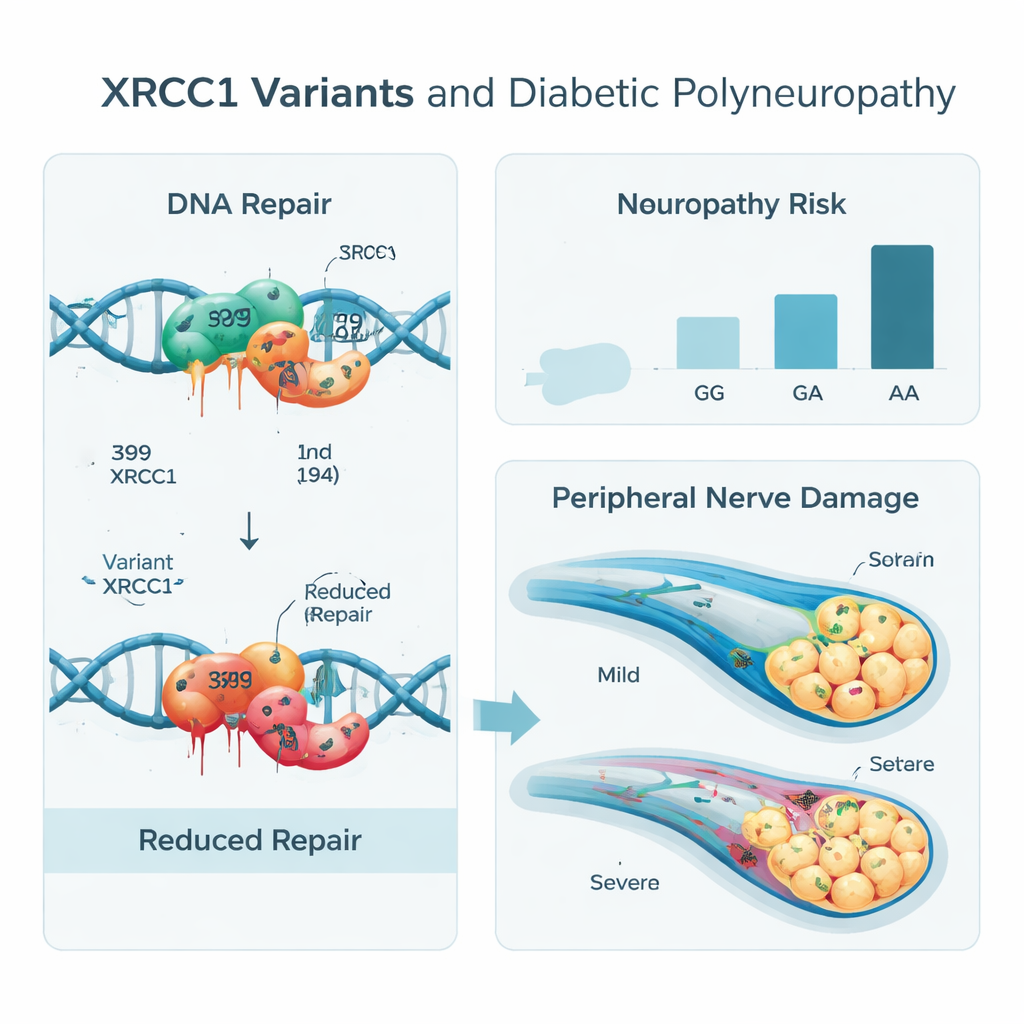
Die Ergebnisse zeigten ein klares Muster. Menschen mit Diabetes, die die selteneren Varianten von XRCC1 trugen — die A‑Form an Position 399 und die T‑Form an Position 194 — hatten eine höhere Wahrscheinlichkeit für Nervenschäden als jene mit den häufigen Varianten. Insbesondere hatten Personen mit zwei A‑Kopien an Position 399 ein mehrfach erhöhtes Odds‑Verhältnis für Neuropathie gegenüber Personen mit zwei G‑Kopien, selbst nach Berücksichtigung von Alter, Geschlecht und Rauchen. Ebenso erhöhte das Vorhandensein mindestens einer T‑Kopie an Position 194 das Risiko. Betrachtete man beide Positionen gemeinsam als Haplotypen, stach eine Kombination (A–T) als besonders riskant für Nervenerkrankungen hervor, während andere Kombinationen trotz einer riskanten Base schützend zu wirken schienen — ein Hinweis auf komplexere Gen‑Gen‑Interaktionen.
Wie Machine Learning das Bild schärfte
Um über einfache Vergleiche hinauszugehen, griffen die Forscher auf Machine Learning zurück, einen Bereich der künstlichen Intelligenz, der viele Variablen gleichzeitig durchsieben kann. Mit Random Forest‑ und XGBoost‑Algorithmen trainierten sie Modelle an 80 % der Daten und testeten sie an den restlichen 20 %. Diese Modelle hoben nicht nur die XRCC1‑Varianten hervor, sondern auch klassische klinische Faktoren — wie längere Diabetesdauer, höhere Nüchternglukose und „schlechtes“ LDL‑Cholesterin, niedriges „gutes“ HDL‑Cholesterin, höheres Alter und höheren Body‑Mass‑Index — als wichtige Prädiktoren für Neuropathie. Ein Erklärungswerkzeug namens SHAP veranschaulichte, wie jeder Faktor das individuelles Risiko nach oben oder unten verschob. Das Team verglich außerdem zwei Punktesysteme für die Bettenauswertung von Nervenschäden und fand heraus, dass der Toronto Clinical Neuropathy Score das Krankheitsausmaß besser erfasste als ein älterer Disability‑Score.
Was das für Patienten und Prävention bedeutet
Einfach gesagt legt die Studie nahe, dass manche Menschen mit Typ‑2‑Diabetes von Geburt an ein weniger robustes DNA‑Reparaturpaket haben, wodurch ihre Nerven verwundbarer gegenüber den Belastungen von hohem Blutzucker und ungünstigen Blutfettwerten sind. Diese vererbten Unterschiede im XRCC1‑Gen scheinen nicht Diabetes selbst zu verursachen, erhöhen jedoch die Wahrscheinlichkeit, schmerzhafte und behindernde Nervenschäden zu entwickeln, sobald Diabetes vorhanden ist. Durch die Kombination einfacher Bluttests, klinischer Messwerte, Nervenskalen und genetischer Informationen in intelligenten Computermodellen könnten Ärzte eines Tages Risikopatienten früh identifizieren und Nachsorge sowie Behandlung — straffere Zucker‑ und Lipidkontrolle, Lebensstiländerungen und nervenschützende Therapien — gezielt anpassen, bevor schwerwiegende Nervenschäden eintreten.
Zitation: Hashim, N.A., El-Baz, H.A., Afya, Z.I.A. et al. Genetic polymorphisms in DNA repair gene XRCC1 and the risk of diabetic polyneuropathy. Sci Rep 16, 4815 (2026). https://doi.org/10.1038/s41598-026-35213-1
Schlüsselwörter: diabetische Neuropathie, DNA-Reparatur, XRCC1, genetisches Risiko, Machine Learning