Clear Sky Science · de
Integrierte Proteomik und Metabolomik zeigen, dass Phytosesquiterpenlactone die Aktivität von TNBC‑Zellen durch Erschöpfung der ATP‑Synthese und Umprogrammierung des Primärstoffwechsels hemmen
Pflanzenstoffe, die aggressiven Brustkrebs aushungern
Trippelnegativer Brustkrebs ist eine der schwierigsten Formen von Brustkrebs zu behandeln, weil ihm die üblichen hormonellen "Griffe" fehlen, an denen viele Medikamente ansetzen. Diese Studie untersucht zwei Moleküle, die aus einer Heilpflanze isoliert wurden und offenbar die inneren Kraftwerke dieser Krebszellen außer Betrieb setzen, ihnen die Energiezufuhr abschneiden und gleichzeitig normale Brustzellen weitgehend verschonen. Zu verstehen, wie das funktioniert, könnte den Weg für schonendere und gezieltere Therapien für Patientinnen öffnen, die derzeit nur begrenzte Optionen haben.
Warum es wichtig ist, die Energiequelle von Krebs anzugreifen
Jede Zelle ist auf winzige Strukturen namens Mitochondrien angewiesen, um ATP herzustellen, den grundlegenden Brennstoff der Zelle. Krebszellen, insbesondere aggressive, sind oft in besonderem Maße auf ihre Mitochondrien angewiesen, um schnelles Wachstum, Ausbreitung und Überleben unter Stress zu ermöglichen. Die Forschenden konzentrierten sich auf trippelnegative Brustkrebszellen, die etwa 15–20 % aller Brustkrebserkrankungen ausmachen und häufiger als andere Typen erneut auftreten und metastasieren. Untersucht wurden das natürliche Molekül Deoxyelephantopin (DET) und sein veredelter Verwandter DETD‑35, beides Sesquiterpenlactone aus der Heilpflanze Elephantopus. Frühere Arbeiten zeigten, dass diese Verbindungen oxidativen Stress und ungewöhnliche Formen des Zelltods in Krebszellen auslösen, doch wie sie die Energiewerke der Zellen stören, war bisher wenig verstanden.
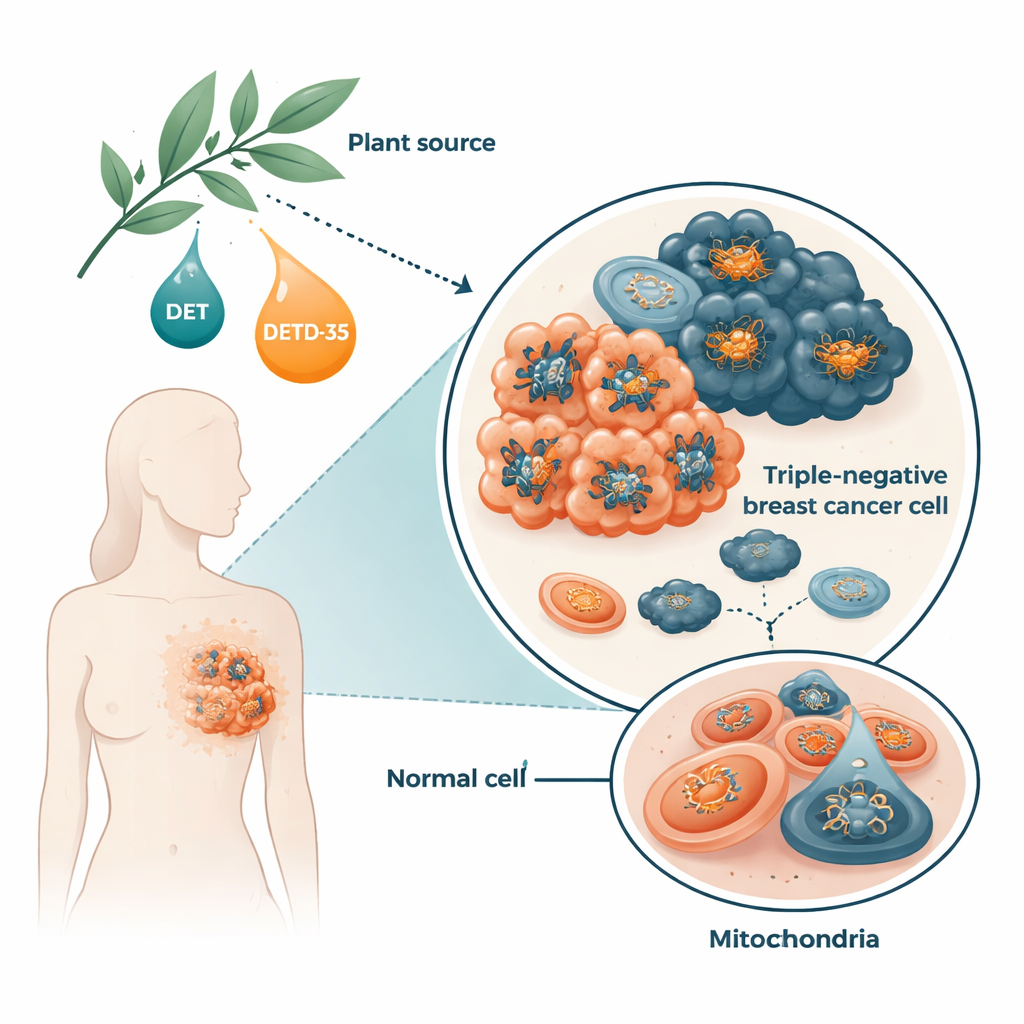
Wie die Pflanzenmoleküle die Mitochondrien von Krebszellen stören
An humanen trippelnegativen Brustkrebszellen, die im Labor kultiviert wurden, fanden die Forschenden, dass DET und DETD‑35 schnell die Produktion reaktiver Sauerstoffspezies erhöhten — eine Art chemisch reaktive "Abgase", die bei der Energieerzeugung entstehen. Als Reaktion verstärkten die Zellen bestimmte Schutzenzyme, jedoch nicht ausreichend, um das Gleichgewicht wiederherzustellen. Die Verbindungen zwangen außerdem einen Kanal in der Mitochondrienmembran auf, den sogenannten Permeability Transition Pore, eine Veränderung, die mit Anschwellen, Verlust der Membrananladung und frühen Schritten des Zelltods verbunden ist. Innerhalb weniger Stunden sanken die ATP‑Spiegel in den Krebszellen deutlich. Wenn die Forschenden vorher ein Antioxidans hinzufügten, wurden diese schädigenden Effekte größtenteils rückgängig gemacht, was zeigt, dass oxidativer Stress ein zentraler Bestandteil des Prozesses ist.
Zuordnung der Schäden an Proteinen und Stoffwechsel
Um das große Ganze zu erfassen, kombinierten die Wissenschaftlerinnen und Wissenschaftler zwei leistungsfähige "Omics"‑Ansätze. Sie katalogisierten Tausende mitochondrieller Proteine und maßen viele kleine Metaboliten in behandelten versus unbehandelten Zellen. Dieser integrierte Blick zeigte, dass DET und DETD‑35 Proteine störten, die an der oxidativen Phosphorylierung beteiligt sind — dem Hauptweg, mit dem Mitochondrien ATP erzeugen — und gleichzeitig todesbezogene Signalwege aktivierten. Parallel dazu wurden zentrale Stoffwechselwege, die Aminosäuren, Fette und Bausteine für DNA handhaben, umprogrammiert. Bestimmte Lipide, die die innere Mitochondrienmembran mitgestalten, sowie Moleküle, die mit antioxidativen Abwehrmechanismen und dem Zuckerabbau zusammenhängen, veränderten sich in einer Weise, die zu gestressten, energiearmen Krebszellen passt. Entscheidend war, dass diese weitreichenden Veränderungen in normalen Brustzellen, die den gleichen Dosen ausgesetzt waren, nicht beobachtet wurden — ein Hinweis auf eine gewisse Selektivität gegenüber Tumorzellen.
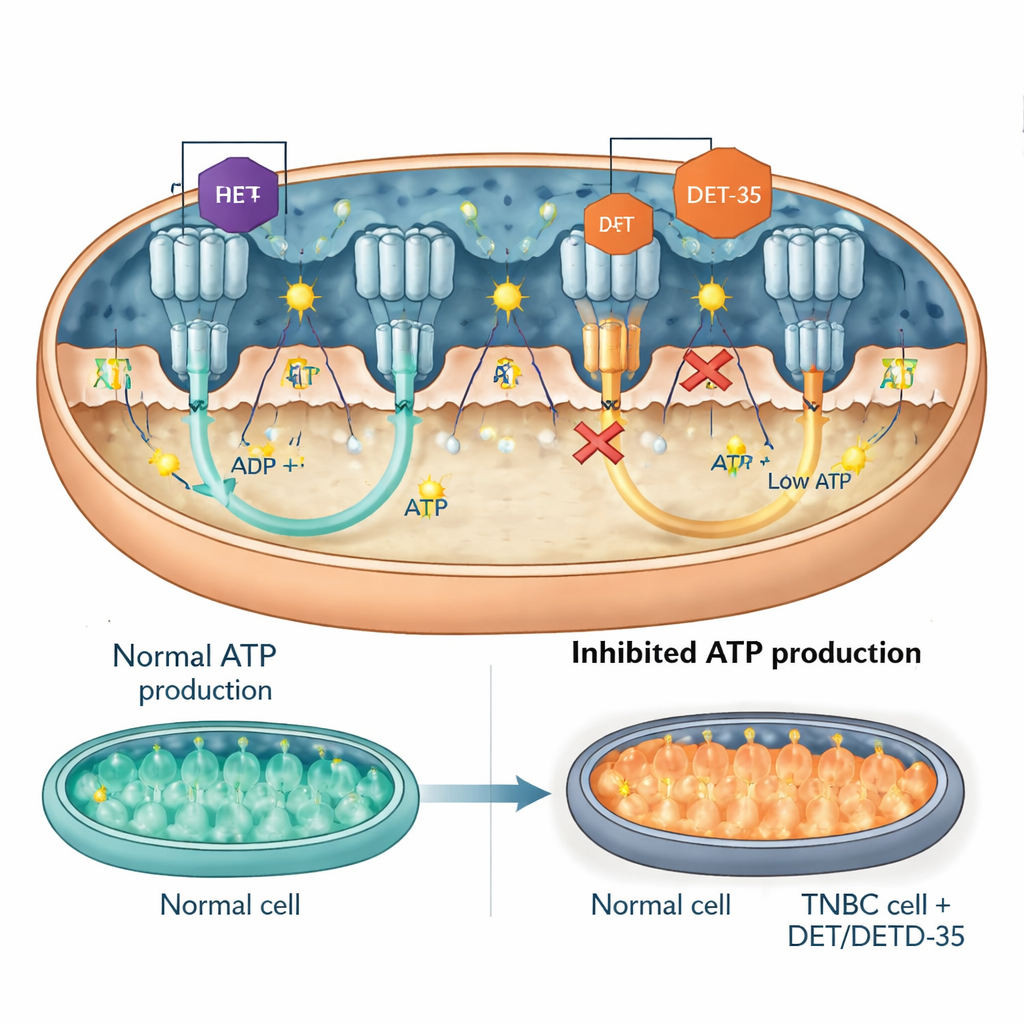
Ein Schlüsselsignalprotein und die ATP‑Turbine selbst
Anschließend richtete das Team den Blick auf einzelne Akteure innerhalb dieser gestörten Netzwerke. Einer davon war PRKCA, ein Signalprotein, das in Mitochondrien wandern und sowohl die Energieproduktion als auch Stressreaktionen beeinflussen kann. DET und DETD‑35 erhöhten die PRKCA‑Spiegel in Krebszellen. Als die Forschenden PRKCA genetisch herunterfuhren, wurden die Wirkstoffe weniger toxisch: Die Krebszellen überlebten häufiger, produzierten mehr ATP und zeigten weniger Anzeichen mitochondrialer Fehlfunktionen und Apoptose. Ein weiterer Fokus war die ATP‑Synthase, die molekulare "Turbine", die sich dreht, um ATP zu erzeugen. Messungen zeigten, dass DET und DETD‑35 die Aktivität der ATP‑Synthase in Mitochondrien von Krebszellen direkt reduzierten. Computerdocking‑Modelle legten nahe, dass beide Verbindungen an kritischen Schnittstellen des Enzyms andocken — in denselben allgemeinen Regionen, an denen bekannte ATP‑Synthase‑blockierende Wirkstoffe binden — und dessen Bewegung physisch behindern, wodurch die ATP‑Produktion sinkt. In Mäusen mit humanen trippelnegativen Brusttumoren senkte die Behandlung mit einer der Verbindungen die Mengen an ATP‑Synthase‑Komponenten im Tumorgewebe, was die Zellkulturbefunde stützt.
Was das für zukünftige Krebsbehandlungen bedeuten könnte
Insgesamt zeichnet die Studie ein stimmiges Bild: Diese pflanzlich abgeleiteten Verbindungen bringen trippelnegative Brustkrebszellen in eine Energiekrise, indem sie diese mit oxidativem Stress überlasten, Mitochondrienporen aufreißen und die ATP‑Herstellungsmaschinerie direkt blockieren. Während ATP zur Neige geht und der Stoffwechsel durcheinandergerät, verlieren die Krebszellen ihre Fähigkeit zu wachsen und zu überleben, während normale Brustzellen unter den gleichen Bedingungen weitgehend unbeschadet bleiben. Für eine nicht‑fachliche Leserschaft lautet die Botschaft, dass Forschende die starke Abhängigkeit von Krebszellen von ihren inneren Kraftwerken ausnutzen könnten, indem sie sorgfältig gestaltete Moleküle — teils von Pflanzen inspiriert — einsetzen, um den Tumorzellen die Energie zu entziehen, ohne gesundes Gewebe lahmzulegen. Bevor solche Wirkstoffe in die Klinik gelangen, ist noch mehr Arbeit nötig, doch dieser integrierte Blick auf Proteine, Metaboliten und Energieflüsse bietet eine vielversprechende Roadmap.
Zitation: Shiau, JY., Huang, HJ., Nakagawa-Goto, K. et al. Integrated proteomics and metabolomics reveal phytosesquiterpene lactones inhibit TNBC cell activity by depleting ATP synthesis and reprogramming primary metabolism. Sci Rep 16, 5264 (2026). https://doi.org/10.1038/s41598-026-35194-1
Schlüsselwörter: trippelnegativer Brustkrebs, Mitochondrien, ATP‑Synthase, Naturstoffe, Krebsstoffwechsel