Clear Sky Science · de
Rab43 mildert die Entzündungsreaktion bei akutem Lungenversagen durch Ubiquitinierung von MyD88
Warum es wichtig ist, Lungenentzündungen zu dämpfen
Wenn eine schwere Infektion oder Verletzung die Lunge trifft, kann die körpereigene Immunantwort gefährlich überreagieren. Diese außer Kontrolle geratene Entzündung, bekannt als akute Lungenschädigung und in ihrer schwersten Form als akutes Atemnotsyndrom, kann Patientinnen und Patienten auf Intensivstationen in Atemnot versetzen und ist mit einem hohen Sterblichkeitsrisiko verbunden. Heute ist die Behandlung meist unterstützend, etwa mit Sauerstoff oder Beatmung, weil es keine gezielten Therapien gibt, die schädliche Entzündung dämpfen, ohne die notwendigen Abwehrmechanismen zu schwächen. Diese Studie deckt ein kleines zelluläres „Verkehrspolizist“-Protein namens Rab43 auf, das hilft, die Lungenentzündung in Schach zu halten, und weist auf eine neue Art gezielter Therapie hin.
Ein genauerer Blick auf überforderte Lungen
Bei akuter Lungenschädigung beschädigen Infekte oder Toxine die dünne Barriere zwischen Lungenbläschen und Blutgefäßen. Lokale Immunzellen, besonders Makrophagen, die den Luftraum überwachen, eilen herbei, um Eindringlinge zu bekämpfen, indem sie Botenstoffe freisetzen, sogenannte Zytokine. Diese Moleküle helfen zwar, Mikroben zu töten, ziehen bei Übermaß jedoch Scharen weißer Blutkörperchen an und fördern Flüssigkeitsaustritt, wodurch die Lungenbläschen mit Flüssigkeit gefüllt werden und der Gasaustausch erschwert ist. Patientinnen und Patienten können einen niedrigen Blutsauerstoff entwickeln, eine weitverbreitete Entzündung haben und oft mechanisch beatmet werden müssen. Zu verstehen, wie Makrophagen entscheiden, wann sie die Produktion dieser entzündlichen Signale einstellen, ist daher entscheidend für die Entwicklung klügerer Behandlungen.
Der winzige Regulator namens Rab43
Rab43 gehört zu einer großen Familie kleiner, schalterähnlicher Proteine, die steuern, wie Fracht innerhalb der Zelle transportiert wird. Die Forschenden hatten zuvor gezeigt, dass Rab43 Makrophagen dabei unterstützt, tote Zellen in beschädigten Lungen zu beseitigen. In der neuen Arbeit untersuchten sie, ob Rab43 auch beeinflusst, wie stark Makrophagen auf bakterielle Komponenten wie Lipopolysaccharid reagieren — ein Molekül, das Entzündungen stark auslöst. Sowohl in Maus-Lungenmakrophagen als auch in im Labor gezüchteten knochenmarkabgeleiteten Makrophagen führte die Exposition gegenüber Lipopolysaccharid zu einem Abfall der Rab43-Spiegel. Das deutet darauf hin, dass die natürliche Bremse durch Rab43 bei akuter Lungenschädigung genau dann verloren gehen könnte, wenn sie am dringendsten gebraucht wird.
Was passiert, wenn Rab43 fehlt
Um die Wirkung von Rab43 im lebenden Organismus zu prüfen, erzeugte das Team Mäuse, denen Rab43 nur in ihren myeloiden Zellen, einschließlich Makrophagen, fehlte. Anschließend induzierten sie eine akute Lungenschädigung, indem sie Lipopolysaccharid direkt in die Atemwege einbrachten. Im Vergleich zu normalen Mäusen entwickelten Rab43-defiziente Tiere schwerere Lungenschäden, mit mehr Flüssigkeit in den Lungen, mehr eindringenden Neutrophilen und höheren Spiegeln entzündlicher Zytokine wie TNF-α, IL‑6 und IL‑1β im Blut und in der Lungenflüssigkeit. Diese Mäuse verloren mehr Gewicht, zeigten Anzeichen einer anhaltenden systemischen Entzündung und hatten nach einer tödlichen Lipopolysaccharid-Exposition eine deutlich höhere Sterblichkeitsrate. Die Befunde deuten darauf hin, dass Rab43 normalerweise makrophagengetriebene Entzündungen bremst und Kollateralschäden am Lungengewebe begrenzt.
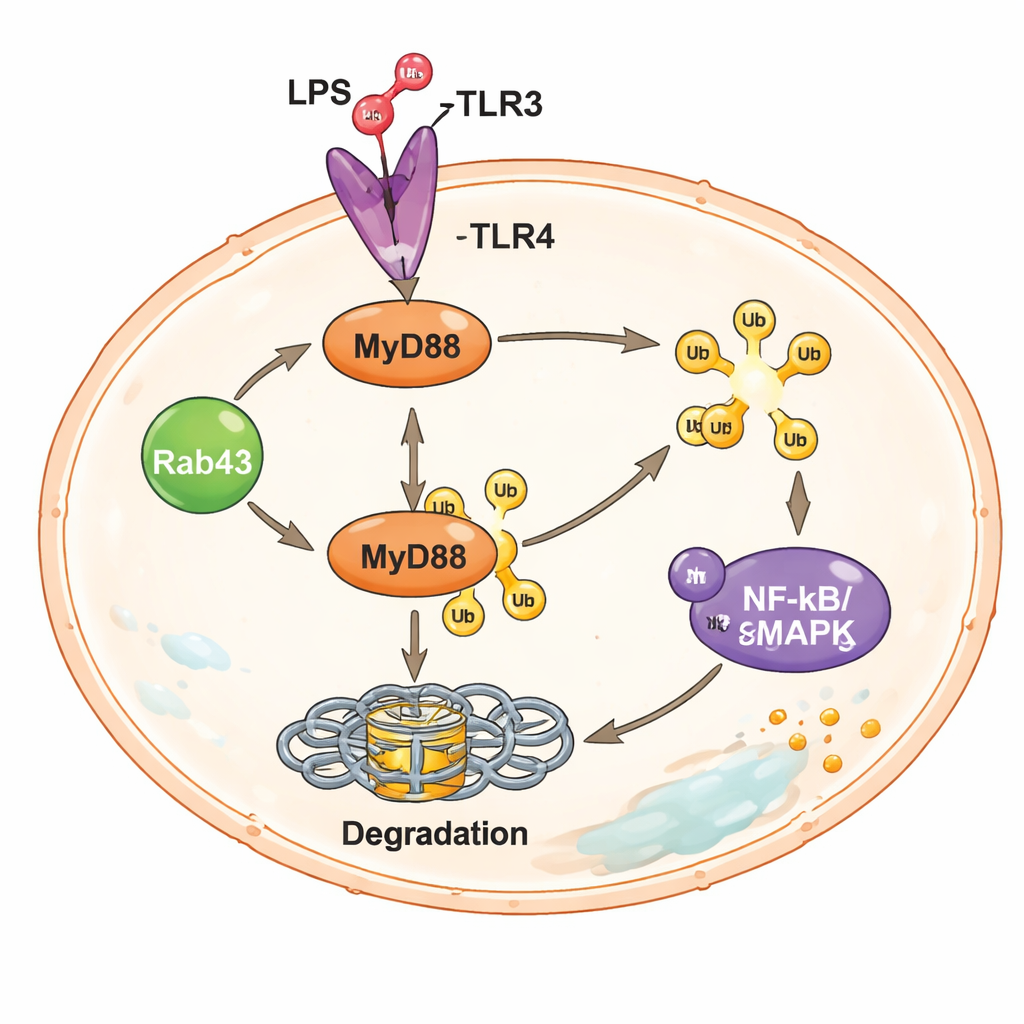
Das Signaling-Zentrum, das Rab43 im Gleichgewicht hält
Bei tieferer Analyse untersuchten die Wissenschaftler einen wichtigen Signalknotenpunkt in Makrophagen namens MyD88, der direkt stromabwärts des Lipopolysaccharid-Sensors an der Zelloberfläche sitzt. Nach Aktivierung startet MyD88 kraftvolle Signalwege, darunter NF‑κB und MAPK, die Gene für entzündliche Zytokine einschalten. In Makrophagen ohne Rab43 lagen die MyD88-Proteinspiegel deutlich höher und die Signale entlang dieser Wege waren stärker, obwohl die Menge der MyD88-Boten-RNA (mRNA) unverändert blieb. Das deutete darauf hin, dass Rab43 beeinflusst, wie schnell MyD88-Protein abgebaut wird, und nicht, wie viel davon produziert wird. Tatsächlich zeigten die Forschenden, dass Rab43 die Anlagerung winziger molekularer „Marken“ namens Ubiquitin an MyD88 fördert, die es für den Abbau durch die zellulären Proteinfaltungs- und -recyclingmechanismen kennzeichnen. Ohne Rab43 trug MyD88 weniger dieser Marken, entging dem rechtzeitigen Abbau und trieb weiterhin entzündliche Signalübertragung voran.
Wie diese Entdeckung künftige Therapien leiten könnte
Indem die Studie Rab43 mit dem kontrollierten Abbau von MyD88 verknüpft, zeigt sie ein eingebautes Sicherheitssystem, das verhindert, dass Makrophagenreaktionen nach Erkennung einer Bedrohung überschiessen. Rab43 fördert die Expression mehrerer Enzyme, die Ubiquitinmarken an MyD88 anbringen oder bearbeiten, und sorgt so dafür, dass dieser potente Signalknoten nicht dauerhaft eingeschaltet bleibt. Fehlt Rab43 oder ist vermindert, verweilt MyD88 länger, entzündliche Kaskaden laufen ungehindert und das Lungengewebe leidet. Obwohl auf Rab43 basierende Therapien noch nicht verfügbar sind, markieren diese Ergebnisse Rab43 und den MyD88-Abbauweg als vielversprechende Ziele für künftige Wirkstoffe, die lebensbedrohliche Lungenentzündungen beruhigen sollen, ohne die Infektabwehr zu beeinträchtigen.
Zitation: Wang, Y., Liu, X., Zhu, Z. et al. Rab43 mitigates the inflammatory response in acute lung injury via MyD88 ubiquitination. Sci Rep 16, 4843 (2026). https://doi.org/10.1038/s41598-026-35187-0
Schlüsselwörter: akute Lungenschädigung, Makrophagen, Entzündung, Rab43, MyD88