Clear Sky Science · de
KI-gestütztes Framework zur genauen Erkennung der Alzheimer-Krankheit im EEG
Warum Hirnwellen für Gedächtnisverlust wichtig sind
Die Alzheimer-Krankheit zersetzt langsam das Gedächtnis und die Selbstständigkeit, doch wenn Symptome offensichtlich werden, ist bereits viel Schaden entstanden. Ärztinnen und Ärzte brauchen dringend Möglichkeiten, die Krankheit früher zu erkennen – mit Instrumenten, die sicher, erschwinglich und für Routineuntersuchungen praktisch sind. Diese Studie untersucht, ob einfache Aufzeichnungen von Hirnwellen – Elektroenzephalogramme, kurz EEG – kombiniert mit moderner künstlicher Intelligenz verborgene Zeichen von Alzheimer offenbaren können, lange bevor sie in Gehirnscans oder im Alltag sichtbar werden.
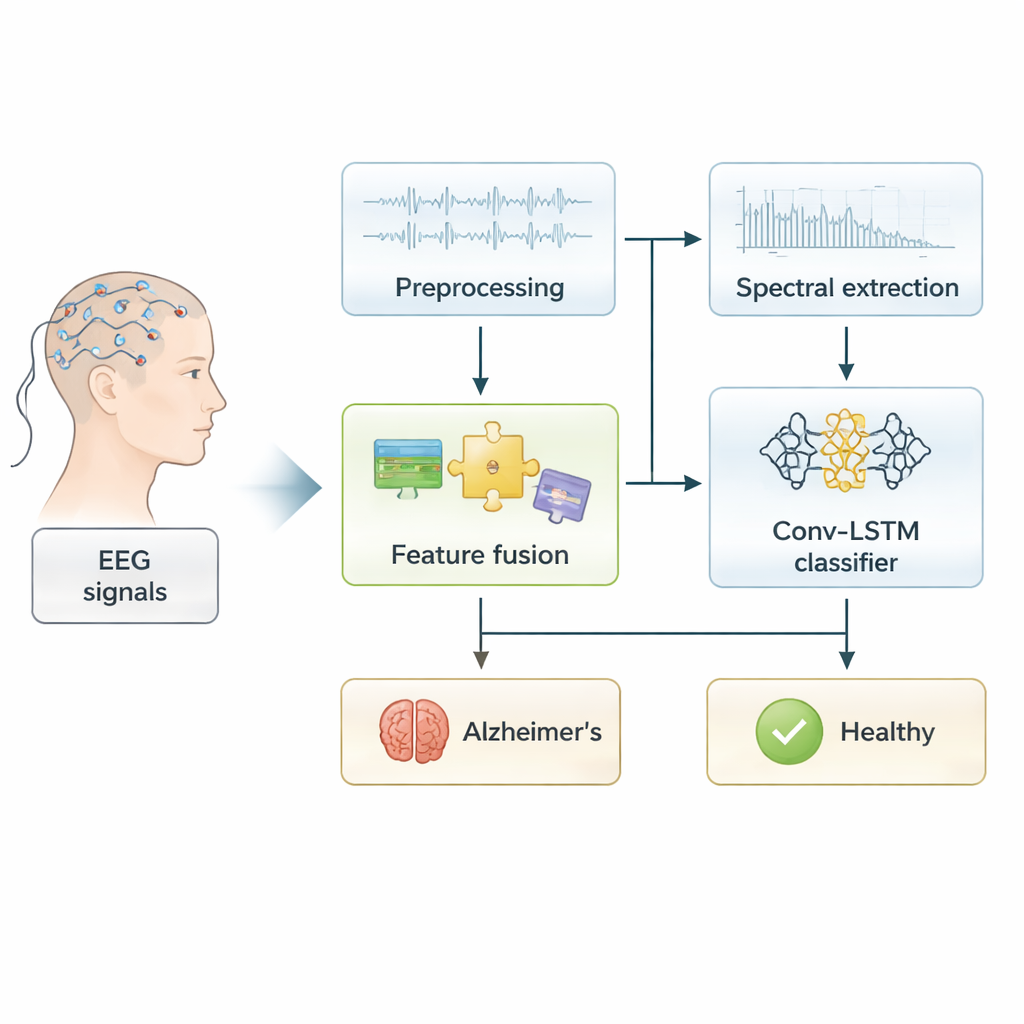
Dem Gehirn zuhören ohne Operation
EEG ist ein schmerzfreier Test, bei dem kleine Elektroden auf der Kopfhaut die elektrische Aktivität des Gehirns messen. Er ist deutlich günstiger und mobiler als MRT- oder PET-Scans und lässt sich häufig wiederholen. Rohe EEG-Signale sind jedoch unordentlich: Sie enthalten viel Rauschen durch Blinzeln, Muskelbewegungen und Umgebungsstörungen, und die mit Alzheimer verbundenen Muster können subtil sein sowie über viele Hirnregionen und Frequenzen verteilt auftreten. Traditionell konzentrierten sich Forschende entweder auf von Hand entwickelte mathematische Zusammenfassungen dieser Signale oder auf Deep-Learning-Modelle, die Muster direkt aus den Rohdaten lernen. Beide Ansätze haben Stärken, aber auch erhebliche Schwachstellen.
Zwei Sichtweisen auf Hirnaktivität verbinden
Die Autorinnen und Autoren schlagen eine hybride Strategie vor, die das Beste aus beiden Welten vereint. Zuerst bereinigen sie die EEG-Aufzeichnungen, indem unerwünschtes Rauschen herausgefiltert und langsame Drift im Signal korrigiert wird. Dann extrahieren sie „spektrale“ Merkmale, die beschreiben, wie die elektrische Leistung des Gehirns über verschiedene Frequenzbänder verteilt ist – langsame Wellen, die etwa mit Schläfrigkeit verbunden sind, gegenüber schnelleren Rhythmen, die mit Aufmerksamkeit assoziiert werden. Diese Maße sind seit Langem dafür bekannt, sich bei Demenz zu verändern. Gleichzeitig betrachtet ein speziell gestaltetes Convolutional Neural Network (CNN) die EEG-Daten ganzheitlicher und lernt automatisch komplexe räumliche Muster, die für menschliche Expertinnen und Experten nicht offensichtlich sein müssen.
Der KI beibringen, Veränderungen über die Zeit zu lesen
Statt diese beiden Merkmalsätze getrennt zu behandeln, verschmilzt das System sie zu einer einzigen, reichhaltigen Beschreibung der Hirnaktivität jeder Person. Diese kombinierte Repräsentation wird dann in ein fortgeschritteneres Netzwerk eingespeist, das als Convolutional Long Short-Term Memory (Conv-LSTM) Modell bezeichnet wird. Der „konvolutionale“ Anteil erfasst, wie Aktivität über die Kopfhaut organisiert ist, während der „LSTM“-Anteil darauf ausgelegt ist, nachzuverfolgen, wie sich Muster über die Zeit entwickeln – ähnlich dem Verfolgen von Phrasen in gesprochener Sprache. Effektiv lernt das Modell sowohl wo als auch wann Alzheimer-assoziierte Veränderungen im EEG auftreten, und zwar mit rund 0,9 Millionen trainierbaren Parametern – kompakt genug, um auf Standardhardware zu laufen.
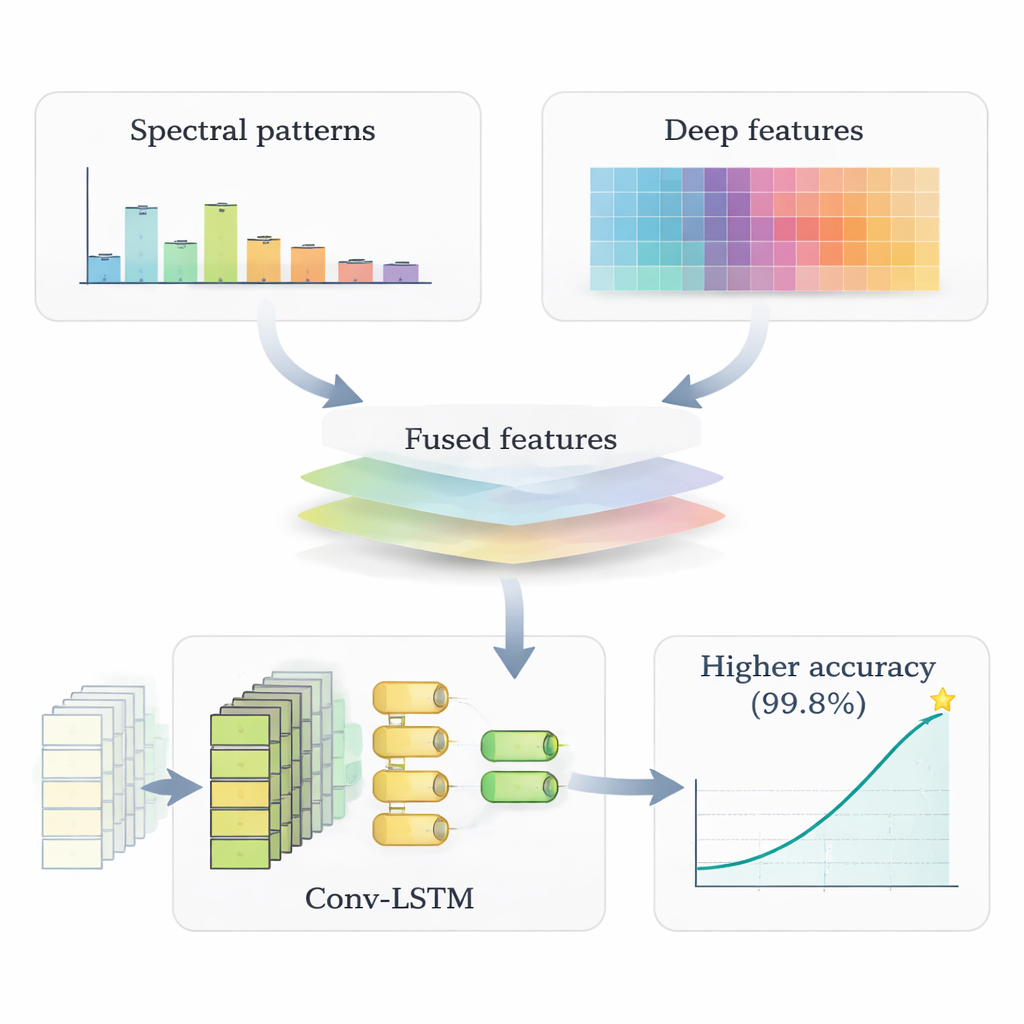
Wie gut funktioniert das System?
Die Forschenden testeten ihr Framework an Ruhestands-EEG-Daten älterer Erwachsener mit und ohne Alzheimer-Krankheit. Sie teilten die Aufzeichnungen in getrennte Sets für Training, Validierung und abschließende Tests auf und bewerteten die Leistung mit gängigen Genauigkeits- und Zuverlässigkeitsmaßen. Das auf Fusion basierende Conv-LSTM-Modell unterschied Alzheimer- von Nicht-Alzheimer-Fällen in 99,8 % der Fälle korrekt – deutlich besser als mehrere Vergleichssysteme, darunter alleinstehende CNNs, alleinstehende LSTM-Netzwerke und konventionelle maschinelle Lernansätze. Modelle, denen entweder die spektralen Merkmale oder die tief gelernten Merkmale fehlten, waren durchweg weniger genau, was den Nutzen der Kombination komplementärer Blickwinkel auf dieselben Hirnsignale unterstreicht.
Was das für Patientinnen, Patienten und Kliniken bedeuten könnte
Für Nicht-Spezialistinnen und -Spezialisten ist die Quintessenz klar: Indem künstliche Intelligenz genauer auf Hirnwellen hört, verwandelt diese Methode einen vertrauten, risikoarmen Test in ein leistungsfähiges Frühwarnsystem für die Alzheimer-Krankheit. Die Arbeit deutet darauf hin, dass ein relativ leichtgewichtiges, automatisiertes EEG-basiertes Werkzeug Klinikerinnen und Klinikern helfen könnte, Patienten in alltäglichen Situationen zu screenen und diejenigen zu markieren, die eine engere Nachverfolgung oder weitergehende Bildgebung benötigen. Während vor einer Anwendung zur Steuerung von Behandlungsentscheidungen noch größere und vielfältigere Studien erforderlich sind, weist diese Forschung in eine Zukunft, in der routinemäßige Hirnwellenaufzeichnungen, interpretiert von intelligenten Algorithmen, helfen, Demenz früher und genauer zu erkennen – und somit Patientinnen, Patienten und Familien mehr Zeit zu verschaffen, um zu planen und von aufkommenden Therapien zu profitieren.
Zitation: Hemalatha, B., Venkatachalam, K., Siuly, S. et al. AI-driven framework for accurate detection of Alzheimer’s disease in EEG. Sci Rep 16, 5509 (2026). https://doi.org/10.1038/s41598-026-35184-3
Schlüsselwörter: Alzheimer-Krankheit, EEG-Hirnwellen, Deep Learning, Früherkennung, medizinische KI