Clear Sky Science · de
Bakterien aus Lebensmitteln und der Darmmikrobiota produzieren Methylglyoxal und dieses Metabolit führt zur Bildung bioaktiver 1‑acetyl‑β‑carbolin‑Alkaloide
Warum das Chemielabor in Ihrem Darm wichtig ist
In unseren Därmen und in vielen fermentierten Lebensmitteln wandeln Billionen von Bakterien fortlaufend die Zucker, die wir essen, in eine Reihe chemischer Nebenprodukte um. Diese Studie untersucht einen solchen Pfad im Detail: wie manche verbreiteten Bakterien Zucker in eine hochreaktive Verbindung namens Methylglyoxal verwandeln und daraus eine Familie bioaktiver Moleküle, die 1‑acetyl‑β‑carboline heißen, entstehen. Da diese Substanzen sowohl mit Krankheitsprozessen als auch mit potenziellen neuen Wirkstoffen in Verbindung gebracht werden, könnte das Verständnis, wann und wie Bakterien sie produzieren, unser Denken über Nahrung, das Mikrobiom und Gesundheit verändern.
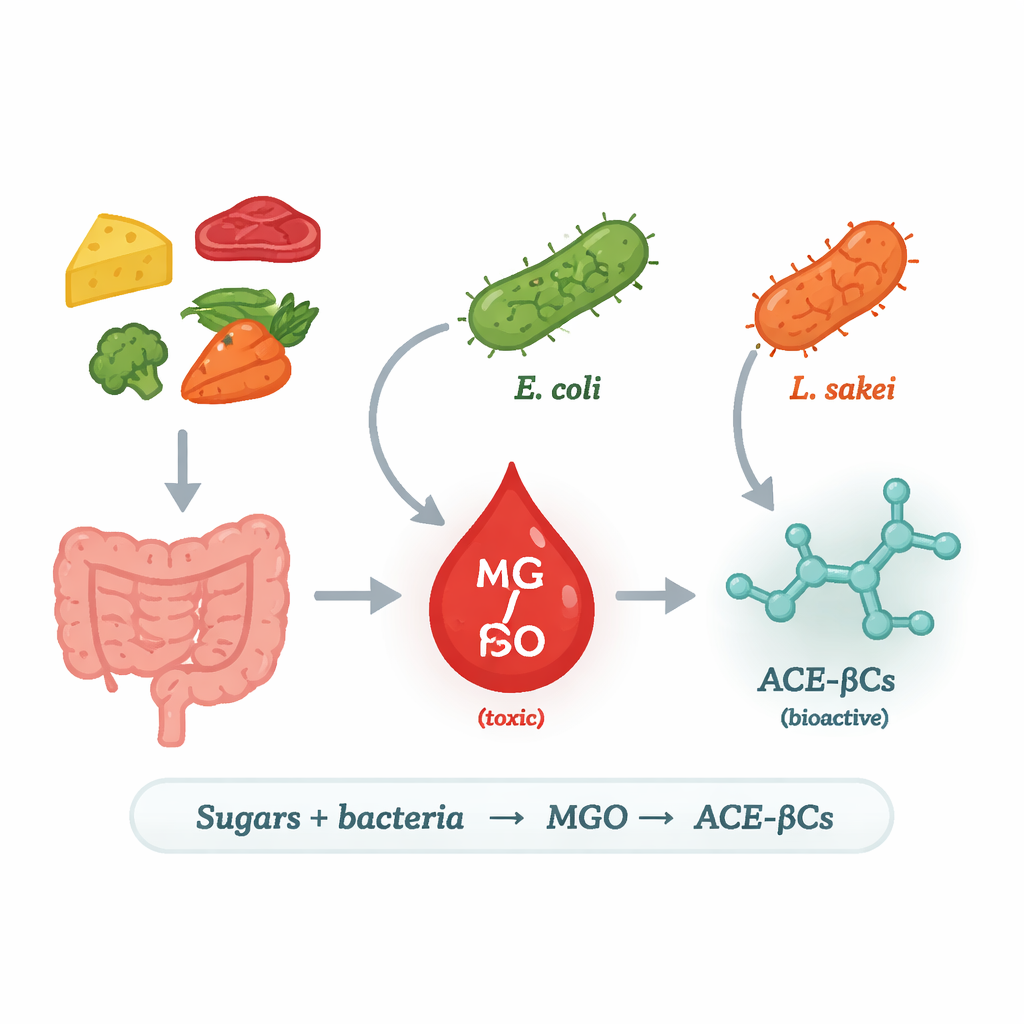
Vom Alltagszucker zu einem riskanten Molekül
Die Forscher konzentrierten sich auf Methylglyoxal (MGO), ein sehr reaktives, toxisches Nebenprodukt des Zuckerabbaus. Beim Menschen steht ein Überschuss an MGO im Zusammenhang mit Diabetes, Herzkrankheiten und Neurodegeneration, weil es Proteine und DNA schädigen kann. Unsere Zellen halten MGO normalerweise mit Entgiftungssystemen in Schach, doch sie sind nicht die einzige Quelle: Auch Bakterien können MGO herstellen. Bei einigen Mikroben wandelt ein Enzym namens Methylglyoxal‑Synthase (MgsA) ein Zwischenprodukt des Zuckerstoffwechsels direkt in MGO um und schafft damit eine „Abkürzung“ im Energiestoffwechsel. Das Team fragte, welche Lebensmittel‑ und Darmbakterien diese Route nutzen, unter welchen Bedingungen das geschieht und was mit dem freigesetzten MGO passiert.
Wer sind die bakteriellen Produzenten?
Um das zu klären, kultivierten die Wissenschaftler mehrere Stämme Milchsäurebakterien, die häufig in Lebensmitteln vorkommen, zusammen mit einem Laborstamm von Escherichia coli in einem kontrollierten Medium, das entweder Glukose oder Galaktose enthielt. Sie verfolgten dann mit hochpräziser Chromatographie und Massenspektrometrie über die Zeit MGO und zwei verwandte Alkaloide in der Kulturflüssigkeit. Nur E. coli und die fleischassoziierte Art Lactilactobacillus sakei produzierten nennenswerte Mengen an MGO und den Alkaloiden; andere getestete Milchsäurebakterien taten dies nicht. Eine Genomanalyse deckte den entscheidenden Unterschied auf: E. coli und L. sakei tragen das Gen für MgsA, während die meisten ihrer milchsäureverwandten Arten dies nicht tun. Als die Forscher das mgsA‑Gen von L. sakei in einen nicht produzierenden Stamm einfügten, begann das gentechnisch veränderte Bakterium, sowohl MGO als auch die Alkaloide herzustellen — ein klarer Beleg für die Verbindung von MgsA mit diesem Stoffwechselweg.
Wie aus toxischem MGO bioaktive Alkaloide werden
Die nächste Frage war, was mit dem MGO geschieht, sobald es gebildet ist. Das Team richtete seinen Fokus auf 1‑acetyl‑β‑carbolin‑Alkaloide (ACE‑βCs), kleine Moleküle, denen antimikrobielle, antiinflammatorische und anticancerogene Aktivitäten zugeschrieben werden. Sie zeigten, dass beim Wachstum MGO‑produzierender Bakterien in Gegenwart der Aminosäure L‑Tryptophan die Konzentrationen zweier ACE‑βCs — 1‑acetyl‑β‑carbolin und seine 3‑carboxylische Säureform — stark anstiegen. Das Hinzufügen von extra MGO zum Medium förderte ebenfalls ihre Bildung. Das deutet darauf hin, dass MGO aus den Zellen austritt und spontan mit L‑Tryptophan in der umgebenden Flüssigkeit reagiert, ohne zusätzliche Enzyme, und so diese bioaktiven Verbindungen erzeugt. Anders gesagt: dieselbe Chemie, die MGO gefährlich macht, verwandelt es auch in komplexere Moleküle, die nützliche Effekte haben können.
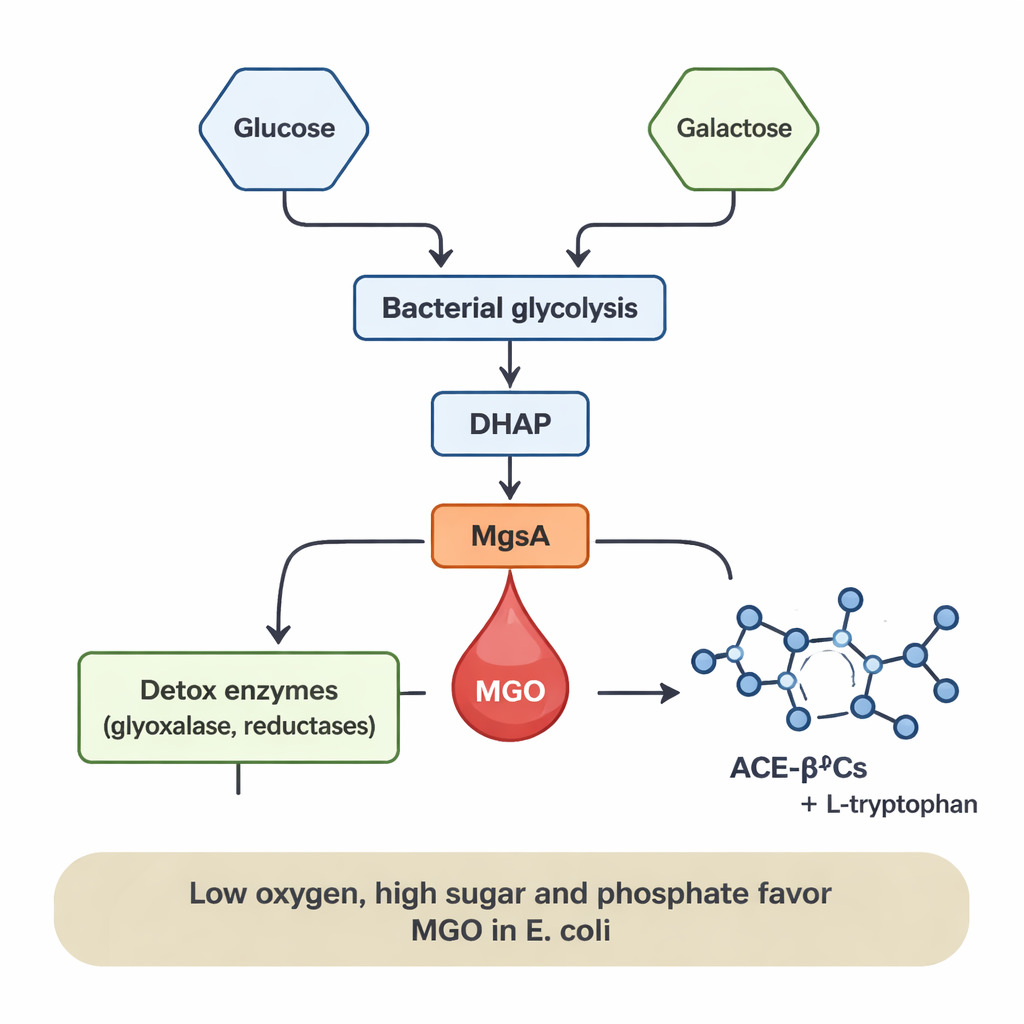
Was den Schalter hoch- oder herunterdreht
Die MGO‑Produktion war nicht konstant; sie hing stark von der Ernährung und Umgebung der Bakterien ab. Bei E. coli trat MGO nur auf, wenn Glukose vorhanden war, und die Mengen stiegen mit zunehmender Glukosekonzentration. Das Hinzufügen von Phosphat, einem üblichen Mineralsalz, verstärkte die MGO‑Bildung um ein Mehrfaches, vermutlich weil es die Anreicherung phosphorylierter Zuckerzwischenprodukte fördert, die in die MgsA‑Abkürzung eingespeist werden. Sauerstoffarme (anaerobe) Bedingungen — ähnlich denen im menschlichen Darm — begünstigten ebenfalls die MGO‑Freisetzung, während gut belüftete, sauerstoffreiche Bedingungen sie stark reduzierten, obwohl die Bakterien weiterhin gut wuchsen. Im Gegensatz dazu erzeugte L. sakei hauptsächlich dann MGO, wenn es auf Galaktose kultiviert wurde, und die Produktion stieg mit höheren Galaktosewerten. Diese Muster deuten darauf hin, dass immer dann, wenn der Zuckerfluss durch den bakteriellen Stoffwechsel hoch und der Sauerstoff begrenzt ist, MGO als eine Art „Überdruckventil“ wirken kann, das die Belastung durch sich anhäufende Zuckerzwischenprodukte verringert.
Was das für Lebensmittel und Gesundheit bedeuten könnte
Die Ergebnisse legen nahe, dass nicht alle Darm‑ oder Lebensmittelbakterien gleich gut MGO und ACE‑βCs bilden können. Arten, die das Enzym MgsA tragen, wie bestimmte L. sakei‑Stämme und E. coli, können bedeutende Beiträge leisten, besonders in zuckerreichen, sauerstoffarmen Umgebungen wie dem Darm oder einigen Fermentationen. Das von ihnen ausgeschiedene MGO könnte die chemische Belastung des Wirtsgewebes erhöhen, doch seine Umwandlung in ACE‑βC‑Alkaloide könnte zugleich einen Teil dieses reaktiven Moleküls „auffangen“ und dabei Verbindungen mit eigenen biologischen Wirkungen erzeugen. Obwohl diese Studie in Laboransätzen durchgeführt wurde, hebt sie eine plausible Route hervor, über die Ernährung, Mikrobiota‑Zusammensetzung und bakterieller Stoffwechsel gemeinsam das Gleichgewicht zwischen schädlichen und potenziell nützlichen Chemikalien in unserem Körper formen können, und sie weist auf ACE‑βCs als mögliche Marker bakterieller MGO‑Produktion in Lebensmitteln und dem Darm hin.
Zitation: Herraiz, T., Sánchez-Arroyo, A., de las Rivas, B. et al. Bacteria from foods and gut microbiota produce methylglyoxal and this metabolite leads to the formation of bioactive 1-acetyl-β-carboline alkaloids. Sci Rep 16, 4905 (2026). https://doi.org/10.1038/s41598-026-35162-9
Schlüsselwörter: Darmmikrobiota, Methylglyoxal, bakterieller Stoffwechsel, Lebensmittelfermentation, Beta‑carbolin‑Alkaloide