Clear Sky Science · de
Herleitung eines intrinsischen Biomarkers für Gehirnaktivität zur frühesten Vorhersage kognitiven Abbaus
Warum frühe Veränderungen im Gehirn wichtig sind
Viele ältere Menschen bemerken subtile Gedächtnislücken lange bevor ein Arzt Demenz diagnostizieren kann. In diesem Stadium sehen herkömmliche Hirnscans und Bluttests oft normal aus, dennoch kann der zugrunde liegende Krankheitsprozess bereits begonnen haben. Diese Studie untersucht, ob ein einfacher, nicht-invasiver Gehirnwellen-Test — das Elektroenzephalogramm (EEG) — sehr frühe Änderungen der Gehirnfunktion aufdecken und zuverlässig vorhersagen kann, wer Jahre später mit hoher Wahrscheinlichkeit einen schweren kognitiven Abbau erfahren wird.
Den leisen Signalen des Gehirns zuhören
Die Forschenden konzentrierten sich auf Personen mit „subjektivem kognitiven Abbau“ (SCI): ältere Erwachsene, die das Gefühl haben, ihr Gedächtnis lasse nach, aber in Standardtests noch normal abschneiden. 88 solcher Freiwilligen im Alter von 52 bis 85 Jahren hatten 20 Minuten Ruhe-EEG mit geschlossenen Augen, anschließend wurden sie 5–7 Jahre lang nachbeobachtet. Während der Nachbeobachtungszeit verfolgten Ärztinnen und Ärzte den kognitiven Zustand jeder Person mit etablierten Bewertungsinstrumenten. Am Ende dieses Zeitraums blieben einige Teilnehmende stabil, während andere in einen milden kognitiven Abbau oder in eine Demenz übergingen. Diese Ergebnisse ermöglichten es dem Team zu prüfen, ob subtile Muster im ursprünglichen EEG hätten vorhersagen können, wer später verschlechtert würde.
Gehirnwellen in einen prädiktiven Fingerabdruck verwandeln
Statt das EEG visuell zu inspizieren, nutzte das Team quantitatives EEG (qEEG), das rohe Gehirnwellen in tausende numerische Merkmale umwandelt. Diese Merkmale erfassen, wie stark verschiedene Frequenzbänder sind (etwa Alpha- und Theta-Rhythmen), wie gut entfernte Hirnregionen miteinander synchronisieren (Konnektivität und Phasenversatz) und wie komplex oder unorganisiert das Gesamtaktivitätsmuster wirkt. Da auch normales Altern das EEG verändert, passten die Forschenden alle Merkmale mathematisch für das Alter an und standardisierten sie so, dass „Null“ den erwarteten Wert einer gesunden Person desselben Alters repräsentiert. Um Overfitting zu vermeiden, reduzierten sie systematisch mehr als 6.000 Kandidatenmaße auf eine kompakte Menge, die stabil, nicht redundant und am besten darin war, stabile von sich verschlechternden Personen zu trennen.
Maschinelles Lernen als Kristallkugel
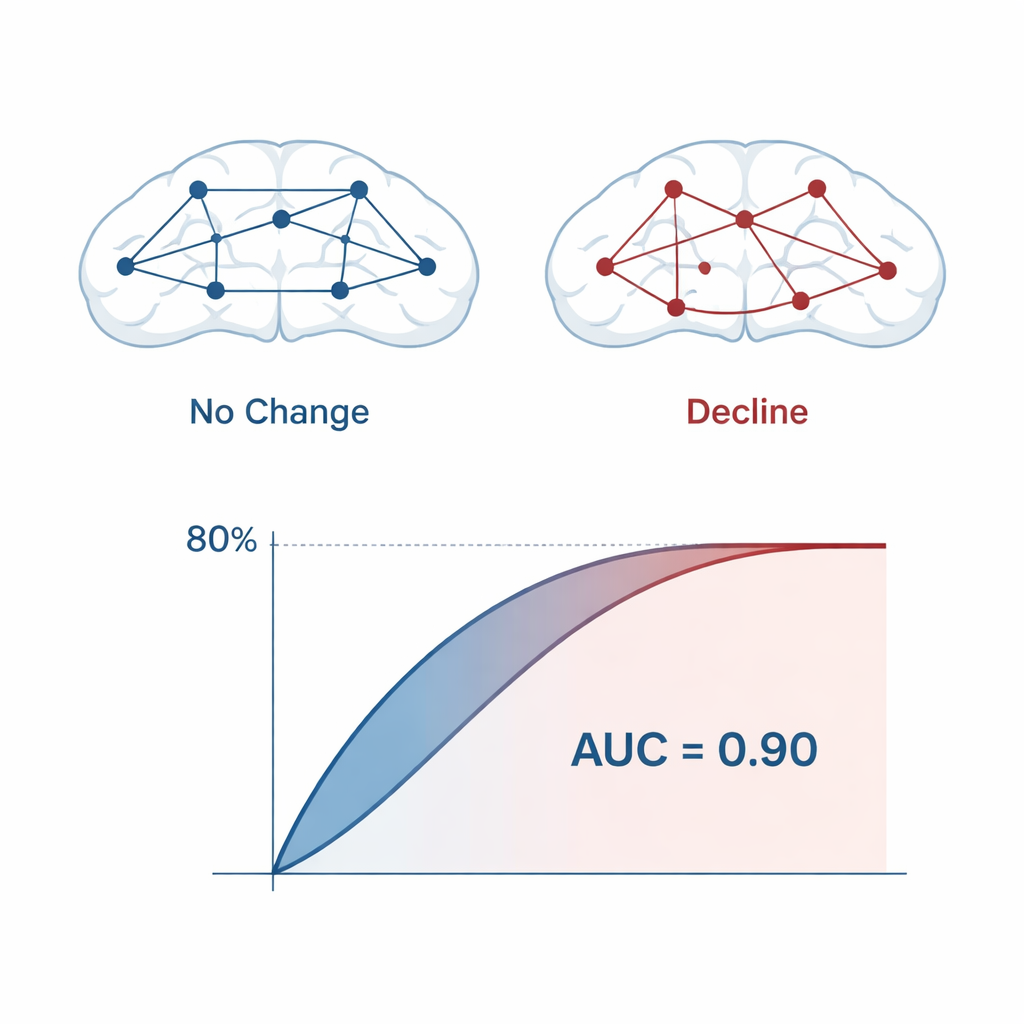
Mit diesem reduzierten Merkmalsatz trainierte das Team mehrere Modelle des maschinellen Lernens — logistische Regression, Support Vector Machines und Random Forests — um die Wahrscheinlichkeit eines zukünftigen Abfalls für jede Teilnehmerin und jeden Teilnehmer zu schätzen. Wiederholte Kreuzvalidierung und ein spezialisierter Bootstrap-Ansatz wurden verwendet, um die Leistungsfähigkeit so realistisch wie möglich zu beurteilen. Über die Modelle hinweg lag die Vorhersagegenauigkeit bei etwa 80 %, mit einer Fläche unter der ROC-Kurve (AUC) von rund 0,90, was auf eine starke Unterscheidung zwischen stabilen und sich verschlechternden Personen hinweist. Die finalen fixierten Modelle nutzten nur 14 qEEG-Merkmale, überwiegend aus frontalen Hirnregionen, die mit einer kleinen Elektrodenanzahl aufgezeichnet wurden, wodurch der Ansatz für den routinemäßigen klinischen Einsatz praktikabel wird.
Was sich im Gehirn ändert
Die Merkmale, die am stärksten zur genauen Vorhersage beitrugen, deuteten auf frühe Störungen in der Kommunikation zwischen Hirnarealen hin. Messgrößen der Konnektivität, insbesondere Phasenversatz und Asymmetrie zwischen linken und rechten frontalen Regionen, waren zentral für das Modell. Auffälligkeiten in den Alpha- und Theta-Frequenzbändern fielen besonders auf: Zunehmende oder verschobene Theta-Aktivität wurde in anderer Forschung mit Hippocampus-Atrophie und kortikaler Ausdünnung in Verbindung gebracht, während Änderungen in Alpha-Leistung und -Frequenz die ersten kompensatorischen Reaktionen des Gehirns auf aufkommende Schäden widerspiegeln könnten. Wichtig ist, dass kein einzelnes EEG-Merkmal die ganze Geschichte erzählen konnte. Es war die spezifische Kombination — der biomarkerartige „Fingerabdruck“ — die ein erhöhtes Risiko Jahre vor dem Auftreten voller Symptome signalisierte.
Das Instrument in der Praxis prüfen
Um zu testen, ob ihr Biomarker über die ursprüngliche Kohorte hinaus generalisiert, prüften die Forschenden ihn an zwei unabhängigen Kohorten aus den USA und Italien, jeweils mit eigenen Aufnahmebedingungen und Patienteneigenschaften. Wie zu erwarten bei wirklich neuen Daten fiel die Genauigkeit moderat auf etwa 60–70 %, doch das Modell schnitt weiterhin deutlich besser als Zufall ab, was darauf hindeutet, dass das erfasste Signal robust ist. Das Team zeigte außerdem, dass Klinikerinnen und Kliniker den Entscheidungs-Schwellenwert anpassen können: Eine Absenkung erhöht die Sensitivität (mehr zukünftige Absteiger werden erkannt, auf Kosten mehrerer Fehlalarme), während eine Anhebung die Spezifität erhöht (weniger falsch-positive Befunde, aber mehr verpasste Fälle). Diese Flexibilität erlaubt es Behandlern, das Instrument an unterschiedliche klinische Prioritäten anzupassen.
Was das für Patientinnen, Patienten und Behandler bedeutet
Einfach gesagt legt diese Arbeit nahe, dass eine kurze, schmerzfreie EEG-Aufnahme — mit nur wenigen Elektroden über der Stirn — älteren Menschen helfen kann, die heute noch normal erscheinen, aber ein hohes Risiko für kognitiven Abbau in den nächsten Jahren haben. Zwar sind größere Studien und Vergleiche mit anderen Biomarkern weiterhin erforderlich, doch ist der Ansatz kostengünstig, nicht-invasiv und wiederholbar, was ihn für ein breites Screening attraktiv macht, insbesondere dort, wo aufwändige Bildgebung oder Nervenwasser-Tests unpraktisch sind. Wird er weiter validiert, könnten solche EEG-basierten Biomarker Ärzten helfen, früher einzugreifen, den Krankheitsverlauf zu überwachen und Teilnehmende für klinische Studien in genau jener Phase auszuwählen, in der Therapien am ehesten nachhaltigen Nutzen bringen.
Zitation: Prichep, L.S., Zaidi, S.N., Brink, K. et al. Derivation of an intrinsic brain activity biomarker for the earliest prediction of cognitive decline. Sci Rep 16, 5500 (2026). https://doi.org/10.1038/s41598-026-35144-x
Schlüsselwörter: frühe Demenzvorhersage, EEG-Gehirnwellen, subjektiver kognitiver Abbau, maschinelles Lernen Biomarker, Alzheimer-Risiko