Clear Sky Science · de
Entwurf und Leistungsanalyse eines vertikal gestapelten Gate-All-Around-Nanosheet-FET mit eingebetteter Nanohöhle für Biosensoranwendungen
Kleinere Sensoren für frühere Warnungen
Die frühzeitige Erkennung von Krebs hängt oft davon ab, wie schnell und genau wir winzige Spuren der Erkrankung im Blut oder anderen Körperflüssigkeiten nachweisen können. Dieser Beitrag untersucht einen neuen Typ ultrasensibler elektronischer Sensoren – gebaut mit derselben Technologie, die in fortschrittlichen Computerchips verwendet wird – der krebsbezogene Moleküle deutlich empfindlicher detektieren kann als viele bestehende Geräte und dabei nur sehr wenig Energie verbraucht.
Aus einem Transistor wird ein Krebsdetektor
Im Mittelpunkt der Arbeit steht ein neu gestalteter Transistor, das grundlegende Schaltelement der Elektronik. Die Autorinnen und Autoren beginnen mit einem hochmodernen Gerätetyp, dem Nanosheet-FET, der bereits von großen Chipherstellern für 3-nm-Prozessoren eingesetzt wird. Sie nutzen ihn als Biosensor, indem sie winzige Hohlräume, sogenannte Nanohöhlen, um das isolierte Gate herum ausbilden, das den Stromfluss steuert. Wenn krebsassoziierte Biomoleküle – etwa Zellen von Darm- oder Nierentumoren, DNA-Stränge oder gelatineartige Proteine – in diese Höhlen gelangen, verändern sie subtil, wie elektrische Ladung im Gerät verteilt wird. Der Transistor „spürt“ diese Änderung als Stromverschiebung und wandelt ein biochemisches Ereignis in ein messbares elektrisches Signal um.
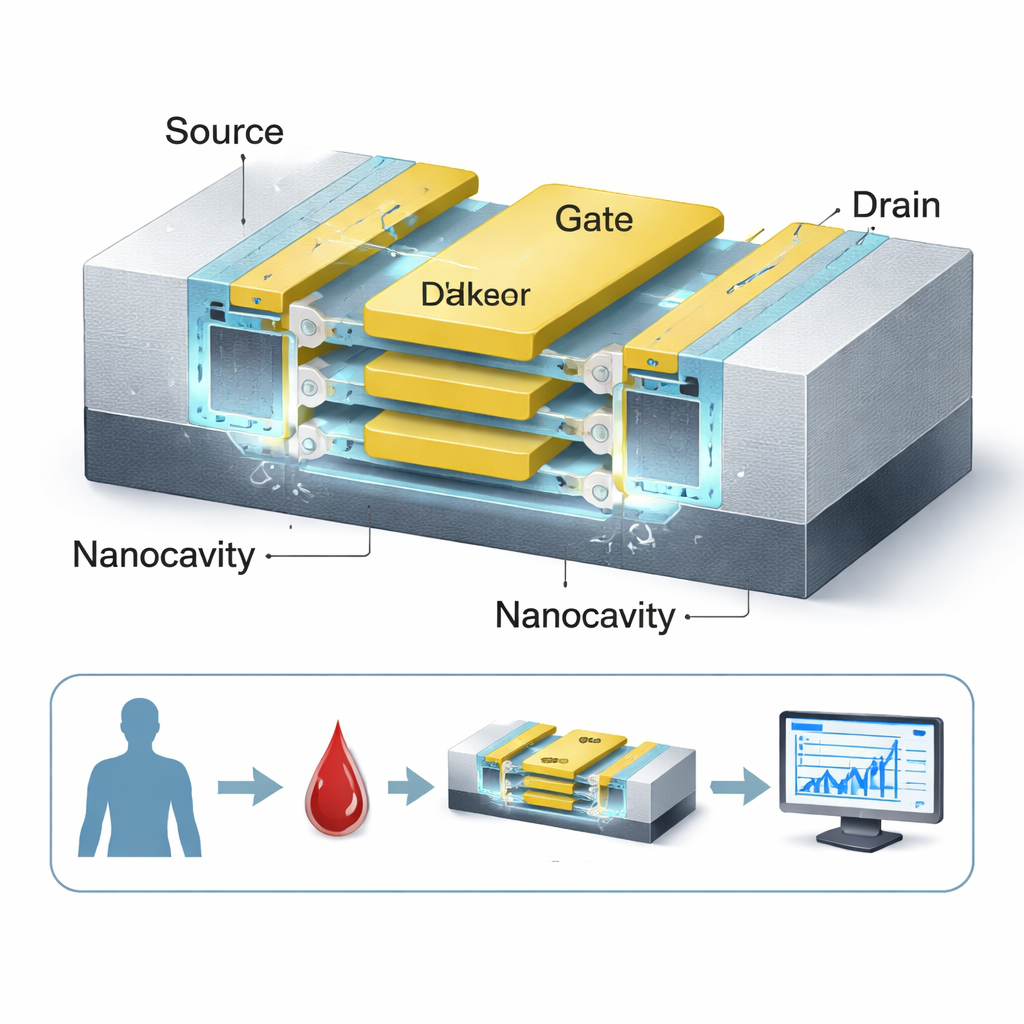
Schichtenstapel für stärkere Signale
Ein wesentliches Merkmal des Designs ist, dass der Sensorkanal nicht aus einem einzelnen Draht besteht, sondern aus drei extrem dünnen Siliziumschichten, die vertikal gestapelt und von einem gemeinsamen Gate umgeben sind. Diese Gate-All-Around-Struktur gibt dem Gate eine deutlich stärkere Kontrolle über den Kanal als bei herkömmlichen flachen Transistoren, was das Ein-/Ausschaltverhalten schärft und die messbare Änderung erhöht, wenn Biomoleküle vorhanden sind. Zwei Nanohöhlen sind an beiden Seiten einer hochkappa-Isolatorschicht (HfO₂) positioniert, wodurch der Bereich maximiert wird, in dem Moleküle mit dem elektrischen Feld interagieren können. Da der Kanal „dopingfrei“ ist, also auf starke chemische Dotierung verzichtet, ist die Sensorantwort gleichmäßiger und weniger anfällig für Fertigungsvariationen – ein Vorteil für zuverlässige medizinische Tests.
Feinabstimmung winziger Höhlen für maximale Reaktion
Mithilfe detaillierter Computersimulationen (TCAD) passen die Forschenden systematisch die Geometrie der Höhlen an: deren Länge, Dicke und wie vollständig sie mit Molekülen gefüllt sind. Kürzere und dünnere Höhlen bringen Gate und Kanal in engeren elektro-statischen Kontakt, erhöhen den Einschaltstrom und verringern die sogenannte Subthreshold Swing – ein Maß dafür, wie scharf das Gerät einschaltet. In ihrem optimalen Design erreicht der Sensor einen bemerkenswert niedrigen Swing von etwa 28 Millivolt pro Dekade, deutlich unter der 60 mV/dec-Grenze konventioneller Transistoren. Das bedeutet, dass das Gerät stark auf sehr kleine Spannungsschwankungen reagiert, eine entscheidende Eigenschaft zum Nachweis niedriger Biomolekülkonzentrationen. Zudem zeigen sie, dass mit zunehmender Ausfüllung des Höhlenvolumens – oder wenn Moleküle näher an der Stelle sitzen, an der der Strom beginnt – das Signal stärker wird, wodurch klar wird, wie Dichte und Lage der Zielmoleküle die Leistung beeinflussen.
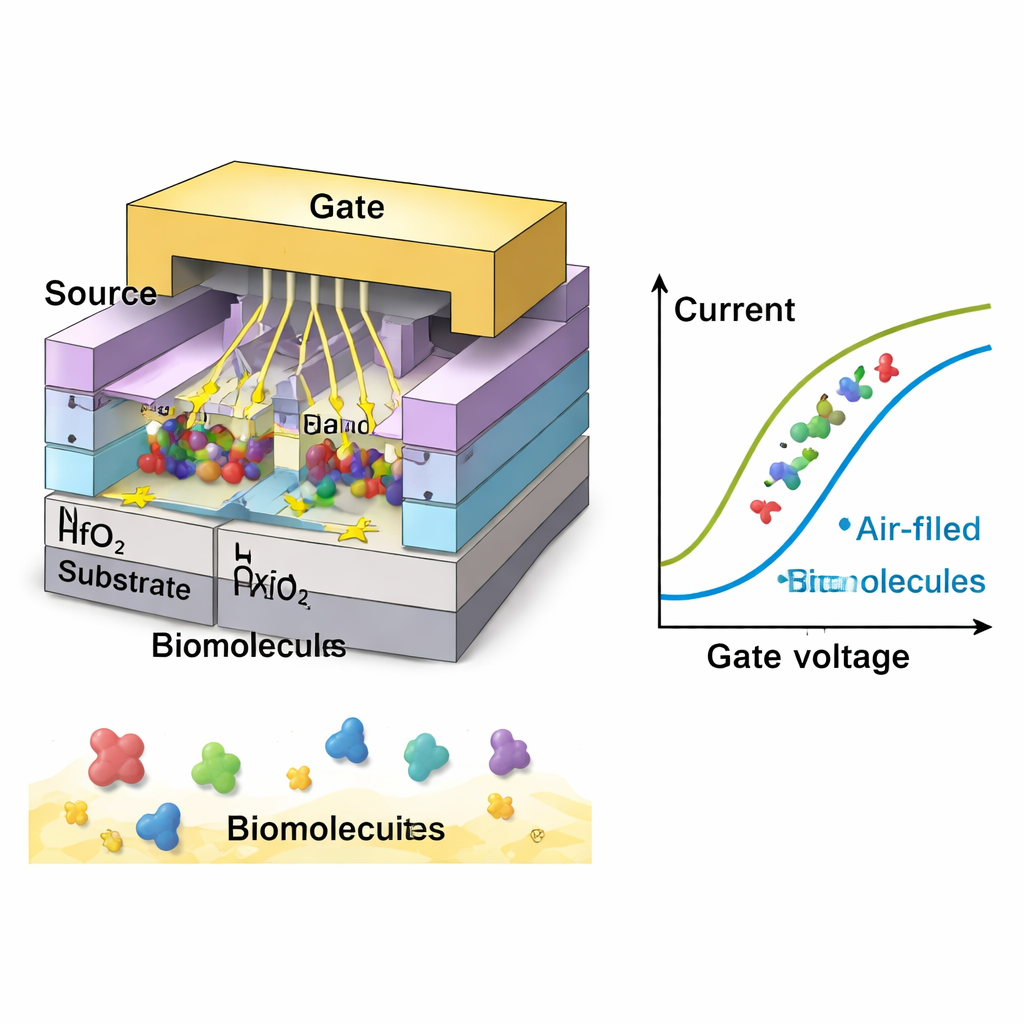
Krebsindikatoren in elektrischen Signalen lesen
Das Team untersucht anschließend, wie sich verschiedene Arten von Biomolekülen elektrisch darstellen würden. Neutrale Spezies mit höherer Permittivität (eine elektrische Eigenschaft, die beschreibt, wie sie sich in einem Feld polarisieren) führen zu größeren Stromänderungen und besserer Empfindlichkeit; die stärkste Reaktion tritt bei einem Wert auf, der typisch für Gelatine und einige dichte biologische Gewebe ist. Geladene Moleküle, wie DNA oder bestimmte Zelloberflächen, können das Signal noch weiter verstärken. In den Simulationen erzeugen negativ geladene Biomoleküle die größte Stromverschiebung, gefolgt von positiv geladenen und dann neutralen. Unter optimalen Bedingungen erreicht das Gerät eine Stromempfindlichkeit, die mehr als 3.000-mal höher ist als der Ausgangswert und bei stark negativ geladenen Proben über 9.000 liegt – damit schlägt es mehrere frühere nanosheet-basierte Biosensoren. Der Sensor zeigt zudem schnelle Ansprechzeiten, stabile Betriebsbedingungen nahe Raumtemperatur und gute Spezifität, also die Fähigkeit, Zielmoleküle von ähnlichen, unerwünschten zu unterscheiden.
Auf dem Weg zu praktischen, chipbasierten Krebs-Tests
Um die Realisierbarkeit des Konzepts zu belegen, skizzieren die Autorinnen und Autoren einen Fertigungsablauf, der eng an die heutige hochentwickelte Chipherstellung angelehnt ist und Standard-Silicon-on-Insulator-Wafer, bekannte Oxid- und Metallschichten sowie übliche Ätzschritte zur Ausbildung der Nanohöhlen verwendet. Da die Struktur kompakt bleibt und mit gängigen CMOS-Prozessen kompatibel ist, könnte sie prinzipiell in dichte Arrays auf einem einzigen Chip integriert werden. Für nichtfachliche Leser ist die Quintessenz, dass diese Arbeit transistorbasierte Biosensoren näher an praktikable Lab-on-a-Chip-Geräte bringt, die eines Tages schnell und hochsensitiv auf Krebsmarker testen könnten – ohne Marker oder komplizierte Chemie und mit Technologien, die denen moderner Elektronik sehr ähnlich sind.
Zitation: Prasanna, R.L., Karumuri, S.R., Sreenivasulu, V.B. et al. Design and performance analysis of a vertically stacked gate-all-around nanosheet FET with embedded nanocavity for biosensing applications. Sci Rep 16, 5508 (2026). https://doi.org/10.1038/s41598-026-35132-1
Schlüsselwörter: Krebs-Biosensor, Nanosheet-FET, Lab-on-a-Chip, Nanohöhlen-Sensor, Früherkennung