Clear Sky Science · de
Die dualspezifische Phosphatase 6 beeinträchtigt die repressive Aktivität von Forkhead Box O1 gegenüber CYP4A11, das die Lipidakkumulation in der Leber vermittelt
Warum Fett in der Leber wichtig ist
Zuviel Fett in der Leber, oft als Fettlebererkrankung bezeichnet, wird mit modernen, zucker‑ und fettreichen Ernährungsgewohnheiten immer häufiger. Während viele Menschen von Cholesterin oder Blutzucker gehört haben, wissen weniger, dass winzige molekulare Schalter in Leberzellen mitentscheiden, ob Fett verbrannt oder gespeichert wird. Diese Studie betrachtet drei solche Schalter — Proteine namens DUSP6, FOXO1 und CYP4A11 — und deckt auf, wie ihr Tauziehen Leberzellen dazu bringen kann, überschüssiges Fett einzulagern. Das Verständnis dieses verborgenen Kontrollsystems könnte den Weg zu neuen Therapien gegen Fettlebererkrankungen und verwandte Stoffwechselprobleme weisen.
Ein verborgener Verkehrsregler in Leberzellen
Die Forschenden konzentrierten sich auf ein Protein namens DUSP6, das hauptsächlich dafür bekannt ist, eine Zell‑Signalstrecke namens ERK‑Pathway auszuschalten. Frühere Arbeiten zeigten, dass Mäuse ohne DUSP6 überraschend resistent gegen ernährungsbedingt entstehende Fettleber waren und niedrigere Mengen an CYP4A‑Enzymen in der Leber aufwiesen, die an der Fettverarbeitung beteiligt sind. Im vorliegenden Ansatz fragte das Team, was DUSP6 in menschlichen, leberabgeleiteten Zellen bewirkt und wie es eine menschliche Version dieser Enzyme, genannt CYP4A11, beeinflussen könnte. Sie verwendeten zwei übliche Leberkrebszelllinien, HepG2 und HuH‑7, als Ersatz für menschliche Leberzellen und setzten sie einer Mischung aus Fettsäuren (Palmitin‑ und Ölsäure) aus, um eine ungesunde, fettreiche Umgebung zu simulieren. 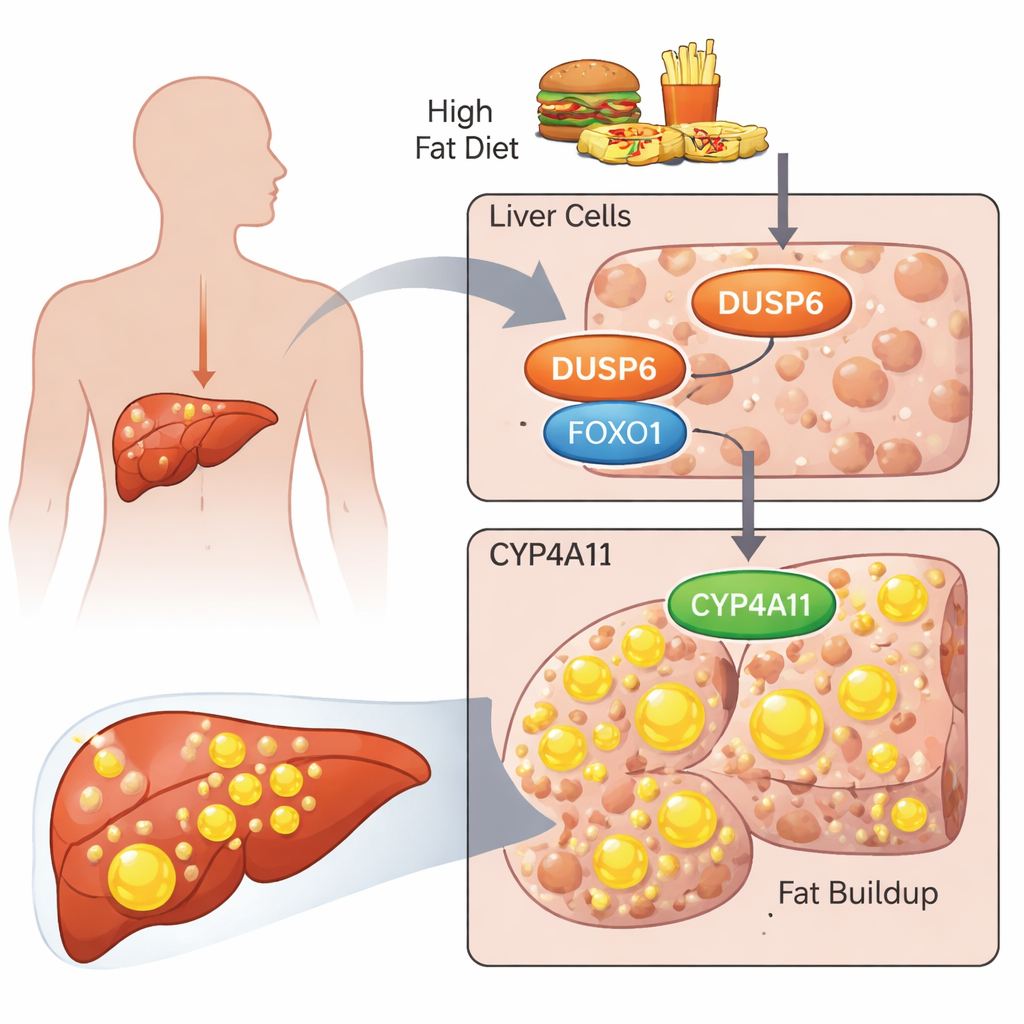
Von Fettsäuren zur fettreichen Zelle
Als die Zellen mit diesen Fettsäuren belastet wurden, bildeten sie sichtbar Fetttropfen, die die Forschenden anfärbten und quantifizierten. Gleichzeitig stiegen die Spiegel von DUSP6 und CYP4A11, zusammen mit aktivierten Formen zweier wichtiger Signalproteine, AKT und FOXO1. Durch gezieltes Ausschalten von DUSP6 mit RNA‑Molekülen kehrten sich diese Veränderungen um: Die Zellen speicherten weniger Fett, CYP4A11‑Spiegel sanken, aber aktiviertes ERK, AKT und FOXO1 nahmen zu. Alleiniges Blockieren des ERK‑Wegs verschlechterte die Fettansammlung tatsächlich, während alleiniges Hemmen von AKT sie verringerte. Wenn sowohl ERK als auch AKT gemeinsam gehemmt wurden, fiel die Fettakkumulation und die CYP4A11‑Spiegel sanken. Diese Experimente verbanden CYP4A11 eng mit dem Ausmaß der Fettablagerung und deuteten darauf hin, dass AKT‑Aktivität besonders wichtig für die Förderung der Fettspeicherung ist.
Eine Bremse für fettfördernde Gene
Ein weiterer wichtiger Akteur ist FOXO1, ein Transkriptionsfaktor — ein Protein, das in den Zellkern gelangen und Gene an‑ oder ausschalten kann. FOXO1 wirkt bekanntermaßen als Bremse für mehrere Mitglieder derselben Enzymfamilie wie CYP4A11. Das Team fand heraus, dass eine Verringerung der FOXO1‑Spiegel dazu führte, dass die Zellen mehr Fett horteten und CYP4A11 anstieg, während eine direkte Erhöhung von CYP4A11 die Zellen noch fetter machte. Im Gegensatz dazu reduzierten erzwungene erhöhte FOXO1‑Mengen sowohl CYP4A11 als auch die Fettakkumulation. Ein Wirkstoff, der die CYP4A11‑Aktivität blockiert (HET0016), verringerte das zusätzliche Fett, das durch niedrige FOXO1‑Spiegel verursacht wurde, und untermauerte damit die Vorstellung, dass CYP4A11 nicht nur ein Zuschauer, sondern ein Treiber der Lipidansammlung ist. Chemische Analysen zeigten, dass HET0016 20‑HETE senkte, ein von CYP4A11 erzeugtes Produkt, das mit oxidativem Stress und Entzündung verbunden ist, und banden diesen Weg weiter an Leberschäden.
Wie DUSP6 die Bremse außer Kraft setzt
Um zu verstehen, wie FOXO1 CYP4A11 kontrolliert, untersuchten die Forschenden die DNA‑Region vor dem CYP4A11‑Gen und fanden Sequenzen, an die FOXO1 binden kann. Mit einem Chromatin‑Immunpräzipitations‑Assay zeigten sie, dass FOXO1 — speziell in seiner nicht phosphorylierten Form — direkt an den CYP4A11‑Promotor bindet, was mit einer repressiven, bremsenden Funktion für dieses Gen vereinbar ist. Co‑Immunpräzipitations‑Experimente zeigten, dass DUSP6 physisch mit FOXO1 interagiert, jedoch nicht mit dessen phosphorylierter Form. Fraktionierungs‑ und Mikroskopiestudien zeigten, dass DUSP6 im Zytoplasma der Zelle sitzt und, wenn vorhanden, mehr FOXO1 aus dem Zellkern fernhält. Wurde DUSP6 herunterreguliert, wanderte mehr FOXO1 in den Kern, wo es DNA binden und CYP4A11 unterdrücken konnte. Effektiv wirkt DUSP6 wie ein Anker, der FOXO1 im Zytoplasma sequestriert und daran hindert, seine Funktion als Bremse für CYP4A11 auszuüben. 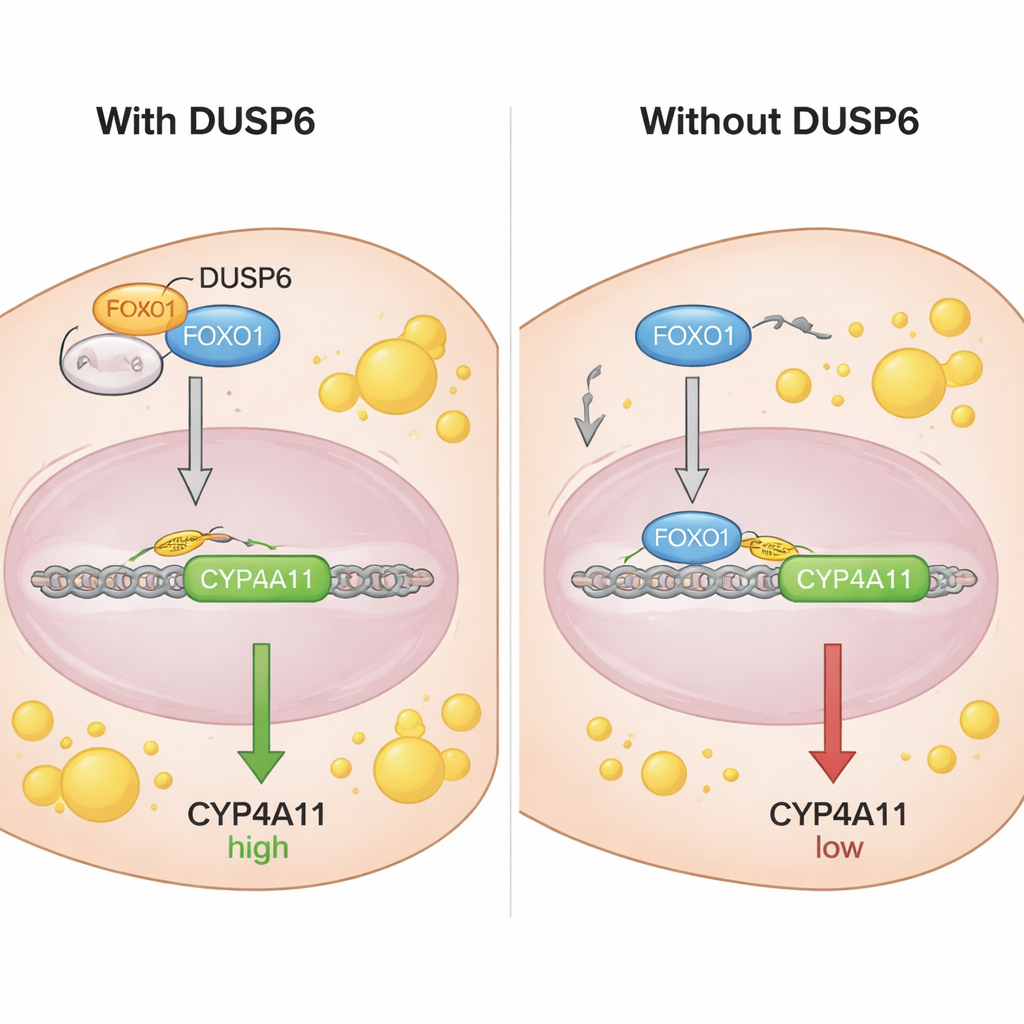
Was das für Fettleber und darüber hinaus bedeutet
Kurz gesagt, diese Arbeit kartiert eine Ereigniskette innerhalb von Leberzellen: DUSP6 hält FOXO1 im Zytoplasma, wodurch FOXO1s Fähigkeit, das CYP4A11‑Gen herunterzufahren, geschwächt wird. Mit FOXO1 außer Gefecht gerät CYP4A11 in einen aktiveren Zustand, was die Zelle dazu treibt, mehr Fett zu speichern und Moleküle wie 20‑HETE zu produzieren, die oxidativen Stress und Entzündungen fördern können. Zwar stammen diese Befunde aus kultivierten, leberabgeleiteten Zellen und nicht aus gesundem menschlichem Lebergewebe, doch heben sie DUSP6 und CYP4A11 als potenzielle neue Ziele zur Behandlung der metabolisch bedingten Steatose hervor. Therapien, die DUSP6‑Aktivität reduzieren oder die Effekte von CYP4A11 dämpfen, könnten theoretisch FOXO1s Bremsfunktion wiederherstellen und helfen, Leberfett unter Kontrolle zu halten.
Zitation: Kimura, M., Saiki, Y., Iwata, K. et al. Dual-specificity phosphatase 6 interferes with the repressive activity of forkhead box O1 towards CYP4A11 that mediates lipid accumulation in the liver. Sci Rep 16, 4795 (2026). https://doi.org/10.1038/s41598-026-35118-z
Schlüsselwörter: Fettlebererkrankung, DUSP6, FOXO1, CYP4A11, Leberstoffwechsel