Clear Sky Science · de
Kristallstruktur von Echinococcus multilocularis Cystatin B zeigt ein neuartiges Merkmal bei klassischen Stefinen
Warum die Geheimwaffe eines Leberparasiten wichtig ist
Alveoläre Echinokokkose ist ein sperriger Name für eine winzige Bandwurminfektion, die sich in der Leber verhält wie ein langsam wachsender Tumor. Sie ist oft tödlich, und die verfügbaren Medikamente wirken nur begrenzt und können schwere Nebenwirkungen haben. Diese Studie untersucht ein bestimmtes Molekül, das der Parasit bildet — ein Protein namens EmCystatin‑B —, um zu verstehen, wie es dem Wurm helfen könnte, unsere Abwehr zu umgehen, und wie es eines Tages als Ansatzpunkt für neue Behandlungen dienen könnte.
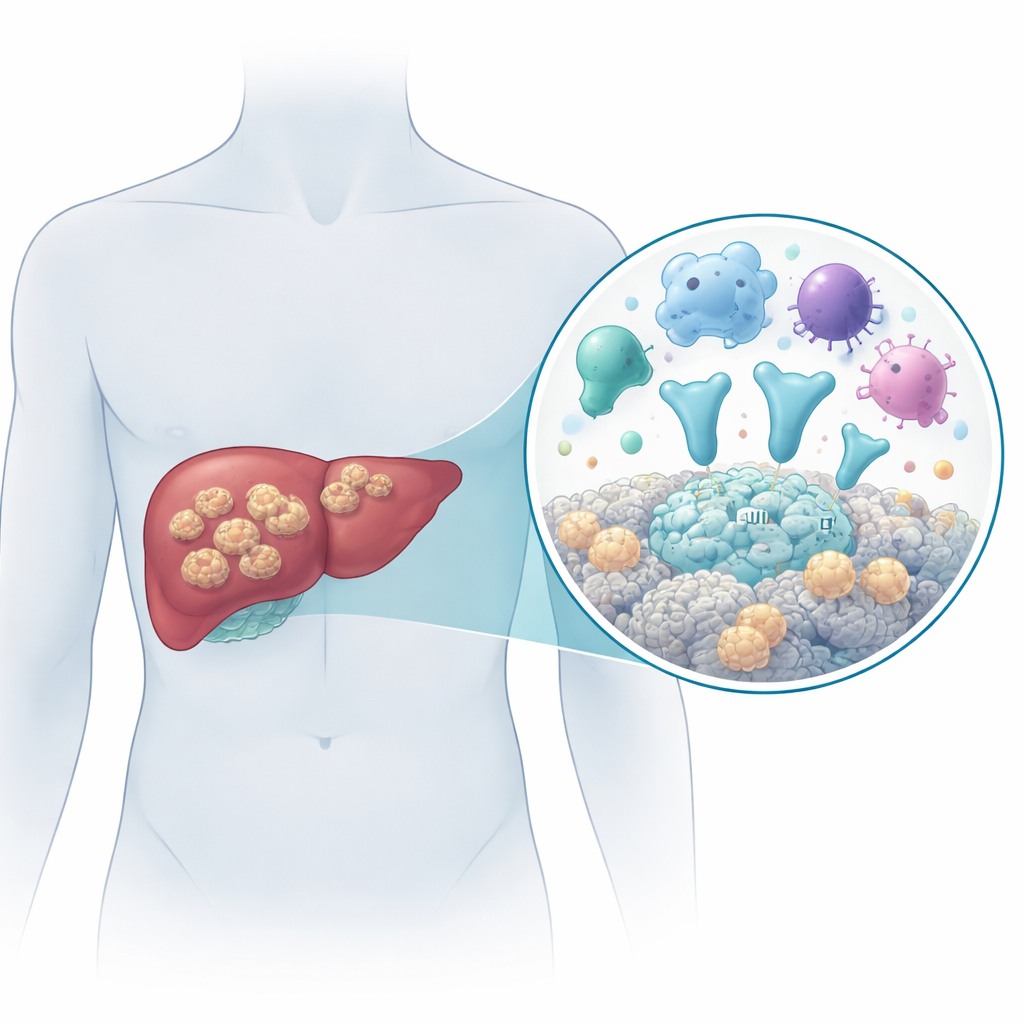
Ein gefährlicher Bandwurm, der wie ein Tumor wächst
Die Krankheit wird durch die Larvenform des Bandwurms Echinococcus multilocularis verursacht. Menschen infizieren sich durch versehentliches Verschlucken von Parasiteneiern, etwa über kontaminierte Nahrung oder Wasser. Einmal im Körper, siedeln sich die Larven vorwiegend in der Leber an und wachsen als viele winzige flüssigkeitsgefüllte Bläschen, die das umliegende Gewebe infiltrieren, in benachbarte Organe wie die Milz übergreifen und manchmal entfernte Orte wie Lunge oder Gehirn erreichen. Ohne effektive Behandlung sterben mehr als neun von zehn Patienten innerhalb von 10 bis 15 Jahren. Eine Operation in Kombination mit langwieriger antiparasitärer Therapie ist derzeit die beste Option, doch die frühe Diagnose ist schwierig und die Medikamente heilen die Infektion nicht zuverlässig. Daher ist es entscheidend, zu verstehen, wie der Parasit auf molekularer Ebene mit dem menschlichen Körper interagiert.
Ein Parasiteneiweiß, das “schneidende” Enzyme lahmlegt
Viele Tiere, einschließlich des Menschen, produzieren eine Familie von Proteinen namens Cystatine, die als Sicherheitsriegel für potente Verdauungsenzyme dienen, die als Cysteine‑Proteasen bekannt sind. Diese Enzyme können andere Proteine zerschneiden und sind wichtig für Prozesse wie den Abbau alter Zellbestandteile und die Aktivierung von Immunantworten. Parasiten haben gelernt, eigene cystatin‑ähnliche Proteine herzustellen, um die Enzyme und das Immunsystem des Wirts zu stören. In dieser Arbeit identifizierten die Forschenden ein cystatin‑ähnliches Protein von E. multilocularis und nannten es EmCystatin‑B. Sie fanden heraus, dass das Gen für EmCystatin‑B in den reifen Larvenköpfen (Protoskolizes) des Parasiten deutlich stärker aktiv ist als im umgebenden Zystengewebe und dass das Protein im Zytoplasma und im Zellkern der Parasitenzellen vorhanden ist, insbesondere in sich teilenden, „stammzellähnlichen“ germinativen Zellen. Labortests zeigten, dass EmCystatin‑B die Aktivität des menschlichen Cathepsin B, einer wichtigen Cysteine‑Protease, die an Immunfunktionen und Gewebeumbau beteiligt ist, stark hemmen kann.
Eine bekannte Form mit unerwarteter Wendung
Um genau zu sehen, wie EmCystatin‑B aufgebaut ist, kristallisierten die Forschenden das gereinigte Protein und lösten seine dreidimensionale Struktur mittels Röntgenkristallographie fast auf atomarer Auflösung. Wie andere Mitglieder der Cystatin‑Familie besitzt jede EmCystatin‑B‑Einheit eine charakteristische Form: ein zentrales Helixsegment, unterstützt von mehreren flachen, bandartigen Strängen, die einen Keil bilden, der normalerweise in die aktive Stelle einer Protease passt. Aufgrund seiner Sequenz und des fehlenden offensichtlichen Signalpeptids für die Sekretion gehört EmCystatin‑B zur Untergruppe der „Stefine“, die in der Regel kleine, intrazelluläre Proteine sind und keine stabilisierenden Disulfidbrücken enthalten. Überraschenderweise zeigte die Struktur, dass obwohl jede EmCystatin‑B‑Einheit die erwartete Faltung aufweist, die Art und Weise, wie sich diese Einheiten miteinander verbinden, ungewöhnlich und im Vergleich zum menschlichen Gegenstück Cystatin B artspezifisch ist.
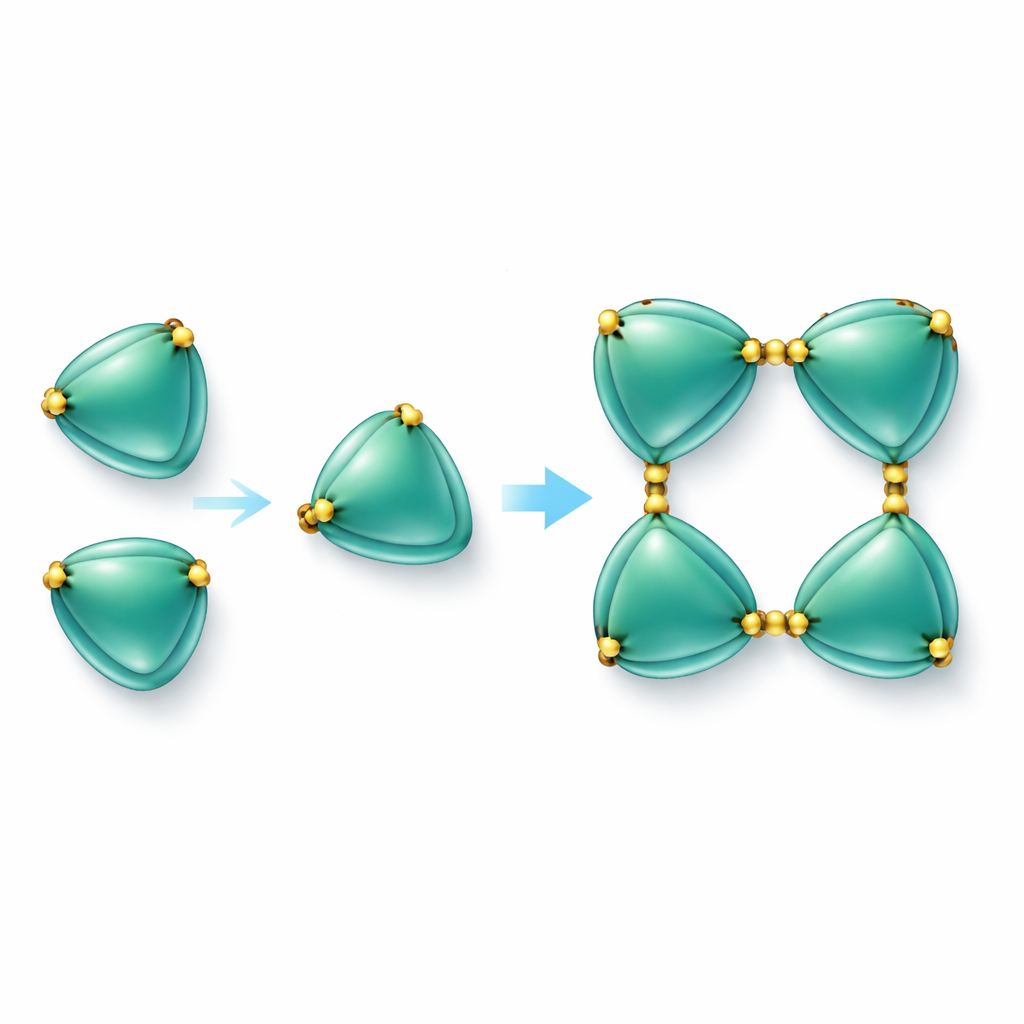
Protein‑Ketten mit Schwefelverbindungen bauen
Der auffälligste Befund war, dass EmCystatin‑B‑Moleküle nicht einfach als Einzeleinheiten frei herumschwimmen. Stattdessen können sie schrittweise zu Dimeren (Paaren) und dann zu Tetrameren (Vierergruppen) zusammenschließen. Zwei verschiedene Mechanismen tragen zur Bildung der initialen Dimere bei. In einem Fall schwingt ein Abschnitt eines Moleküls über und vervollständigt die Struktur seines Nachbarn — ein Phänomen, das als Domänen‑Tausch bekannt ist. Im anderen Fall werden Molekülpaare durch Disulfidbrücken verbunden — starke chemische Bindungen zwischen schwefelhaltigen Aminosäuren (Cystein). Bei EmCystatin‑B verbindet das Cystein an Position 4 eines Moleküls das Cystein an Position 76 eines Partnermoleküls. Vier solcher Querverbindungen stabilisieren dann das Tetramer. Diese Verwendung multipler intermolekularer Disulfidbrücken ist für klassische Stefine, die typischerweise solche Bindungen nicht besitzen, völlig neu. Als die Forschenden diese Schlüssel‑Cysteine gegen eine andere Aminosäure austauschten, konnte das Protein nicht mehr effizient zu höher geordneten Komplexen assemblieren und seine Fähigkeit, Cathepsin B zu hemmen, fiel deutlich ab.
Was das für den Kampf gegen die Infektion bedeutet
Für Nicht‑Spezialisten lautet die Botschaft, dass der Parasit eine speziell verdrahtete Version einer gewöhnlichen Proteinfamilie entwickelt hat und zusätzliche chemische „Nieten“ verwendet, um mehrere Inhibitor‑Einheiten zusammenzuschließen. Diese oligomere Form scheint wichtig zu sein, um ein Wirtsenzym außer Gefecht zu setzen, das sonst helfen würde, die Infektion zu kontrollieren. Durch die Aufklärung der genauen Architektur von EmCystatin‑B und seiner einzigartigen, disulfidverknüpften Assemblierungen erweitert die Studie unser Verständnis dafür, wie Cystatin‑Proteine zwischen Arten feinabgestimmt werden können. Langfristig könnten diese Erkenntnisse die Entwicklung von Wirkstoffen leiten, die entweder den schützenden Effekt von EmCystatin‑B auf den Parasiten blockieren oder dessen immunberuhigende Eigenschaften nachahmen, um entzündliche Erkrankungen zu behandeln.
Zitation: Hong, W., Cheng, Z., Xu, Z. et al. Crystal structure of Echinococcus multilocularis cystatin B reveals a novel feature in classical stefins. Sci Rep 16, 5114 (2026). https://doi.org/10.1038/s41598-026-35060-0
Schlüsselwörter: alveoläre Echinokokkose, Echinococcus multilocularis, Cystatin B, Proteinstruktur, Immunmodulation