Clear Sky Science · de
Störung der NLRP3-Inflammasombildung durch ligand‑induzierte Umgestaltung von Pyrin‑Domänen‑Schnittstellen
Warum die Beruhigung außer Kontrolle geratener Entzündung wichtig ist
Viele chronische Erkrankungen – von Arthritis und Gicht bis zu Herzkrankheiten und Neurodegeneration – werden durch ein überaktives zelluläres Alarmsystem angetrieben. Ein zentraler Bestandteil dieses Alarms, das NLRP3‑Inflammasom, hilft zwar bei der Bekämpfung von Infektionen, kann aber auch schädliche Entzündungen antreiben, wenn es fehlgesteuert wird. Diese Studie beschreibt ein neues Kleinmolekül namens E9, das einen frühen Schritt der NLRP3‑Aktivierung angreift und damit einen neuen Ansatz für die Entwicklung von Medikamenten bietet, die schädliche Entzündung dämpfen, ohne das Immunsystem vollständig auszuschalten.
Ein zellulärer Feuermelder mit Schattenseiten
Wenn unser Körper Gefahr wahrnimmt, bauen Immunzellen das NLRP3‑Inflammasom zusammen — einen großen Proteinkomplex, der wie ein molekularer Feuermelder funktioniert. Sobald er gebildet ist, schaltet diese Struktur ein Enzym namens Caspase‑1 ein, das seinerseits potente entzündungsfördernde Botenstoffe wie die Zytokine IL‑1β und IL‑18 aktiviert. Diese Signale sind wichtig, um Infektionen zu bekämpfen und beschädigtes Gewebe zu beseitigen. Bleibt das Inflammasom jedoch zu lange aktiv oder wird es zur falschen Zeit ausgelöst, trägt es zu chronischen Entzündungszuständen in Gelenken, Blutgefäßen, Gehirn und anderen Organen bei. Deshalb suchen Forscher weltweit nach präzisen Wegen, NLRP3 zu kontrollieren, ohne die Immunabwehr breit zu unterdrücken.
Über die üblichen Wirkziele hinausblicken
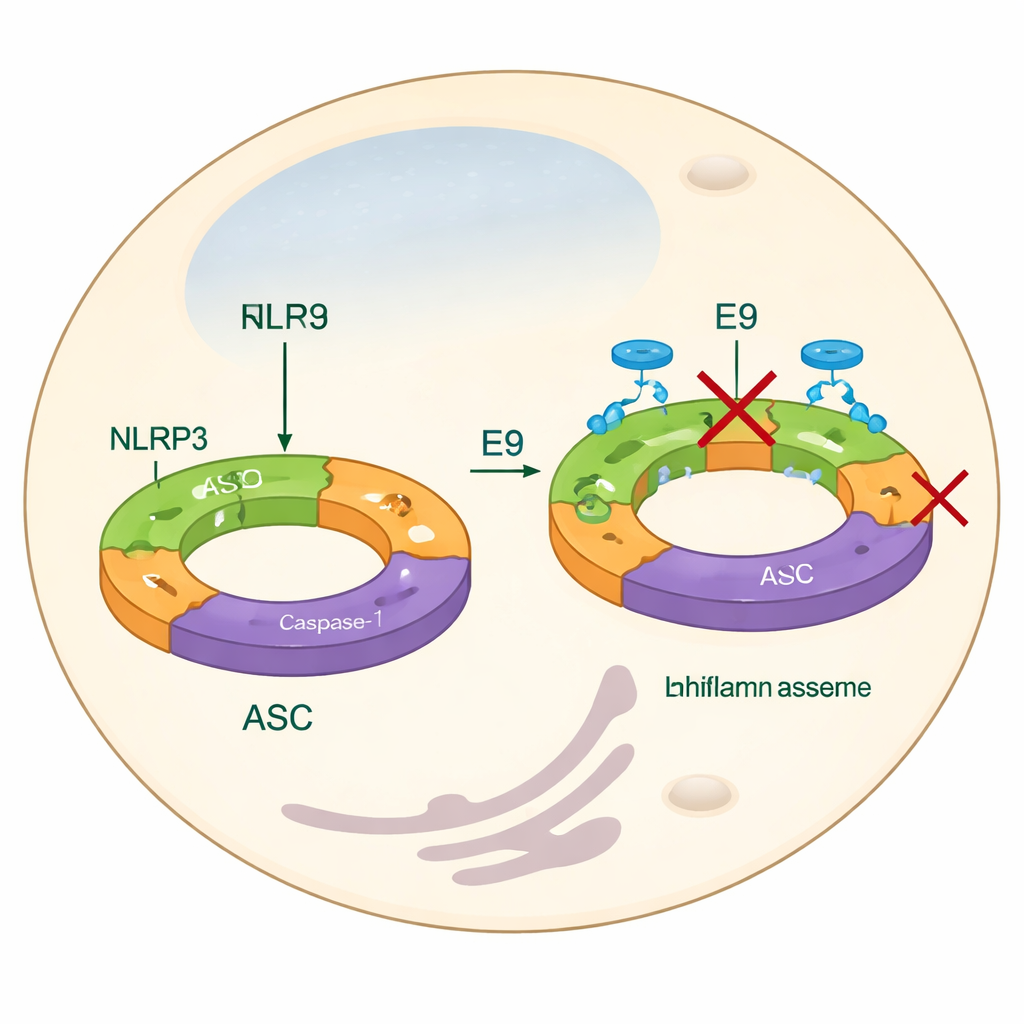
Die meisten aktuellen Strategien zur Eindämmung von NLRP3 zielen darauf ab, seine Endprodukte wie IL‑1β zu blockieren oder eine zentrale, motorähnliche Domäne zu stören, die Energiebausteine wie ATP verwendet. Diese Ansätze können wirken, greifen jedoch die allerkleinsten Assemblierungsschritte nicht an und berücksichtigen nicht vollständig, wie sich NLRP3‑Proteine zusammenschließen, um eine funktionsfähige Maschine zu bilden. In dieser Arbeit richten die Autoren ihren Fokus stattdessen auf die Pyrin‑Domäne, einen Teil von NLRP3, der einzelnen Einheiten hilft, sich zu langen Filamenten zusammenzufügen. Diese Filamente rekrutieren dann ein weiteres Adaptorprotein, ASC, das zu hellen „Specks“ in Zellen verklumpt — ein sichtbares Kennzeichen der Inflammasomaktivierung. Indem sie Chemikalien finden, die verhindern, dass Pyrin‑Domänen richtig ineinandergreifen, wollen die Forscher das Entstehen des Inflammasoms bereits im Ansatz verhindern.
Ein Molekül finden, das die Kette unterbricht
Die Forschenden durchsuchten eine Bibliothek von 1500 neu synthetisierten Kleinmolekülen mithilfe eines raffinierten lichtbasierten Tests. Sie verbanden gespaltene Teile eines Luciferase‑Enzyms mit der NLRP3‑Pyrin‑Domäne; wenn zwei Pyrin‑Domänen zusammenkamen, setzten sich die Enzymfragmente wieder zusammen und erzeugten Licht. Verbindungen, die Pyrin–Pyrin‑Kontakte blockierten, führten zu einem Abfall des Lichts. Aus diesem Screening identifizierten sie vier vielversprechende Kandidaten, von denen einer — E9 — durch starke und konsistente Hemmung hervorstach. Nachfolgende Messungen mittels Mikroskaliger Thermophoresis zeigten, dass E9 eng an die Pyrin‑Domäne bei sehr niedrigen (submikromolaren) Konzentrationen bindet, was bestätigt, dass seine Wirkung kein zufälliger Artefakt, sondern das Ergebnis einer spezifischen Interaktion ist.
Die Wirkung in lebenden Zellen beobachten
Um zu prüfen, ob E9 auch in einem lebenden System wirkt, verwendete das Team humane immunähnliche Zellen, die so verändert wurden, dass sie eine fluoreszierende Version von ASC herstellen. Werden diese Zellen mit bakteriellen Komponenten und einem zweiten Stimulus aktiviert, schaltet NLRP3 ein und ASC‑Proteine clustern zu hellen Specks, die unter dem Mikroskop gezählt werden können. In Gegenwart von E9 ging die Zahl dieser Specks deutlich zurück, vergleichbar mit oder besser als bei einigen bekannten NLRP3‑Blockern. Dies zeigt, dass das Stören von Pyrin‑Domänen‑Kontakten ausreicht, um die Bildung des Inflammasoms und die frühen Schritte des entzündlichen Zelltods zumindest unter Laborbedingungen zu verringern.
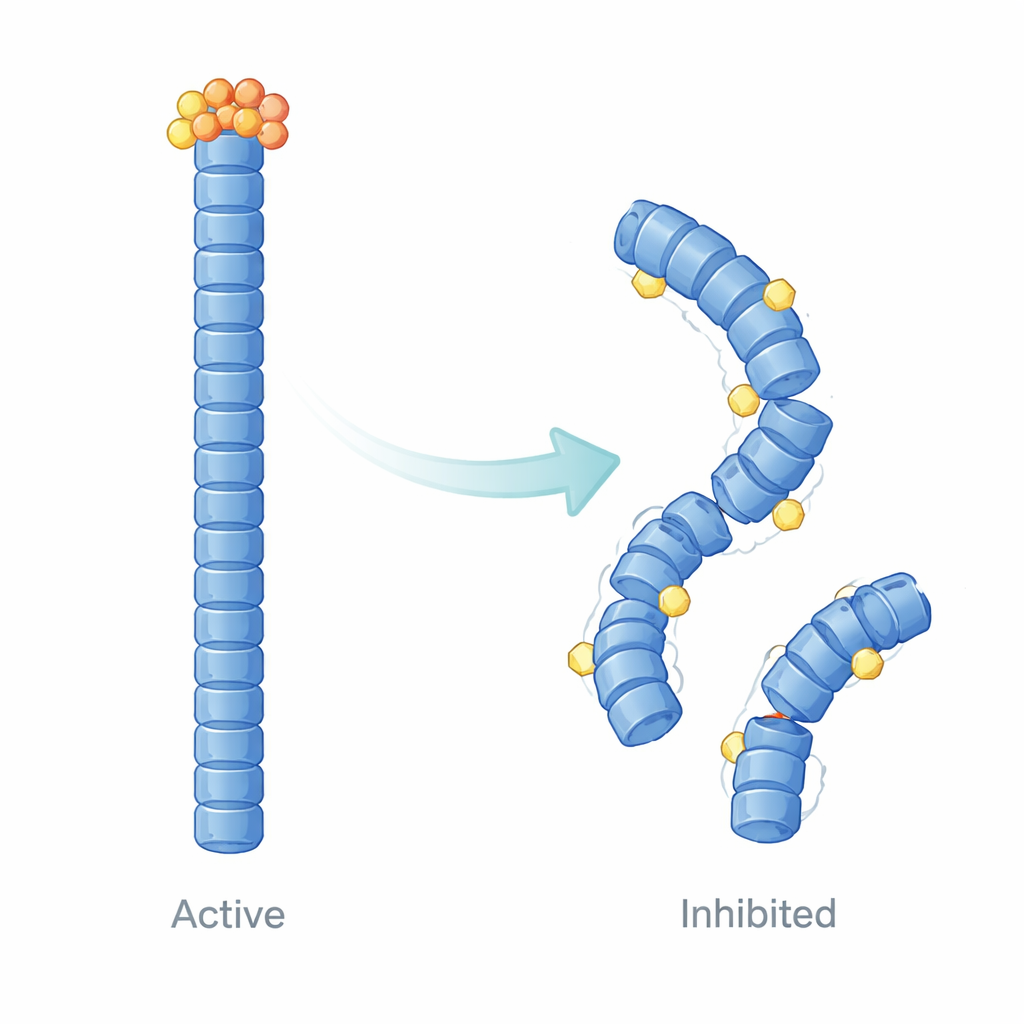
Wie E9 das Gerüst des Inflammasoms umgestaltet
Über reine Bindungsmessungen hinaus nutzten die Autoren computergestützte Strukturmodellierung und Molekulardynamik‑Simulationen, um zu visualisieren, wie E9 das Verhalten von NLRP3‑Filamenten im Lauf der Zeit verändert. Ihre Berechnungen legen nahe, dass E9 an spezifischen Kontaktflächen bindet, an denen Pyrin‑Domänen aneinandergrenzen, und das Filament subtil lockert und umgestaltet. Anstatt einer gleichmäßig stabilen, kooperativen Struktur wird das Filament ungleichmäßig: Bereiche in der Nähe des gebundenen E9 werden flexibler und verlieren ihre präzise Ausrichtung, während andere Teile dynamisch isolierter werden. Diese Verschiebungen dämpfen die großskaligen Bewegungen und die enge Kommunikation, die für eine effiziente Rekrutierung von ASC nötig sind, und liefern eine physikalische Erklärung für die verringerte Speckbildung, die in Zellen beobachtet wurde.
Was das für künftige Therapien bedeuten könnte
Insgesamt positionieren die Ergebnisse E9 als Prototyp für eine neue Klasse von Inflammasom‑gerichteten Wirkstoffen, die dadurch wirken, dass sie die Schnittstellen zwischen NLRP3‑Bausteinen stören, statt dessen Energieverbrauch oder Endprodukte zu blockieren. Zwar beschränkt sich die aktuelle Arbeit auf Reagenzglas‑Assays, Computersimulationen und kultivierte Zellen — und es sind weitere Studien in Tieren und Menschen nötig —, doch zeigt sie, dass sorgfältig gestaltete Kleinmoleküle das Gerüst des Inflammasoms selbst umgestalten können. Für Patientinnen und Patienten mit durch außer Kontrolle geratene Entzündungen verursachten Krankheiten könnten derartige schnittstellen‑fokussierte Wirkstoffe eines Tages präzisere Kontrolle bieten, indem sie schädliche Immunaktivierung dämpfen und gleichzeitig wichtige Abwehrmechanismen weitgehend erhalten.
Zitation: Khosravifard, S., Hosseinkhani, S., Bakhtiary, N. et al. Disruption of NLRP3 inflammasome assembly via ligand-induced remodeling of pyrin domain interfaces. Sci Rep 16, 4951 (2026). https://doi.org/10.1038/s41598-026-35050-2
Schlüsselwörter: NLRP3-Inflammasom, Pyrin‑Domäne, kleinmolekularer Inhibitor, angeborene Immunität, Pyroptose