Clear Sky Science · de
CD13-Aktivierung baut Phosphoinositid-(PI-)Signalgebungskomplexe zusammen, um das Aktin-Zytoskelett zu regulieren
Zellen, die ihre Nachbarn erreichen, um zu helfen
Wenn Gewebe verletzt sind oder unter Stress stehen, müssen Zellen schnell miteinander kommunizieren, um zu entscheiden, ob sie reparieren, sich bewegen oder sogar absterben. Diese Studie zeigt, wie ein wenig bekanntes Oberflächenprotein namens CD13 Zellen dabei hilft, lange, dünne Brücken zu bauen, die räumlich entfernte Zellen physisch verbinden. Über diese Brücken können Zellen Signale wie Calciumwellen teilen und so möglicherweise Überleben und Reparatur im geschädigten Gewebe koordinieren.
Lebende Zellbrücken unter Stress
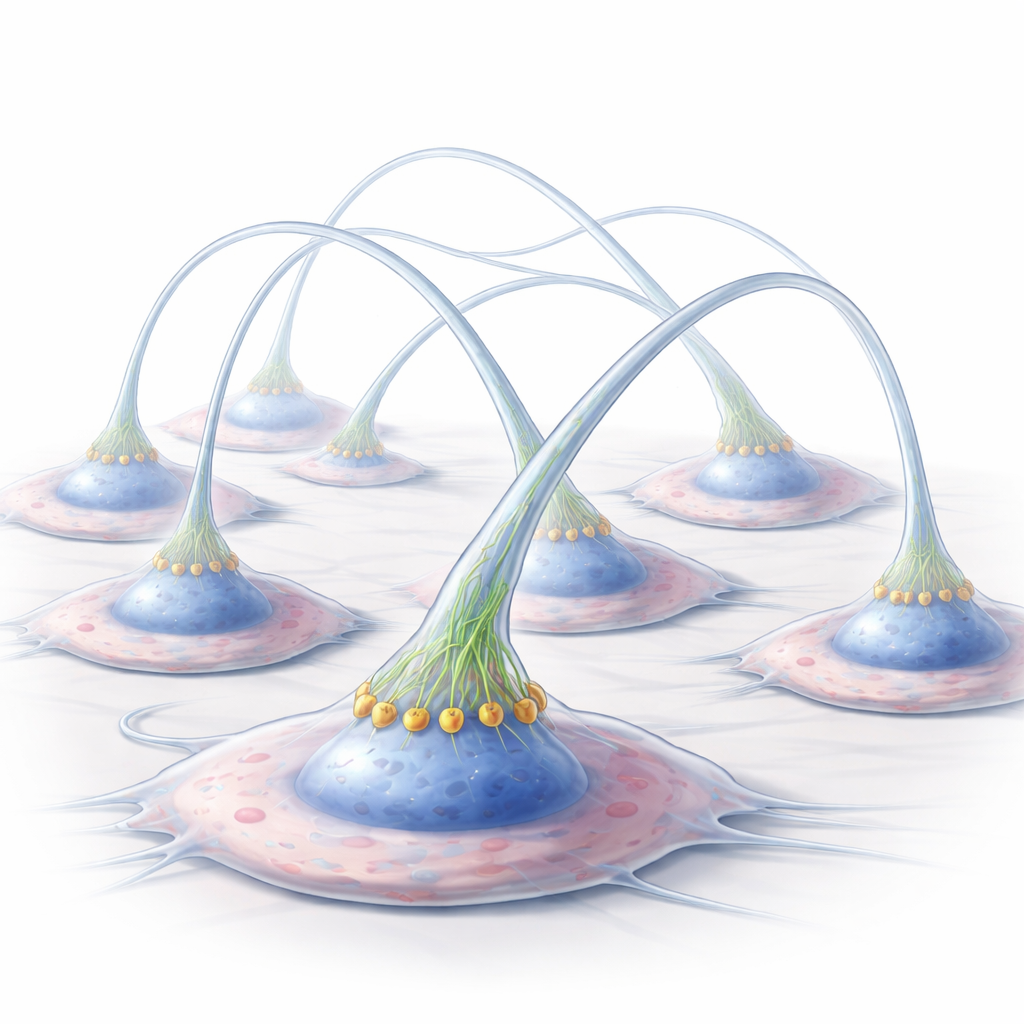
Die Forscher arbeiteten mit menschlichen Zellen aus dem Kaposi‑Sarkom, einem Tumortyp, dessen Zellen unter harten Bedingungen wie Nährstoffmangel oder hohem Zuckergehalt leicht Fortsätze bilden. Unter Stress bildeten normale Zellen viele lange, erhöhte Membranfortsätze, die reich an Aktin waren — dem Strukturprotein, das Zellen ihre Form gibt. Diese Fortsätze ragten über die Oberfläche hinaus und überspannten überraschend große Entfernungen, um nicht berührende Zellen zu verbinden. Als die Wissenschaftler CD13 genetisch entfernten, produzierten die Zellen deutlich weniger und kürzere Fortsätze, die dicht an der Oberfläche blieben. Das zeigte, dass CD13 für den Aufbau dieser auffälligen Zell‑zu‑Zell‑Brücken erforderlich ist.
Aktivierung eines zellulären Bauleiters
CD13 sitzt in der äußeren Zellmembran, hat aber einen winzigen Schwanz im Zellinneren. Das Team verwendete einen speziellen Antikörper, der CD13 zusammenklumpt und „einschaltet“, wodurch eine starke Aktivierung nachgeahmt wird. Diese Behandlung verstärkte die Bildung von Fortsätzen in normalen Zellen deutlich, hatte aber keinen Effekt, wenn CD13 fehlte oder ein nicht‑aktivierender Antikörper eingesetzt wurde. Das Blockieren der Enzymaktivität von CD13 hatte ebenfalls keinen Einfluss, was bedeutet, dass seine Rolle hier als Signalzentrum und nicht als Proteinschneider zu sehen ist. Als die Forscher ein kurzes Peptid einschleusten, das Wechselwirkungen an CD13s innerem Schwanz blockiert, nahm die Fortsatzbildung ab, obwohl CD13 weiterhin an der Oberfläche vorhanden war. Zusammengenommen zeigen diese Ergebnisse, dass CD13 wie ein Bauleiter funktioniert: Bei Aktivierung rekrutiert es die richtige Gruppe von Proteinen an die Membran, um die Zelloberfläche nach außen zu drücken.
Von Lipiden und Proteinen zu wachsenden Fortsätzen
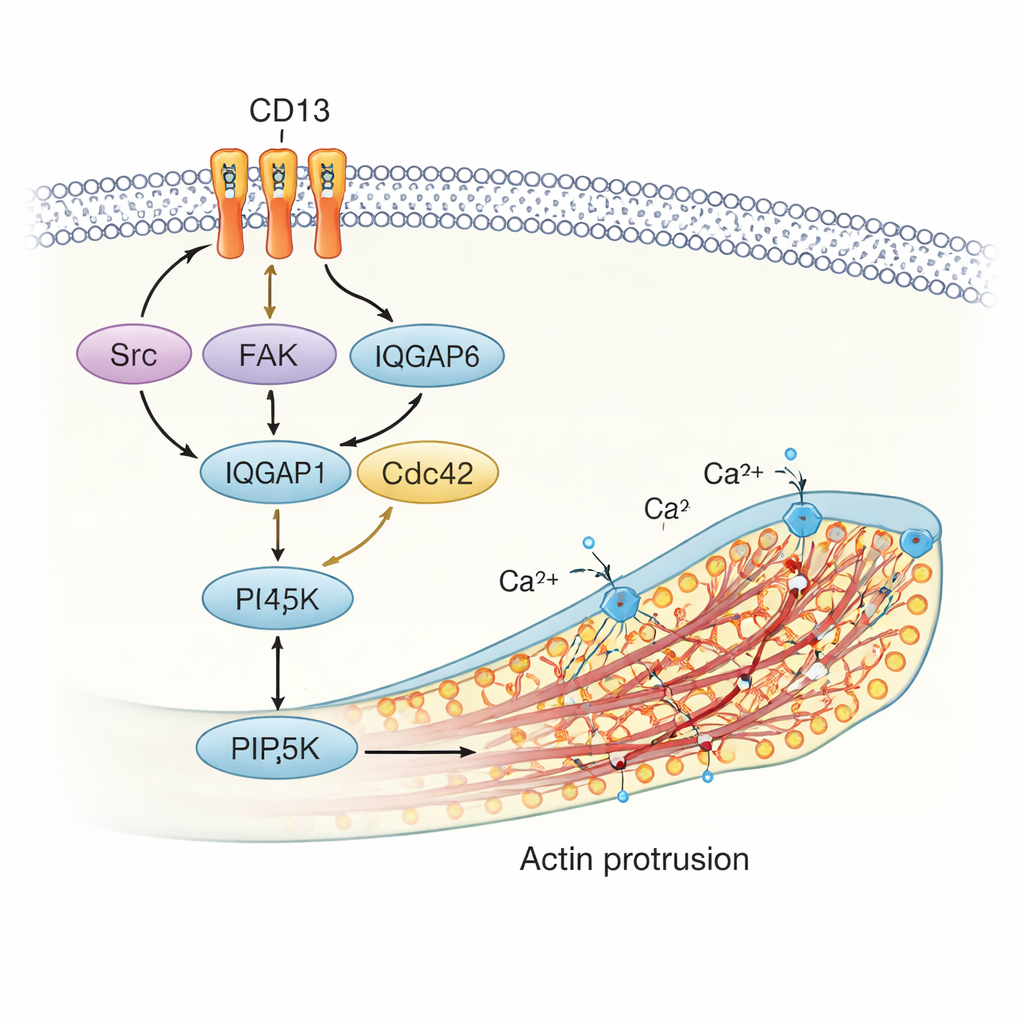
Im Zellinneren bringt CD13 mehrere Schlüsselakteure der Signalgebung zusammen, darunter die Kinasen Src und FAK, das Scaffold IQGAP1 und die kleine GTPase ARF6. Diese Moleküle regulieren sowohl das Aktin‑Skelett als auch die Zusammensetzung der Membran. Die Studie zeigt, dass CD13 bei Aktivierung diesen Proteinkomplex an bestimmte Stellen rekrutiert, wo er ein weiteres Enzym, PIP5K, aktiviert. PIP5K erzeugt ein Signallipid namens PI(4,5)P2 direkt in der Membran. PI(4,5)P2 ist ein starker Organisator: Es bindet an Aktin‑regulierende Proteine und fördert die Aktinpolymerisation, die mechanisch Membranfortsätze antreibt. Die Autoren fanden, dass PI(4,5)P2, CD13 und Aktin sich an der Basis und entlang dieser Strukturen anreichern, was einen eng abgestimmten Protein‑Lipid‑Mechanismus offenbart, der die Membran nach außen schiebt.
‘Handyleitungen’ der Zelle für Calcium‑Signale
Diese CD13‑abhängigen Fortsätze sind nicht nur eindrucksvoll anzusehen; sie verhalten sich wie private Telefonleitungen zwischen Zellen. Mit einem Farbstoff, der Calciumwerte anzeigt, stimulierte das Team mechanisch eine Zelle und beobachtete eine Calciumwelle in ihren Nachbarn. In normalen Zellen mit zahlreichen Fortsätzen verbreitete sich das Calciumsignal schnell und effizient zu vielen verbundenen Zellen, selbst wenn externes Calcium blockiert war. Im Gegensatz dazu zeigten Zellen ohne CD13 — und damit ohne ausgeprägte Fortsätze — eine deutlich schlechtere Signalweiterleitung. Die Fortsätze trugen das Gap‑Junction‑Protein Connexin 43, das Kanäle zwischen Zellen bildet, und stützt damit die Idee, dass es sich um „geschlossen endende tunneling nanotubes“ handelt, die auf die Übertragung interner Signale spezialisiert sind und nicht auf den freien Austausch großer Mengen an Material.
Warum das für Heilung und Krankheit wichtig ist
Indem diese Arbeit zeigt, wie CD13 ein lokales Signalzentrum organisiert, um das Aktin‑Skelett und Membranlipide umzugestalten, identifiziert sie CD13 als zentralen Schalter, der Zellen hilft, unter Stress Kommunikationsbrücken zu bauen. Für Laien lautet die Schlussfolgerung, dass Zellen nicht nur chemische Nachrichten in ihre Umgebung „rufen“; sie können physische Kabel verlegen, um gezielte Signale an entfernte Partner zu senden. Da CD13 in geschädigten und entzündeten Geweben häufig vorkommt und aktiviert wird, könnte das Verständnis dieses Weges neue Strategien zur Förderung der Gewebereparatur, zur Begrenzung schädlicher Entzündungen oder zum Unterbrechen maligner Zellkommunikation bei Krebs informieren.
Zitation: Meredith, E., Aguilera, B., Sharma, R. et al. CD13 activation assembles phosphoinositide (PI) signaling complexes to regulate the actin cytoskeleton. Sci Rep 16, 5191 (2026). https://doi.org/10.1038/s41598-026-35022-6
Schlüsselwörter: zellkommunikation, Aktin-Zytoskelett, Membranfortsätze, CD13-Protein, Phosphoinositid-Signalgebung