Clear Sky Science · de
Molekulares Profiling von Primär- gegenüber asynchronen, gepaarten metastasierten klarzelligen Nierenkarzinomen zeigt Heterogenität im tumorimmunen Mikromilieu
Warum diese Nierenkrebsstudie wichtig ist
Nierenkrebs breitet sich häufig in andere Körperregionen aus, und moderne Immuntherapien wirken nicht bei allen Patientinnen und Patienten oder bei jedem Tumor gleich gut. Diese Studie schaut in das Innere des klarzelligen Nierenzellkarzinoms — der häufigsten Nierenkrebsform — und untersucht, wie das Immunsystem im ursprünglichen Nierentumor im Vergleich zu späteren Metastasen unterschiedlich reagiert. Das Verständnis dieser Unterschiede könnte erklären, warum einige Tumoren besser auf Therapien ansprechen als andere, und zu präziseren, personalisierten Behandlungsstrategien führen.
Blick in Primärtumoren und Metastasen
Die Forschenden konzentrierten sich auf 19 Patientinnen und Patienten, bei denen der Nierentumor (der Primärtumor) entfernt worden war und später Metastasen in Lunge, Knochen, Leber, Nebennieren, Lymphknoten oder Weichgewebe auftraten. Von diesen Patienten sammelten sie 42 Tumorproben: 19 Primärtumoren und 23 unbehandelte Metastasen. Sie isolierten RNA — ein Molekül, das abbildet, welche Gene gerade aktiv sind — aus dünnen Schnitten des konservierten Gewebes und nutzten Hochdurchsatzsequenzierung, um die Genaktivität von Tausenden Genen in jeder Probe zu erfassen. 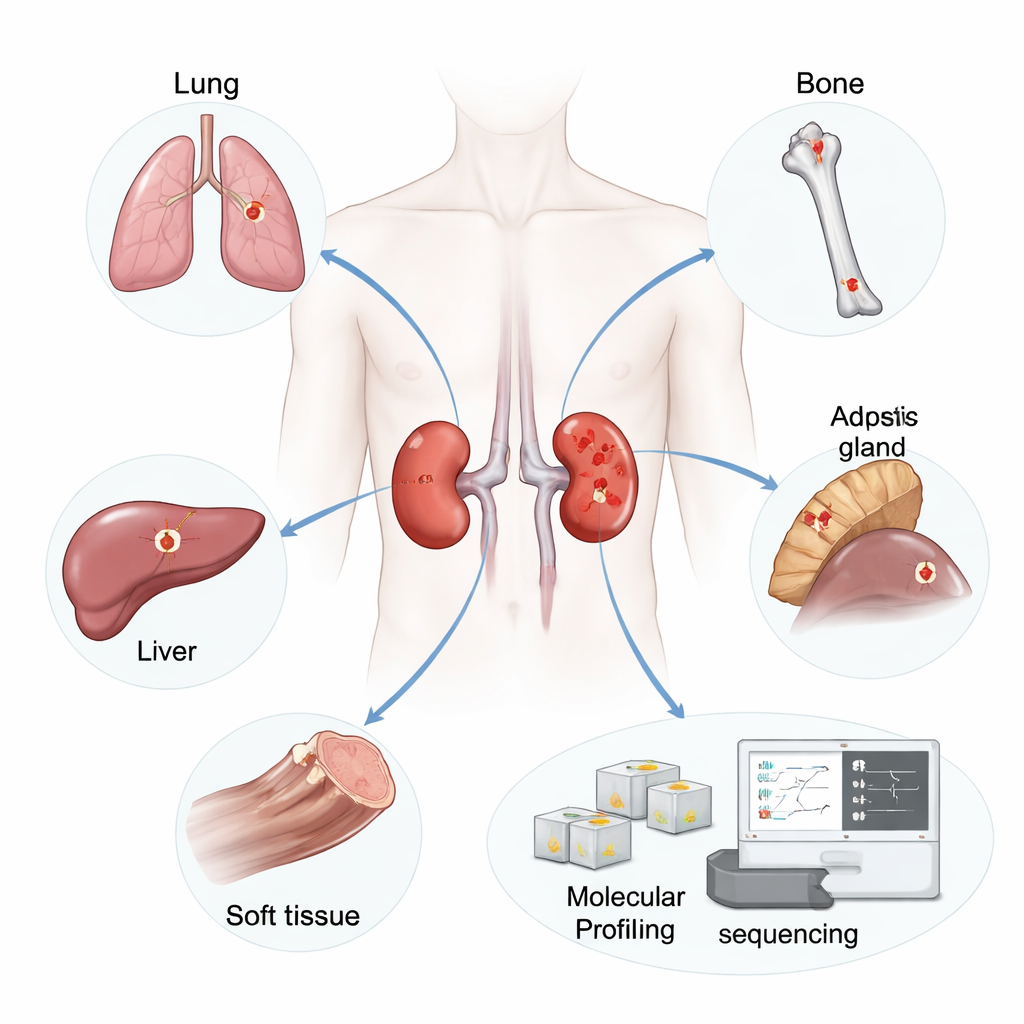
Primär- und Metastastumoren sind molekular unterschiedlich
Bei der Analyse der Genaktivitätsmuster stellten die Forschenden fest, dass Primärnierentumoren dazu neigten, untereinander zu clustern und einander ähnlicher zu sein als ihren eigenen Metastasen. Anders gesagt: Die Metastase einer Patientin oder eines Patienten konnte sich stärker vom ursprünglichen Tumor derselben Person unterscheiden als von der Metastase einer anderen Person. Tausende Gene zeigten in Metastasen entweder eine höhere oder niedrigere Aktivität im Vergleich zu Primärtumoren. Metastatische Tumoren wiesen stärkere Signale aus Genprogrammen auf, die mit schneller Zellteilung und aggressivem Verhalten verknüpft sind, einschließlich Signalwegen, die Zellzyklus-Checks und Proteinproduktion betreffen. Im Gegensatz dazu waren Primärtumoren stärker angereichert für Stress- und Signalwege wie Hypoxie (niedriger Sauerstoff) und Entzündungssignale, was auf unterschiedliche biologische Belastungen in der Niere gegenüber entfernten Organen hindeutet.
Die Immunlandschaft verändert sich, wenn Krebs sich ausbreitet
Über die rohe Genaktivität hinaus schätzten die Forschenden mithilfe einer computergestützten Methode, die Bulk-RNA-Daten dekonvolviert, welche Immunzelltypen in jedem Tumor vorhanden waren. Sie entdeckten einen auffälligen Unterschied: Primärtumoren in der Niere enthielten einen signifikant höheren Anteil an regulatorischen T-Zellen (Tregs), einer Immunzellenart, die Immunreaktionen dämpft und Tumoren vor Angriffen schützen kann. In Primärtumoren fanden sich außerdem mehr ruhende dendritische Zellen, Monozyten, natürliche Killerzellen und CD8+-T-Zellen. Im Gegensatz dazu waren Metastasen reicher an sogenannten M2-Makrophagen — Immunzellen, die oft mit Wundheilung und einer tumorfördernden statt tumorzellenden Umgebung assoziiert werden — sowie an mehr Plasmazellen und aktivierten dendritischen Zellen. 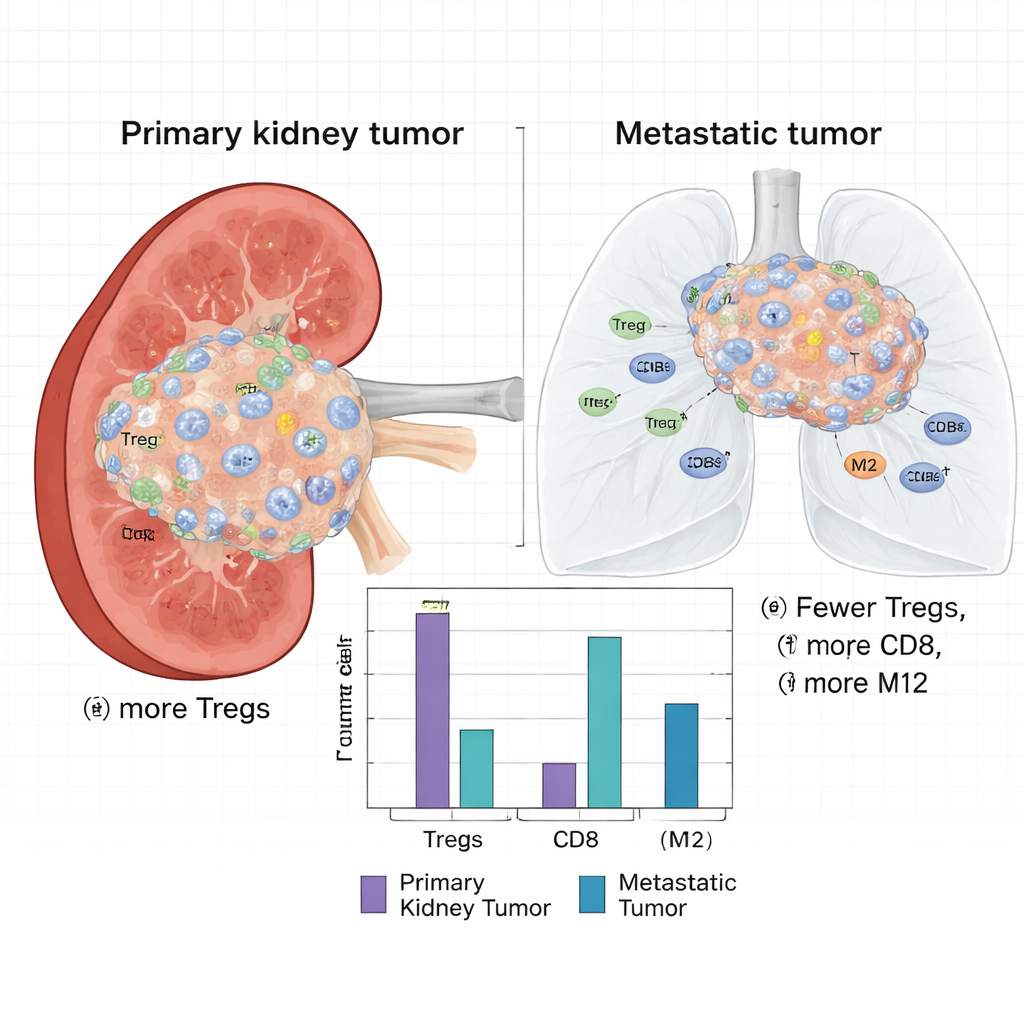
Lungen- und Knochenmetastasen erzählen unterschiedliche Immun-Geschichten
Bei genauer Betrachtung spezifischer Metastasierungsorte traten wichtige Nuancen zutage. Lungenmetastasen zeigten eine erhöhte Aktivität von Genmengen, die mit der Kontrolle der Zellteilung (G2M-Checkpoint) und E2F-Transkriptionsfaktoren verknüpft sind, sowie eine hohe Expression von Hornerin, einem Protein, das mit Gefäßneubildung in Tumoren in Verbindung gebracht wird. Die dazugehörigen Primärtumoren in der Niere waren stärker angereichert für hypoxiebezogene Genprogramme und enthielten wiederum mehr Tregs. Knochenmetastasen hoben sich dagegen durch eine stärkere Aktivierung der epithelial‑to‑mesenchymalen Transition hervor, eines Prozesses, der Krebszellen beweglicher und invasiver macht. Diese Knochenläsionen enthielten zudem höhere Anteile an M2-Makrophagen, während die Primärtumoren, die zu ihnen führten, eine erhöhte Expression von HHLA2 zeigten, einem kürzlich erkannten Immun-Checkpoint-Molekül. Zusammen unterstreichen diese Befunde, dass die immunologischen und molekularen Umgebungen von Metastasen sich nicht nur von Primärtumoren unterscheiden, sondern auch zwischen verschiedenen Metastasierungsorten variieren.
Gleichgewicht der Immunzellen und Patientenergebnisse
Um zu verstehen, was diese Immunmuster für Patientinnen und Patienten bedeuten, nutzte das Team drei große öffentliche Datensätze zum klarzelligen Nierenkrebs. Sie wandten denselben computergestützten Ansatz an, um Treg- und CD8+-T-Zell‑Niveaus zu schätzen, und verknüpften diese mit Überlebensdaten. In den Kohorten zeigte sich: Personen, deren Tumoren eine Kombination aus niedrigen CD8+-T-Zellen (den wichtigsten tumorabtötenden T‑Zellen) und hohen Treg-Werten aufwiesen, hatten tendenziell schlechtere progressionsfreie oder krankheitsspezifische Überlebensraten — selbst nach Berücksichtigung von Alter, Tumorgrad und Stadium. Während das Gesamtstadium weiterhin einen starken Einfluss auf das Überleben hatte, erwies sich das Verhältnis zwischen unterdrückenden Tregs und angreifenden CD8+-Zellen als zusätzlicher Risikomarker.
Was das für die zukünftige Nierenkrebsbehandlung bedeutet
Einfach ausgedrückt zeigt diese Studie, dass der ursprüngliche Nierentumor und seine Metastasen in unterschiedlichen immunologischen „Nachbarschaften“ leben. Der Primärtumor scheint besonders gut darin zu sein, friedensstiftende Zellen anzuziehen, die das Immunsystem beruhigen — das könnte teilweise erklären, warum Tumoren in der Niere oft schlechter auf Immuntherapie ansprechen als metastatische Ablagerungen. Metastasen entwickeln hingegen eigene lokale Unterstützungsnetzwerke, die organspezifisch variieren. Diese Erkenntnisse legen nahe, dass Ärztinnen und Ärzte in manchen Fällen sowohl den Nierentumor als auch Metastasen untersuchen sollten, um die Erkrankung vollständig zu erfassen, und dass Kombinationstherapien, die Immun-Checkpoint-Inhibitoren mit Strategien zur gezielten Beeinflussung von Tregs oder M2‑Makrophagen verbinden, das Behandlungsergebnis für Menschen mit metastasiertem klarzelligem Nierenzellkarzinom verbessern könnten.
Zitation: Cotta, B., Nallandhighal, S., Monda, S. et al. Molecular profiling of primary versus paired asynchronous metastatic clear cell renal cell carcinoma reveals heterogeneity in tumor immune microenvironment. Sci Rep 16, 5473 (2026). https://doi.org/10.1038/s41598-026-35021-7
Schlüsselwörter: Nierenkrebs, Tumormikroumgebung, Immuntherapie, Metastase, regulatorische T-Zellen