Clear Sky Science · de
Transkriptomische Charakterisierung der abweichenden alternativen Spleißung in Skelettmuskeln von Sarkopenie-Patienten
Warum alternde Muskeln ihre Kraft verlieren
Sarkopenie — der schrittweise Verlust von Muskelmasse und -kraft mit dem Alter — ist eine der Hauptursachen dafür, dass ältere Menschen im Alltag Schwierigkeiten haben, von Treppensteigen bis zum Tragen von Einkaufstüten. Diese Studie blickt in alternde Muskeln auf der Ebene der RNA, der Botschaften, die Zellen sagen, welche Proteine sie herstellen sollen. Die Autorinnen und Autoren zeigen, dass bei Sarkopenie viele dieser RNA-Botschaften auf abnorme Weise geschnitten und zusammengesetzt werden, was möglicherweise die Energieproduktion in den Muskeln stört und auf neue Behandlungsziele hinweist.
Muskelschwund und das genetische „Schnittsystem“ des Körpers
Unsere Gene sind in der DNA geschrieben, doch Zellen arbeiten mit RNA-Kopien dieser Gene. Bevor eine RNA-Botschaft genutzt wird, wird sie normalerweise getrimmt und gespleißt — ähnlich wie das Schneiden eines Films — sodass ein Gen mehrere Proteinvarianten erzeugen kann. Dieser Prozess, alternative Spleißung genannt, ist besonders aktiv im Muskel, der fein abgestimmte Proteine zum Kontrahieren, Reparieren und Anpassen an Bewegung benötigt. Wenn das Spleißen schiefläuft, können falsche Proteinvarianten entstehen oder wichtige verloren gehen, was zu Erkrankungen wie Muskeldystrophien und einigen Hirnerkrankungen beiträgt. Die Autorinnen und Autoren vermuteten, dass eine ähnliche verdeckte Schicht von RNA-Fehlschnitten die Sarkopenie antreiben könnte.
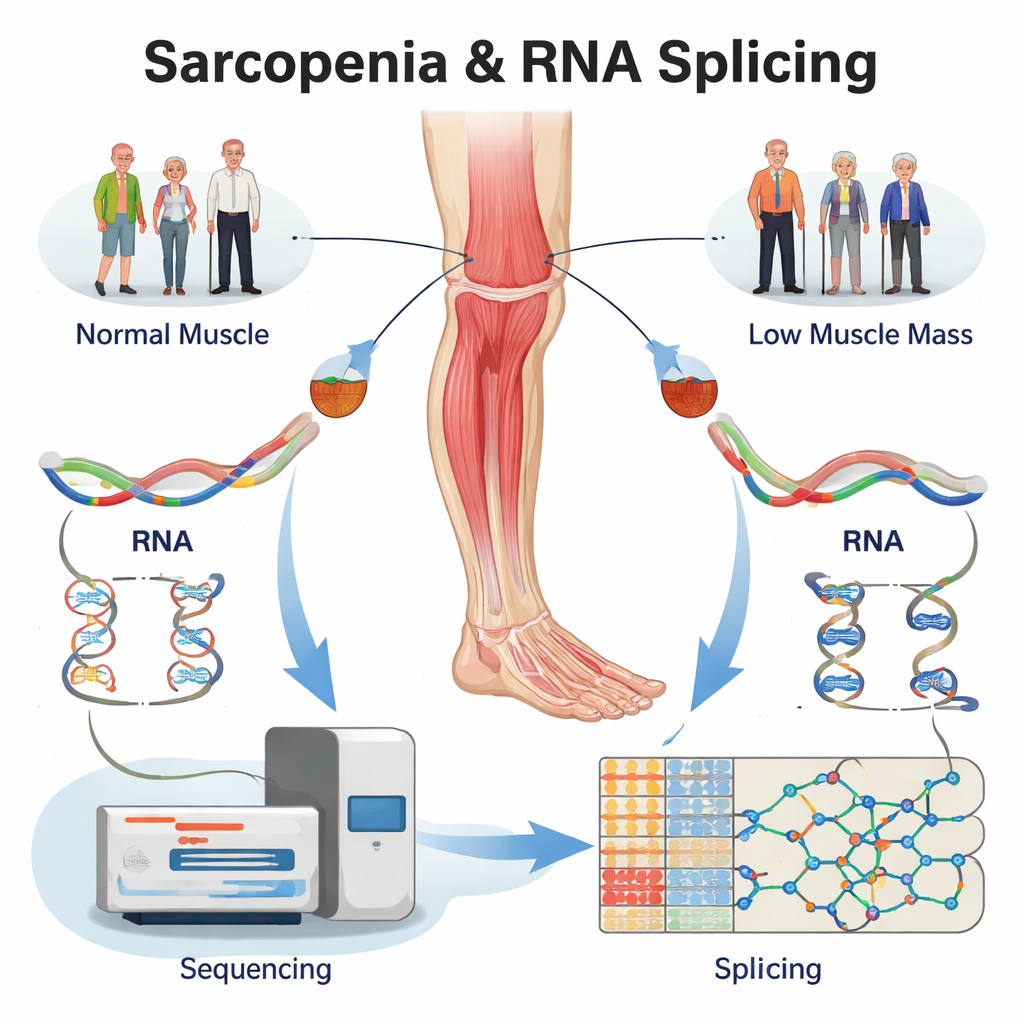
Existierende Daten neu lesen, um versteckte RNA-Fehler zu finden
Anstatt neue Probanden zu rekrutieren, analysierte das Team ein bestehendes großes RNA-Sequenzierungs-Datenset aus menschlichen Oberschenkelmuskelbiopsien erneut. Die Proben stammten aus vier Gruppen: ältere Erwachsene mit ausgeprägter Sarkopenie, Personen mit lediglich geringer Muskelmasse, Personen mit lediglich geringer Muskelkraft und altersentsprechende gesunde Kontrollen. Mit spezialisierter Software bestätigten sie zunächst, dass Hunderte von Genen in den erkrankten Muskeln hoch- oder herunterreguliert waren. Wichtiger noch: Sie untersuchten dann, wie die RNA jedes Gens gespleißt wurde, und katalogisierten mehr als 5.000 Spleißveränderungen in den drei Problemgruppen im Vergleich zu gesundem Muskel. Diese Veränderungen konzentrierten sich auf einige grundlegende Typen — etwa das Überspringen eines Exons oder die Wahl alternativer Schnittstellen — Muster, von denen bekannt ist, dass sie die Proteinstruktur stark verändern können.
Energiefabriken und zelluläre „Tankanzeige“-Signalwege sind gestört
Die Spleißveränderungen traten in Genen auf, die im Herzen der Muskelbiologie liegen. Viele betroffene Gene kodieren Teile der Mitochondrien, der winzigen Energiefabriken, die die Muskelkontraktion antreiben. In sarkopenischem Muskel zeigten 16 Gene, die an der oxidativen Phosphorylierung beteiligt sind — dem Prozess, der Nährstoffe in nutzbare Energie umwandelt — veränderte Spleißmuster, insbesondere Komponenten der mitochondrialen Komplexe, die den Elektronentransport und Protonentransport steuern. Weitere Veränderungen fanden sich in Genen, die NAD⁺ herstellen oder nutzen, einem zentralen Molekül für zelluläre Energie und Reparatur. Statt einfach nur in ihrer Menge verändert zu sein, produzierten wichtige Enzyme wie CD38, PARP2 und mehrere Sirtuine unterschiedliche RNA-Varianten, was darauf hindeutet, dass das Gleichgewicht zwischen NAD⁺-Produktion und -Verbrauch auf der Spleißebene verzerrt ist. Die betroffenen Gene gruppierten sich außerdem in bekannten Muskel-Signalwegen, darunter AMPK- und FoxO-Wege, die wie zelluläre Tankanzeigen und Stressantwortsysteme funktionieren.
Gemeinsame Muster über verschiedene Stadien — und über Arten hinweg
Bemerkenswerterweise zeigten viele derselben Gene Spleißveränderungen nicht nur bei Menschen mit ausgeprägter Sarkopenie, sondern auch bei denen mit nur geringer Muskelmasse oder nur geringer Kraft. Das deutet darauf hin, dass abnormes Spleißen früh beginnt und die verschiedenen klinischen Erscheinungsformen der Erkrankung übergreift. Um zu prüfen, ob sich diese Veränderungen in einem Tiermodell nachbilden lassen, lösten die Forschenden Muskelschwund bei Mäusen mit dem Steroid Dexamethason aus, einer gängigen Methode, um einige Merkmale der Sarkopenie zu imitieren. Die Mäuse entwickelten eine schwächere Griffkraft und schlechtere Leistungen bei Lauf- und Balancetests. Als das Team die Mausmuskel-RNA sequenzierte, fanden sie erneut Hunderte von Genen mit verändertem Spleißen. Etwa ein Fünftel davon überschneidete sich mit den menschlichen Sarkopenie-Genen, und viele waren an der Steuerung von Transkription, Chromatinstruktur und dem Spleißen selbst beteiligt — übergeordnete Schalter, die die gesamte Proteinausgabe einer Zelle umgestalten können.
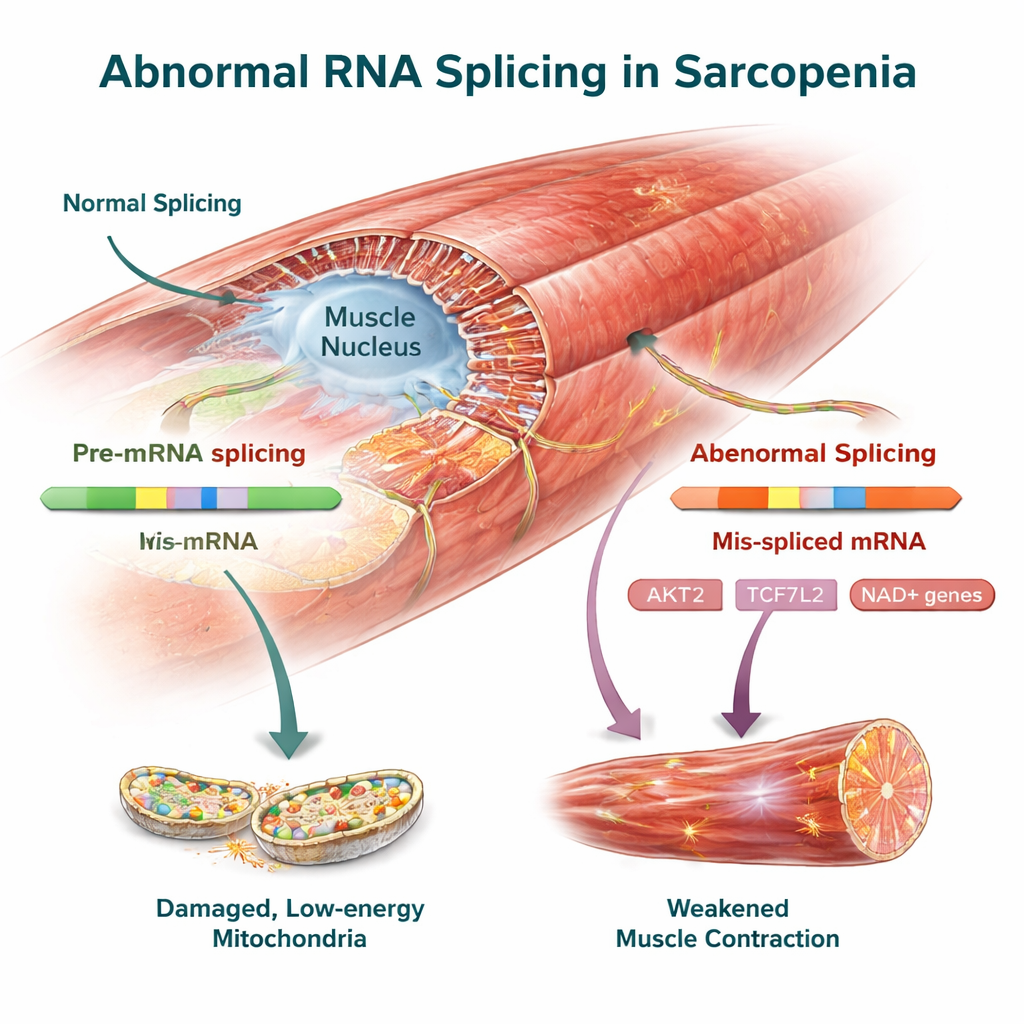
Wichtige Muskelschnittstellengene als potenzielle Therapieziele
Unter den artsübergreifenden Veränderungen fanden sich mehrere Gene, die bereits mit Muskelgesundheit in Verbindung stehen. AKT2, ein zentraler Regulator von Wachstum und Proteinsynthese im Muskel, zeigte in Mensch und Maus charakteristische Spleißverschiebungen, die seine Fähigkeit, Muskelmasse zu erhalten, abschwächen könnten. TCF7L2, Teil des Wnt-Signalwegs, sowie FMNL2 und USP40, die beim Organisieren des intrazellulären Gerüsts und der Proteinqualitätskontrolle helfen, trugen ebenfalls veränderte RNA-Varianten. Das Team bestätigte diese Spleißveränderungen experimentell in Mausmuskelgewebe, was die Auffassung stärkt, dass es sich um echte Merkmale der Erkrankung handelt und nicht um Artefakte der Datenanalyse.
Was das für die Verhinderung von Gebrechlichkeit bedeutet
Für Nichtfachleute lautet die Botschaft: Sarkopenie ist nicht nur ein „Abnutzen“ der Muskeln oder ein einfaches Ein- oder Ausschalten von Genen. Sie umfasst auch eine weitverbreitete Fehlschnittigkeit von RNA-Botschaften, die steuern, wie Muskelzellen ihre Maschinerie bauen und erhalten, insbesondere die Systeme, die Energie erzeugen und Stress wahrnehmen. Da Spleißen prinzipiell mit präzise entworfenen RNA-basierten Arzneien korrigiert werden kann, bieten die hier entdeckten konservierten Spleißfehler — insbesondere in Genen wie AKT2 und TCF7L2 — neue Ansatzpunkte für Therapien, die älteren Muskeln helfen könnten, länger stärker zu bleiben.
Zitation: Li, Y., Guo, X., Li, S. et al. Transcriptomic characterization of the aberrant alternative splicing in skeletal muscles of sarcopenia patients. Sci Rep 16, 5334 (2026). https://doi.org/10.1038/s41598-026-35002-w
Schlüsselwörter: Sarkopenie, Muskelseneszenz, RNA-Spleißen, Mitochondrien, AKT2