Clear Sky Science · de
Phänomenologisches Modell zur Stabilisierung von Transthyretin
Warum das für Patientinnen und Patienten und ihre Familien wichtig ist
Die Transthyretin-Amyloidose ist eine ernste Erkrankung, bei der ein normales Blutprotein, Transthyretin (TTR), zerfällt und seine Fragmente sich im Herzen und in Nerven zu schädlichen Ablagerungen verklumpen können. Neue Medikamente wie Tafamidis und Acoramidis sollen dieses Protein in seiner stabilen, vierteiligen Form erhalten, und sie haben bereits die Ergebnisse für viele Menschen verbessert. Dennoch sehen Ärztinnen und Ärzte bei behandelten Patientinnen und Patienten einen rätselhaften Effekt: Die TTR-Spiegel im Blut steigen um mehr als 30 %, und es ist nicht offensichtlich, warum. Dieses Papier verwendet ein stark vereinfachtes, mathematikbasiertes Modell, um zu untersuchen, was im Körper passieren könnte und was das für die Wirkungsweise dieser Medikamente bedeutet. 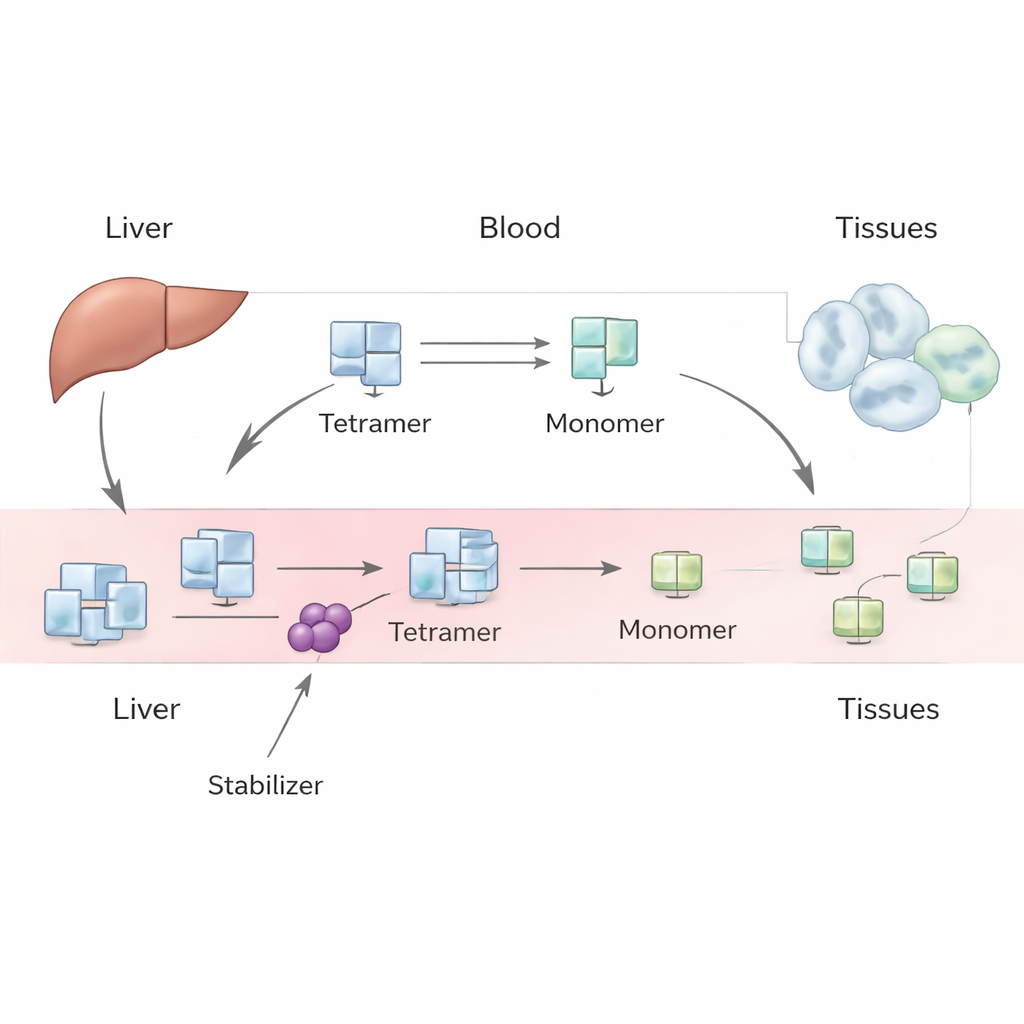
Ein Protein, das helfen oder schaden kann
TTR wird hauptsächlich in der Leber gebildet und zirkuliert normalerweise als stabiles Bündel aus vier identischen Untereinheiten, ein sogenanntes Tetramer. Es transportiert Schilddrüsenhormon und Vitamin A. Unter bestimmten Bedingungen, etwa altersbedingt oder durch vererbte Genvarianten, kann dieses Tetramer in einzelne Untereinheiten, Monomere, zerfallen. Diese Monomere können falsch gefaltet sein und sich als Amyloidfibrillen zusammenlagern, die Gewebe schädigen und zur Transthyretin-Amyloidose des Herzens (Kardiomyopathie) oder der Nerven (Neuropathie) führen. Medikamente wie Tafamidis und Acoramidis binden an das Tetramer und erschweren dessen Zerfall, wodurch das Fortschreiten der Krankheit verlangsamt werden soll. Wenn Patientinnen und Patienten jedoch mit diesen Medikamenten beginnen, steigen die gemessenen TTR-Werte im Blut verlässlich an, und dieser Anstieg ist größer, als einfache Laborexperimente erwarten lassen würden.
Ein einfaches Bild eines komplexen Systems erstellen
Die Autorinnen und Autoren gehen dieses Rätsel mit einem phänomenologischen Modell an – einem Modell, das sich auf das beobachtbare Gesamtverhalten konzentriert statt auf jedes mikroskopische Detail. In ihrem Rahmen produziert die Leber Tetramere von TTR mit einer gleichmäßigen Rate, die dann in den Blutkreislauf gelangen. Einmal in der Zirkulation, können Tetramere in Monomere dissoziieren und sich wieder zusammensetzen, und sowohl Tetramere als auch Monomere können durch Aufnahme in Gewebe und Abbau aus dem Blut entfernt werden. Durch Aufstellen eines Paares von Massenbilanzen für Tetramere und Monomere untersucht das Team verschiedene Szenarien: eines, in dem Monomere überwiegend wieder zu Tetrameren zusammenfinden, eines, in dem sie schnell entfernt werden, und einen Zwischenfall, in dem beide Prozesse eine Rolle spielen. Sie verwenden historische menschliche Tracer-Studien und moderne Labordaten, um Schlüsselgrößen abzuschätzen, etwa wie schnell Tetramere geklärt werden, wie rasch sie zerfallen und wie stark Medikamente diesen Zerfall verlangsamen.
Warum allein die Stabilisierung des Tetramers nicht ausreicht
Mit diesen Abschätzungen fragen die Forschenden gezielt: Wenn ein Medikament Tetramere vollständig daran hindern könnte, auseinanderzufallen, um wie viel würden dann die TTR-Werte im Blut steigen? In allen plausiblen Regimen ist die Antwort moderat – im Bereich von höchstens etwa 15 % für typische Parameterwerte und oft deutlich weniger, abhängig davon, wie mit Monomeren umgegangen wird. Das reicht bei weitem nicht an den beobachteten Anstieg von über 30 % bei behandelten Patientinnen und Patienten heran. Die Diskrepanz bleibt selbst dann bestehen, wenn man großzügige Unsicherheiten in den bekannten Parametern zulässt. Das Modell legt daher nahe, dass das bloße Verlangsamen des Tetramer-Zerfalls allein den klinischen Effekt nicht erklären kann. Weitere Prozesse, die steuern, wie schnell TTR hergestellt, von Zellen aufgenommen oder abgebaut wird, müssen ebenfalls verändert sein, wenn Stabilisator-Medikamente vorhanden sind. 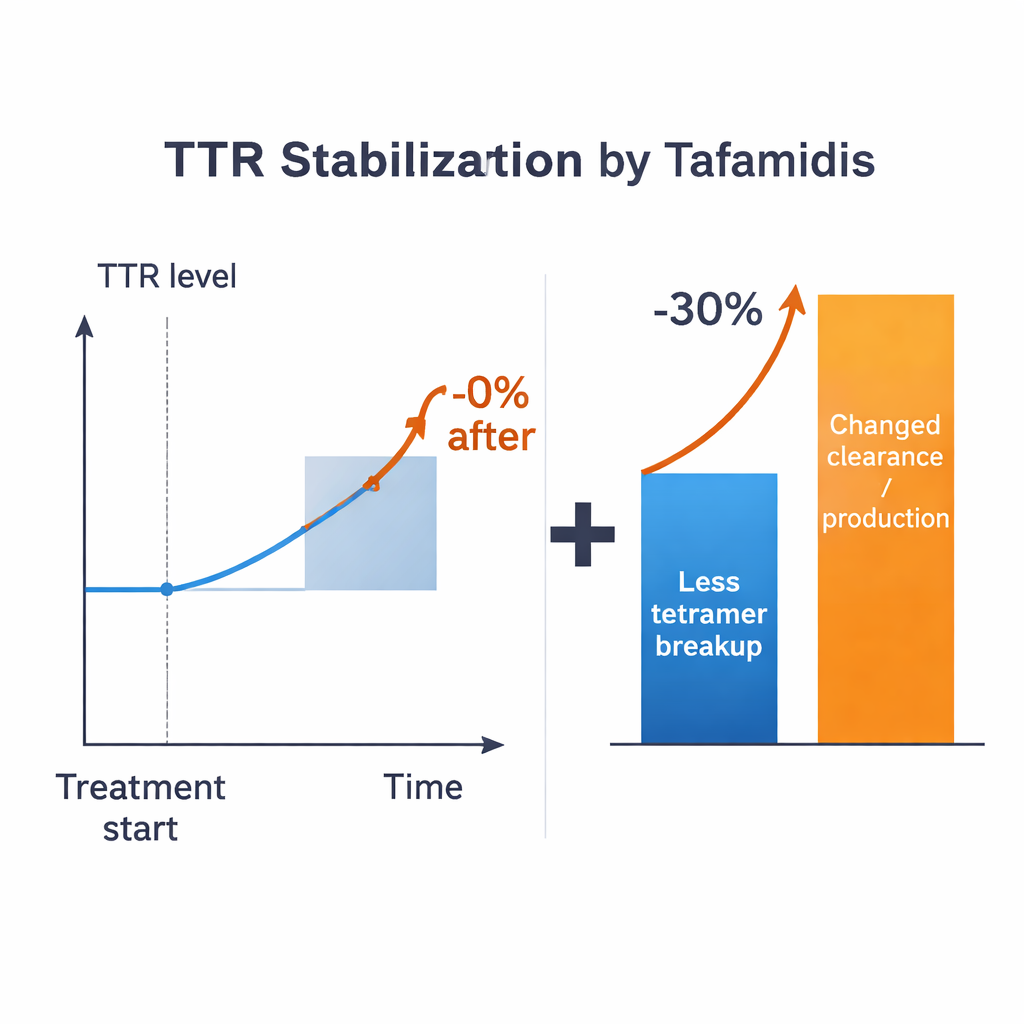
Hinweise aus Arzneispiegeln und cleveren Experimenten
Um die Arzneimittel-Exposition mit dem Verhalten von TTR zu verknüpfen, kombinieren die Autorinnen und Autoren ein einfaches pharmakokinetisches Modell von Tafamidis (wie sich das Medikament über die Zeit im Körper verteilt) mit spezialisierten „Subunit-Exchange“-Assays. In diesen Experimenten werden markierte und unmarkierte TTR-Tetramere in humanes Plasma gemischt, und der allmähliche Austausch von Untereinheiten zeigt, wie oft Tetramere auseinanderfallen. Die Messung dieses Prozesses bei unterschiedlichen Arzneimittelkonzentrationen liefert eine direkte, datengetriebene Verbindung zwischen Tafamidis-Spiegel und effektiver Tetramer-Stabilität, ohne dass man wissen muss, wie viel Medikament an Albumin oder Schilddrüsenhormon gebunden ist. Diese phänomenologische Verbindung fließt in das Modell ein und umgeht sauber viele biochemische Unbekannte. Selbst mit diesem Vorteil begrenzen die Berechnungen jedoch den erwarteten Anstieg von TTR auf ungefähr die Hälfte des klinisch beobachteten Zuwachses, was die Idee stützt, dass Änderungen in Clearance, Internalisierung, Abbau oder sogar Synthese Teil der Erklärung sein müssen.
Was das für die Zukunft bedeutet
Für Nicht-Spezialistinnen und Nicht-Spezialisten lautet die Kernbotschaft, dass diese Stabilisator-Medikamente wahrscheinlich mehr tun, als nur TTR-Tetramere „zusammenzukleben“. Sie beeinflussen wahrscheinlich auch, wie der Körper das Protein produziert, entfernt oder recycelt. Die Autorinnen und Autoren argumentieren, dass einfache, transparente Modelle wie ihres mächtig sind, weil sie solche Lücken in unserem Verständnis offenlegen und auf konkrete Experimente hinweisen – zum Beispiel direkte Messungen, wie schnell Monomere geklärt werden, wie schnell verschiedene TTR-Formen von Zellen aufgenommen werden, oder ob mit Medikamenten gebundene TTR anders gehandhabt wird als ungebundenes Protein. Bessere Antworten auf diese Fragen würden nicht nur die Behandlung der Transthyretin-Amyloidose verfeinern, sondern könnten auch allgemeine Regeln für andere Erkrankungen aufdecken, bei denen normale Proteine zu schädlichen Aggregaten werden.
Zitation: Lisowski, B., Ulaszek, S., Wiśniowska, B. et al. Phenomenological model of transthyretin stabilization. Sci Rep 16, 4904 (2026). https://doi.org/10.1038/s41598-026-35000-y
Schlüsselwörter: Transthyretin-Amyloidose, Protein-Stabilisierung, Tafamidis, pharmakokinetische Modellierung, Amyloid-Erkrankungen