Clear Sky Science · de
Das Ubiquitin‑Proteasom‑System treibt die Progression EBV‑assoziierten Nasopharynxkarzinoms: eine Metaanalyse transkriptomischer Daten
Krebs in einer verborgenen Ecke des Rachens
Das Nasopharynxkarzinom ist ein Tumor, der in einem kleinen, schwer zugänglichen Raum hinter der Nase und oberhalb des hinteren Rachenraums entsteht. Weltweit ist er relativ selten, trifft jedoch viele Menschen in Teilen Südostasiens und Chinas und verläuft dort oft tödlich. Fast alle dieser Tumoren tragen eine persistente Infektion mit dem Epstein‑Barr‑Virus (EBV), demselben Virus, das auch Pfeiffersches Drüsenfieber verursachen kann. Diese Studie stellt eine dringende Frage für Patientinnen, Patienten und Ärztinnen sowie Ärzte: Wie verändert dieses Virus unauffällig Zellen und ihr Umfeld, sodass Krebs wachsen, sich dem Immunsystem entziehen und Therapien widerstehen kann?
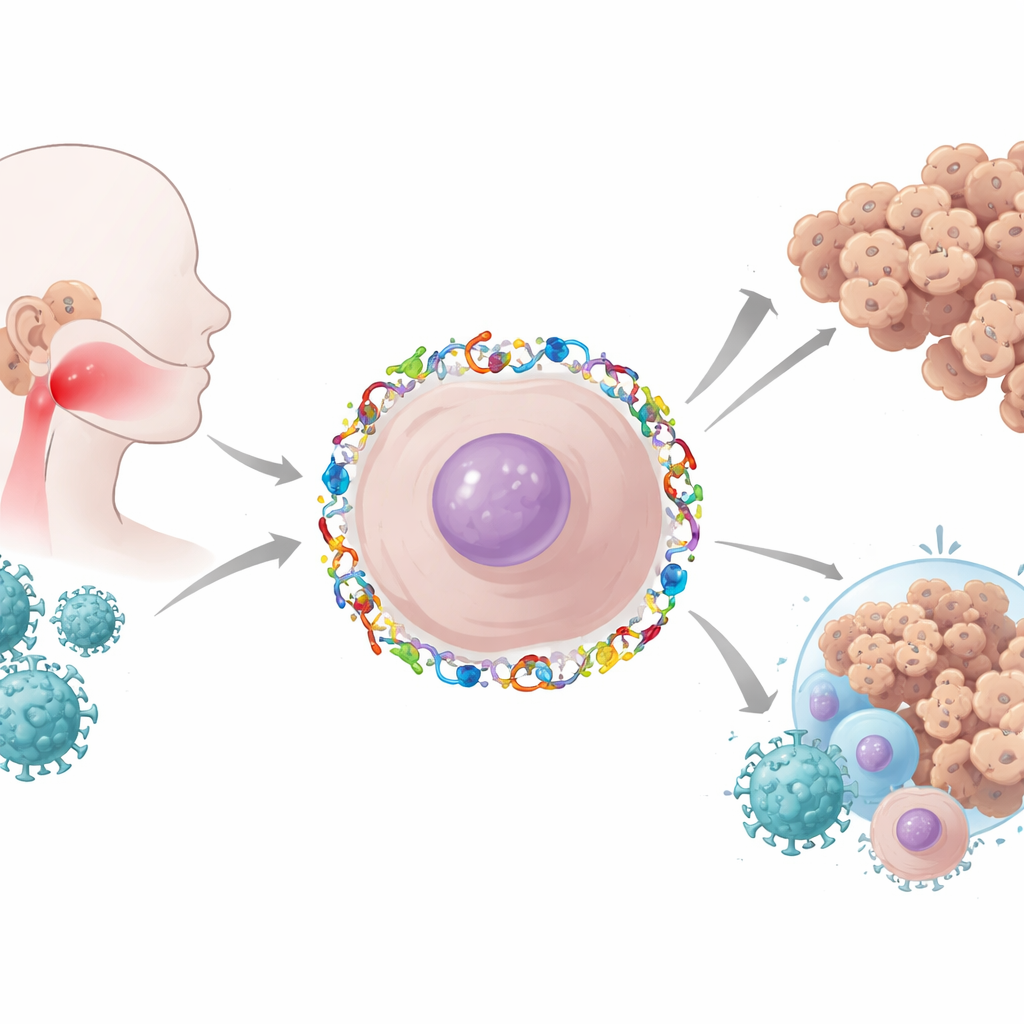
Ein viraler Eindringling und ein überfülltes immunes Schlachtfeld
EBV‑assoziierte nasopharyngeale Tumoren sind dicht bevölkert mit Immunzellen, darunter T‑Zellen, natürliche Killerzellen und Makrophagen. In vielen Krebserkrankungen deutet ein solches Ausmaß an Immunzellinfiltrat auf eine aktive Abwehr hin. Hier sind die Immunzellen jedoch merkwürdigerweise ineffektiv. EBV trägt zu diesem Paradox bei, indem es virale Proteine und kleine RNAs freisetzt, die das umliegende Gewebe in Richtung Unterdrückung statt Angriff lenken. Das Virus sorgt dafür, dass Zellen beruhigende Signale aussenden, „Bremsen“ exprimieren, die T‑Zellen erschöpfen, und verändert, wie Krebszellen virale und tumorassoziierte Fragmente an ihrer Oberfläche präsentieren. Das Ergebnis ist eine lebhafte, aber gedämpfte Immunumgebung, in der der Tumor unbemerkt gedeihen kann.
Die zelluläre Müllentsorgung wird zum Doppelagenten
Die Autoren konzentrieren sich auf die Proteinrecycling‑Maschinerie der Zelle, das sogenannte Ubiquitin‑Proteasom‑System. Unter normalen Bedingungen markiert dieses System abgenutzte oder beschädigte Proteine und führt sie einem molekularen Schredder zu. Es erzeugt außerdem kleine Peptidfragmente, die Immunzellen helfen, infizierte oder entartete Zellen zu erkennen. Durch die Kombination von sechs großen Genexpressionsdatensätzen aus Tumoren und gesundem Gewebe identifizierten die Forschenden Tausende von Genen, die sich beim Nasopharynxkarzinom verändern. Darunter interagieren 85 menschliche Gene physisch mit EBV‑Proteinen, und ein eng vernetzter Cluster widmet sich diesem Proteinrecycling. Viele dieser Wirtsgene werden von EBV‑Proteinen reguliert, die während der lytischen Phase des Virus aktiv sind, wenn es kurzzeitig reaktiviert wird, um sich zu replizieren. Das legt nahe, dass periodische virale Reaktivierung die zelluläre Müllentsorgung so abstimmt, dass sie dem Tumor zugutekommt.
Einzelzellanalysen zeigen zwei Gesichter des Tumors
Um zu beobachten, wo diese Gene aktiv sind, nutzte das Team Einzelzell‑RNA‑Sequenzierung, eine Methode, die die Genaktivität in tausenden einzelner Zellen aus Tumoren erfasst. Sie verglichen EBV‑positive nasopharyngeale Karzinome mit virusnegativen oropharyngealen Karzinomen aus einem angrenzenden Rachenbereich. Krebszellen in nasopharyngealen Tumoren zeigten durchgehend höhere Aktivität der Proteinrecycling‑Gene als ihre Gegenstücke, und auch einige Immunzellen wiesen erhöhte Aktivität auf. Als die Forschenden Tumorzellen anhand dieses Signaturprofils gruppierten, traten zwei Hauptzustände hervor. „UPS‑High“-Zellen wiesen sehr aktive Recycling‑Maschinerie, geringere Zeichen der Zellteilung und stärkere Verknüpfungen zu stammzellähnlichen Eigenschaften und immundämpfenden Signalen auf. „UPS‑Low“-Zellen teilten sich schneller und standen in Verbindung mit klassischen wachstumsfördernden Signalwegen, etwa denen, die durch Fibroblasten‑Wachstumsfaktoren und Wnt‑Proteine vermittelt werden.
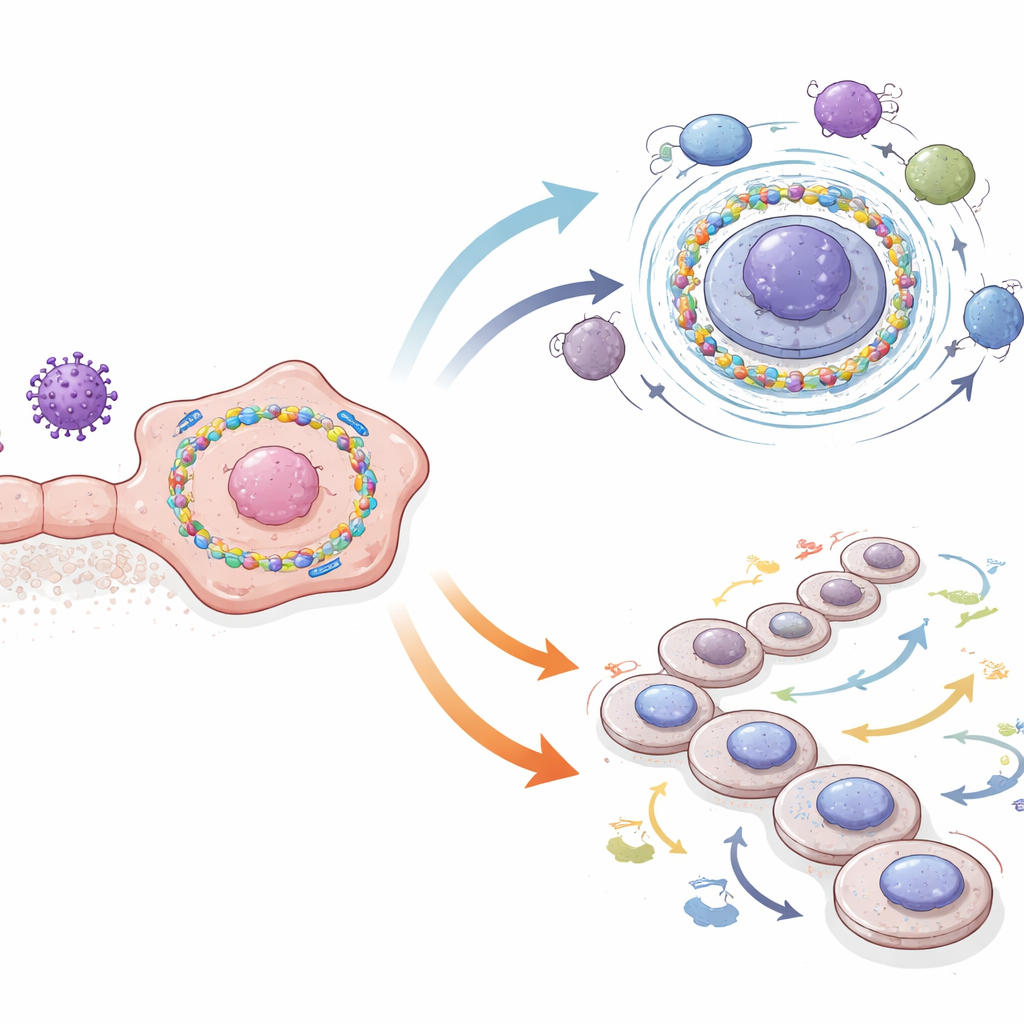
Wie Tumorzellen mit ihrer Nachbarschaft kommunizieren
Das Team setzte anschließend rechnerische Werkzeuge ein, um vorherzusagen, wie diese beiden Tumorzellzustände mit benachbarten Immunzellen kommunizieren. Zellen im UPS‑High‑Zustand schienen Botschaften zu senden, die eher zu Immuntoleranz als zu Angriff ermutigen. Sie zeigten verringerte Aktivität der Signale, die normalerweise interne Proteine Immunwächtern präsentieren, wodurch sie schwerer „sichtbar“ werden. Gleichzeitig aktivierten sie Signalwege, die mit Immunsuppression verknüpft sind, einschließlich Hinweisen von Molekülen wie dem Makrophagenmigrations‑Inhibitor‑Faktor und bestimmten Bauteilen der Basalmembran. Im Gegensatz dazu sendeten und empfingen UPS‑Low‑Zellen mehr Signale, die mit Wachstum und Gewebsumbau zusammenhängen, was zu einem schneller wachsenden, aber weniger versteckten Zellbestand passt.
Was das für Patientinnen, Patienten und zukünftige Therapien bedeutet
Beim Studium von Patientendatensätzen über viele Tumortypen hinweg, darunter Kopf‑Hals‑Tumoren und eine kleinere nasopharyngeale Kohorte, fanden die Forschenden heraus, dass eine höhere Expression dieser 12‑Gen‑Proteinrecycling‑Signatur tendenziell mit schlechterem Überleben korreliert. Sie schlagen vor, dass EBV einige Tumorzellen in einen UPS‑High‑Zustand lenkt, der langsamer wächst, sich aber besser verbirgt und eher stammzellähnliche Eigenschaften aufweist, wodurch solche Zellen Therapien überdauern und Rezidive begründen können. Andere Zellen bleiben UPS‑Low und treiben die rasche Tumorvergrößerung. Obwohl diese Erkenntnisse hauptsächlich aus RNA‑Messungen stammen und noch im Labor bestätigt werden müssen, weisen sie auf die Proteinrecycling‑Maschinerie sowohl als Marker für aggressivere Erkrankungen als auch als vielversprechendes Wirkstoffziel hin. Eine gezielte Modulation dieses Systems — besonders in Kombination mit immunbasierten Therapien — könnte eines Tages helfen, EBV‑getriebene Tumorzellen sichtbar zu machen und die Prognose von Menschen mit Nasopharynxkarzinom zu verbessern.
Zitation: Ratnawati, H., Sanjaya, A., Christiandy, A. et al. The ubiquitin–proteasome system is an important driver of EBV-associated nasopharyngeal carcinoma progression: a meta-analysis of transcriptomic data. Sci Rep 16, 8892 (2026). https://doi.org/10.1038/s41598-025-34808-4
Schlüsselwörter: Nasopharynxkarzinom, Epstein‑Barr‑Virus, Ubiquitin‑Proteasom‑System, tumorales immunes Mikromilieu, Immunflucht