Clear Sky Science · de
Wechselspiel zwischen Autophagie und p38 MAPK während salinomycyn‑induzierter Zellfast in cisplatinresistentem Melanom
Warum diese Forschung wichtig ist
Melanom ist eine der tödlichsten Hautkrebsformen, zum Teil weil Tumoren häufig lernen, Standardchemotherapien wie Cisplatin zu umgehen. Diese Studie untersucht, ob ein ungewöhnliches Antibiotikum namens Salinomycyn diese Resistenz durchbrechen kann, und sie beleuchtet die zellulären Recycling‑ und Stressreaktionssysteme, um zu verstehen, wie das Medikament wirkt. Für alle, die wissen wollen, warum manche Krebsarten nach einer Behandlung zurückkommen — und wie man sie möglicherweise austricksen kann — bietet diese Arbeit Einblicke in die verborgenen Lebens‑oder‑Todes‑Entscheidungen innerhalb von Tumorzellen.
Wenn Krebszellen auf Behandlung nicht mehr hören
Cisplatin ist ein häufig eingesetztes Medikament gegen viele solide Tumoren, aber Melanomzellen passen sich oft an und werden schwerer zu töten. Die Forschenden entwickelten eine murine Melanomzelllinie, die an Cisplatinresistenz gewöhnt war, und testeten darauf Salinomycyn. In Zellkulturen reduzierten steigende Dosen Salinomycyn die Zahl lebensfähiger Melanomzellen stark, lösten klassische Anzeichen programmierter Zelltodwege aus und vernichteten selbst nach kurzer Exposition die Fähigkeit der Zellen, neue Kolonien zu bilden. In Mäusen mit cisplatinresistenten Melanomtumoren führten Injektionen von Salinomycyn zu einer dramatischen Wachstumsverlangsamung, verringerten Tumorvolumen und -gewicht ohne offensichtliche Toxizität. Zusammengenommen deuten diese Ergebnisse darauf hin, dass Salinomycyn Melanomzellen treffen kann, die auf Standardchemotherapie nicht mehr reagieren. 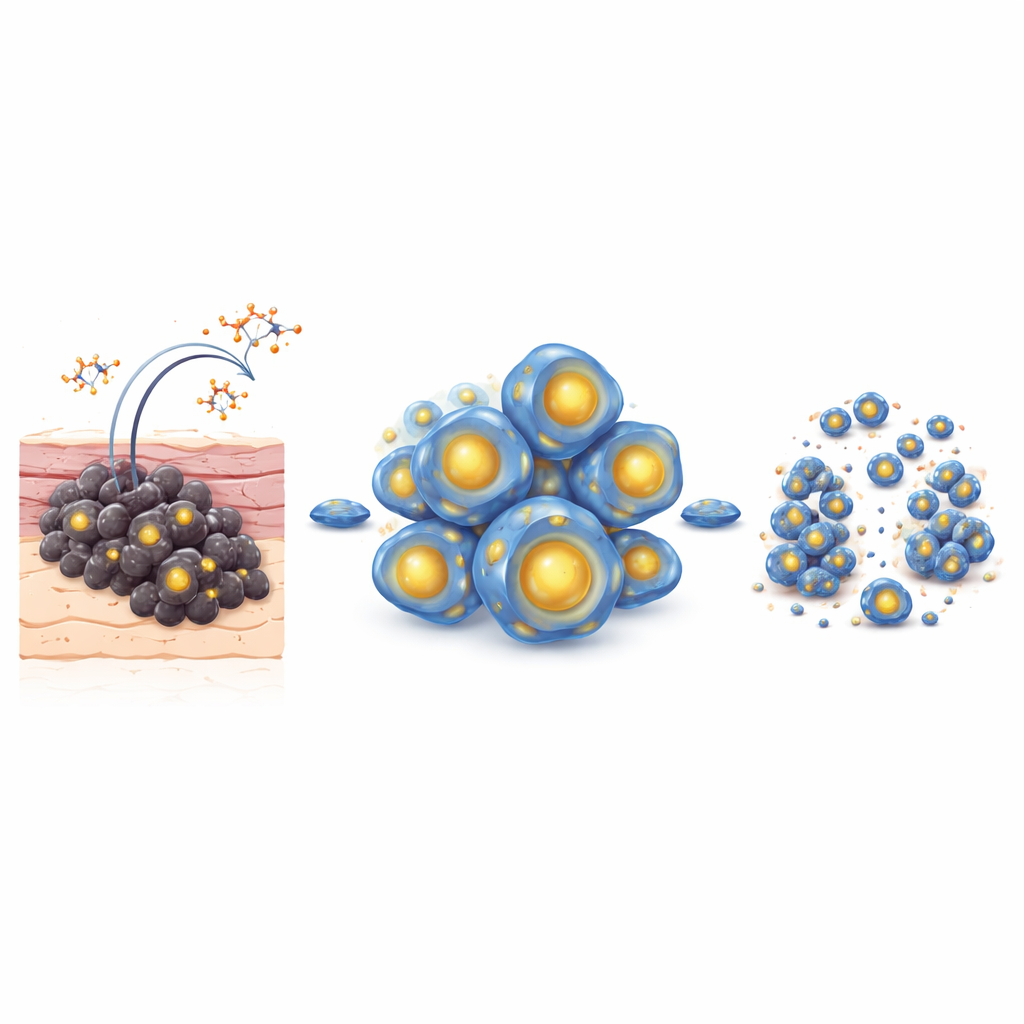
Zellstress, Kalziumwellen und ein unter Druck stehendes Recyclingsystem
Um herauszufinden, was Salinomycyn in der Zelle bewirkt, konzentrierte sich das Team auf das endoplasmatische Retikulum, ein Membrannetzwerk, das beim Falten und Verarbeiten neuer Proteine hilft. Salinomycyn wirkt wie ein Ionen‑Shuttle und stört den Fluss geladener Teilchen über Membranen, was dieses Organell in Fehlfunktion versetzen kann. Die Forschenden beobachteten eine starke Aktivierung von Proteinmarkern, die auftreten, wenn die Proteinfaltmaschinerie der Zelle unter Stress steht. Gleichzeitig detektierten sie eine Kalziumfreisetzung aus dem endoplasmatischen Retikulum in das umliegende Cytosol und in Richtung Mitochondrien, den Kraftwerken der Zelle. Wenn sie die Fähigkeit der Mitochondrien blockierten, dieses Kalzium aufzunehmen, starben die Zellen noch leichter, was darauf hindeutet, dass die Mitochondrien normalerweise als Puffer dienen, um den Zelltod unter Salinomycynstress hinauszuzögern.
Selbstreinigung wird zur tödlichen Verkehrs‑störung
Zellen sind auf einen Prozess angewiesen, der oft als „Selbstverzehr“ beschrieben wird, um schwierige Bedingungen zu überstehen: Sie verpacken beschädigtes Material in kleine Säckchen und schicken es zu sauren Kompartimenten zur Aufspaltung und Wiederverwertung. Salinomycyn verstärkte die frühen Schritte dieses Wegs stark und erhöhte Proteine, die die Bildung dieser Säckchen antreiben. Entscheidend ist jedoch, dass das abschließende Aufräumstadium gestört war. Marker, die eigentlich abgebaut werden sollten, häuften sich stattdessen an, und die mikroskopische Bildgebung zeigte große vakuolenartige Strukturen, die nicht ordnungsgemäß mit Lysosomen, den Verdauungseinheiten der Zelle, verschmolzen. Weitere Tests deuteten darauf hin, dass Lysosomenmembranen undicht wurden und bestimmte Verdauungsenzyme am falschen Ort aktiviert wurden. Das Ergebnis ist eine Art zellulärer Stau: Recycling‑Pakete bilden sich weiter, werden aber nicht effizient abgebaut, was einen normalerweise schützenden Prozess in einen Auslöser für Zelltod verwandeln kann.
Ein Stress‑Signalschalter, der gegen den Tumor gedreht werden kann
Ein weiterer Puzzlestein ist eine Familie von Stresssensoren, bekannt als MAP‑Kinasen. Salinomycyn aktivierte drei Zweige dieses Systems, doch ein Ast stach besonders hervor: p38. Wenn die Forschenden p38 hemmten, tötete Salinomycyn deutlich mehr Melanomzellen und führte zu einem auffälligen Anstieg in Anzahl und Größe der zytoplasmatischen Vakuolen. Die Blockade einer kalziumabhängigen Enzymgruppe namens Calpain hatte einen ähnlichen Effekt, sowohl auf die Vakuolenakkumulation als auch auf das Langzeitüberleben. Im Gegensatz dazu reduzierte ein Wirkstoff, der effizienteres „Self‑cleaning“ fördert (Rapamycin), die schädliche Anhäufung von Recycling‑Säckchen und schützte die Zellen vor Salinomycyn. Diese Experimente legen nahe, dass unter Salinomycynstress p38 und Calpain den Melanomzellen helfen, eine verlangsamte, unvollkommene Recyclingantwort als Überlebensstrategie zu nutzen — und dass das Ausschalten dieser Reserve das Medikament wirksamer macht. 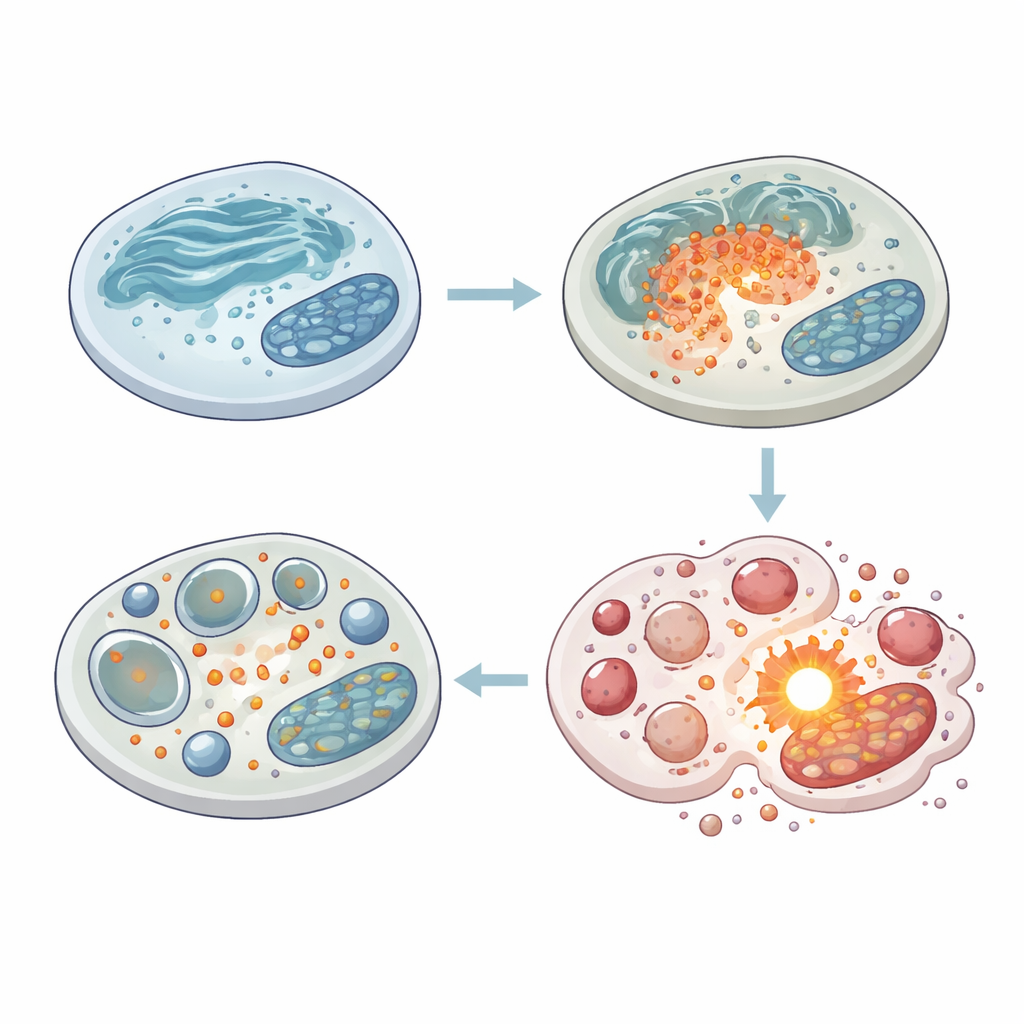
Was das für die künftige Krebsbehandlung bedeuten könnte
Insgesamt zeichnet die Studie Salinomycyn als zweischneidiges Mittel, das cisplatinresistente Melanomzellen in schweren inneren Stress treibt, sie mit Kalzium überflutet, ihr Abfallmanagement blockiert und sie letztlich in den programmierten Zelltod treibt. Gleichzeitig versuchen die Zellen, sich mit einer p38‑gesteuerten Recyclingantwort und anderen Überlebenswegen zu verteidigen. Für Patientinnen und Patienten ist die praktische Botschaft, dass Salinomycyn — oder verbesserte Derivate — eines Tages mit Wirkstoffen kombiniert werden könnten, die diese Überlebenswege blockieren, wie p38‑Inhibitoren oder Autophagiehemmer, um hartnäckige Melanomzellen gezielt zu beseitigen und dabei niedrigere Dosen der Einzelwirkstoffe zu verwenden. Obwohl noch viel Arbeit nötig ist, bevor diese Strategie in die Klinik gelangt, bietet die Studie eine detaillierte Landkarte von Verwundbarkeiten, die kombinatorische Therapien ausnutzen könnten.
Zitation: Tyagi, M., Patro, B.S. Interplay between autophagy and p38 MAPK during salinomycin-induced cell death in cisplatin-resistant melanoma. Sci Rep 16, 9640 (2026). https://doi.org/10.1038/s41598-025-34796-5
Schlüsselwörter: Melanom, Arzneimittelresistenz, Salinomycyn, Autophagie, Kombinationstherapie