Clear Sky Science · de
Ein vollautomatisierter Arbeitsablauf für die digitale Bildanalyse des intestinalen Mikrokolonien-Überlebensassays
Warum schnellere, fairere Gewebeauswertung wichtig ist
Wenn Ärztinnen, Ärzte und Forschende untersuchen, wie Strahlung den Darm beeinflusst, stützen sie sich häufig auf mühsame Inspektionen von Mikroskopbildern. Expertinnen und Experten müssen winzige Taschen regenerierender Zellen im Dünndarm visuell zählen — eine Aufgabe, die langsam, ermüdend und überraschend subjektiv ist. Dieser Artikel stellt einen Weg vor, einen Großteil dieser Arbeit an einen Computer zu übergeben, indem moderne Bildanalyse und künstliche Intelligenz (KI) die Strukturen automatisch zählen. Das Ziel ist einfach, aber wirkungsvoll: Strahlenstudien konsistenter, schneller und weniger abhängig von knappem Expertenaufwand zu machen.
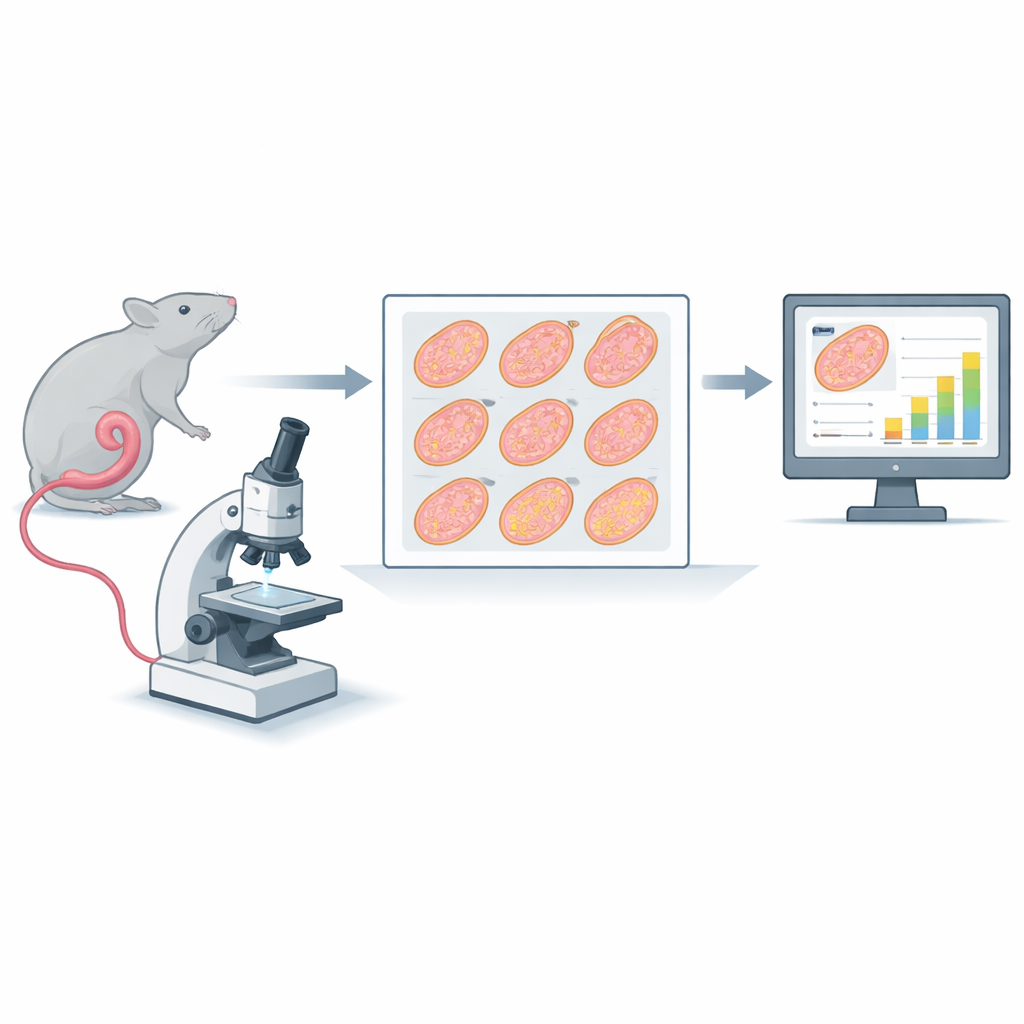
Vom Mausdarm zu digitalen Schnitten
Die Forschung dreht sich um einen klassischen Test, den intestinalen Mikrokolonien-Überlebensassay. Bei diesem Test erhalten Mäuse eine Bestrahlung des Bauchbereichs. Etwa dreieinhalb Tage später wird ein Abschnitt des Dünndarms (Jejunum) entnommen, in neun kurze Segmente geschnitten, in Paraffin eingebettet, in ultradünne Querschnitte geschnitten, gefärbt und hochaufgelöst gescannt. Jeder Scan erzeugt ein riesiges digitales Bild, das neun kreisförmige Querschnitte des Darmgewebes enthält. Traditionell zoomen geschulte Beobachter in jeden Kreis hinein und zählen die Crypten — kleine, drüsenähnliche Taschen am inneren Rand, in denen sich Zellen regenerieren. Weniger überlebende Crypten deuten auf stärkere Schäden durch Strahlung oder kombinierte Behandlungen wie Chemotherapie hin.
Das Problem des manuellen Zählens
Manuelles Zählen klingt vielleicht einfach, doch die Arbeit zeigt, dass dem nicht so ist. Fünfzehn Personen, darunter erfahrene und unerfahrene Zähler, wurden darin geschult, nach standardisierten Regeln zu entscheiden, was als Crypt zählt. Trotzdem wichen ihre Zählungen auf denselben Bildern häufig stark voneinander ab. Über mehr als 300 Schnitte hinweg betrug die durchschnittliche Abweichung vom Gruppenmittel etwa ein Drittel, und die Uneinigkeit war am größten, wenn nur sehr wenige Crypten vorhanden waren. Sogar unter drei Experten mit jahrelanger Erfahrung blieben Unterschiede von rund zehn Prozent. Solche Variation kann so groß sein wie die Behandlungseffekte, die Forschende messen wollen, und erhöht das Risiko, dass wichtige Befunde durch menschliches Rauschen verwischt werden.
Wie der automatisierte Workflow funktioniert
Die Autorinnen und Autoren entwickelten einen vierstufigen automatisierten Workflow, der das Vorgehen eines sorgfältigen Menschen nachbildet und zusätzliche Fähigkeiten bietet. Zuerst nimmt ein Computerprogramm jedes große Digitalbild und schneidet automatisch die neun Gewebekreise aus, wobei Größen- und Farbunterschiede der Färbung ausgeglichen werden. Zweitens markiert ein Tiefenlernmodell namens nnU-Net in jedem Kreis die Pixel, die zu Crypten gehören, und erzeugt eine schwarz-weiße „Maske“ wahrscheinlicher Crypt-Bereiche. Drittens verfolgt ein kundenspezifischer Algorithmus die Konturen jeder Region, filtert winzige Partikel heraus, die zu klein sind, um echte Crypten zu sein, und — entscheidend — versucht verschmolzene Regionen zu teilen, die tatsächlich mehrere benachbarte Crypten enthalten. Schließlich erlaubt eine grafische Oberfläche einem menschlichen Prüfer, die Umrisse über dem Originalbild zu sehen, Fehler mit wenigen Klicks zu korrigieren und die endgültigen Zählungen und Messwerte automatisch zu speichern.
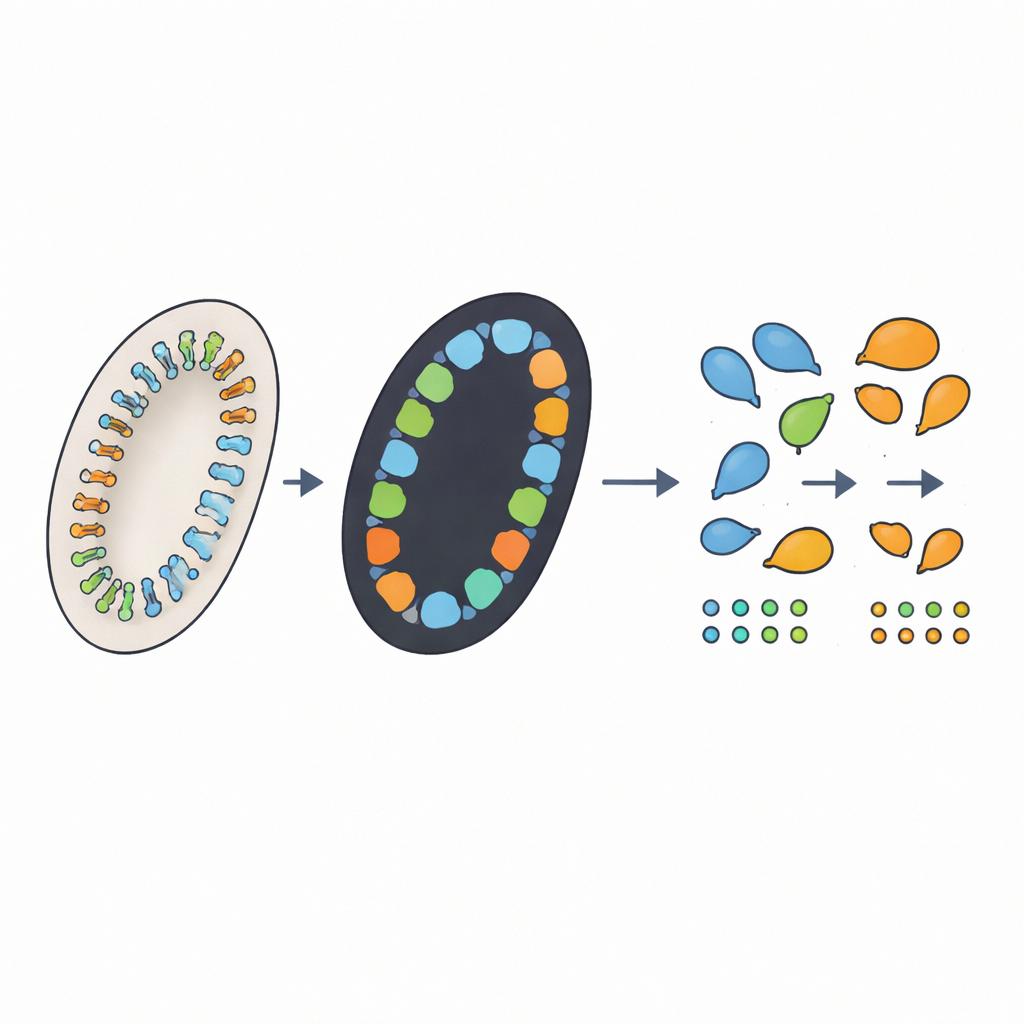
Wie Experten erreichen, aber in Stunden statt Wochen
Um die Leistung des automatisierten Workflows zu bewerten, verglich das Team seine Zählungen mit Expertenbewertungen in mehreren Datensätzen. Für die Bilder, die zur Schulung verwendet wurden, markierte der Tiefenlernschritt die Crypt-Bereiche mit sehr hoher Genauigkeit, und der Zählalgorithmus lag nach dem Hinzufügen des Schritts zum Auftrennen verschmolzener Crypten nur um wenige Crypten vom Expertenkonsens entfernt. Bei neuen, im Training nicht gesehenen Bildern unterschieden sich die automatisierten Zählungen im Mittel um etwa zehn Prozent von dem Durchschnitt der drei Experten — ähnlich groß oder etwas besser als die Unterschiede zwischen den Experten untereinander. Wenn Expertinnen und Experten die automatisierten Ergebnisse später per Oberfläche überprüften und korrigierten, benötigten sie typischerweise weniger als eine Minute pro Bild. Insgesamt konnte ein komplettes Experiment mit 60 Mäusen in nur wenigen Stunden Rechnerzeit und wenigen Minuten menschlicher Arbeit verarbeitet werden.
Neue Wege, Darmschäden zu beschreiben
Weil der Workflow vollständige digitale Bilder analysiert, kann er leicht Merkmale messen, die von Hand schwer zu erfassen sind, etwa die Länge des Darmumfangs oder die Fläche jeder Crypta. Die Autorinnen und Autoren prüften, ob die Anpassung der Crypt-Zahlen an diese Merkmale — also die Frage, ob „Crypten pro Darmlängeneinheit“ oder „Crypten bereinigt nach ihrer Größe“ Strahlenschäden besser widerspiegeln — ein klareres Signal liefert. In dieser Studie übertrafen keine der alternativen Maße durchgehend die rohen Crypt-Zahlen, aber der Ansatz zeigt, wie automatisierte Bildanalyse den Weg zu reichhaltigeren, nuancierteren Markern für Gewebeschäden öffnen kann.
Was das für zukünftige Forschung bedeutet
Für Nicht-Spezialisten ist die wichtigste Erkenntnis: Die Forschenden haben einen praktischen digitalen Helfer gebaut, der komplexe Gewebeschnitte nahezu so zuverlässig wie erfahrene Expertinnen und Experten lesen kann, dabei aber viel schneller und konsistenter ist. Indem mühselige manuelle Arbeit reduziert und menschliche Unterschiede geglättet werden, kann dieses automatisierte System Darmstrahlungsstudien robuster und leichter vergleichbar zwischen Laboren machen. Die Autorinnen und Autoren weisen auch auf klare Verbesserungsmöglichkeiten hin, etwa Modelle, die benachbarte Crypten direkt separieren. Über diesen einzelnen Assay hinaus bietet ihr Rahmen einen Bauplan zur Automatisierung weiterer mikroskopischer Auswertungen und bewegt die Pathologie in Richtung einer Zukunft, in der sorgfältiges menschliches Urteil von transparenten, verlässlichen KI-Werkzeugen unterstützt — nicht ersetzt — wird.
Zitation: Baikalov, A., Wang, E., Neill, D. et al. A fully automated workflow for the digital image analysis of the intestinal microcolony survival assay. Sci Rep 16, 9633 (2026). https://doi.org/10.1038/s41598-025-34719-4
Schlüsselwörter: intestinaler Mikrokolonien-Überlebensassay, automatisierte Histopathologie, Tiefenlern-Bildanalyse, strahleninduzierte Darmschädigung, Crypt-Zähl-Workflow