Clear Sky Science · de
Aktivierung von M1-mAChR verbessert räumliche Lern- und Gedächtnisstörungen bei Ratten, die chronischer intermittierender Hypoxie ausgesetzt sind
Warum nächtliche Atmung für Ihr Gedächtnis wichtig ist
Viele Menschen mit obstruktiver Schlafapnoe hören nachts wiederholt auf zu atmen, wodurch es zu starken Abfällen des Blutsauerstoffs kommt. Neben lautem Schnarchen und Tagesmüdigkeit können diese kurzen erstickungsähnlichen Episoden still und unbemerkt Hirnregionen schädigen, die Lernen und Gedächtnis unterstützen. Diese Studie nutzte ein Rattenmodell, um eine einfache, aber wichtige Frage zu stellen: Kann ein sanftes Anheben einer bestimmten Art von Gehirnsignal die Gedächtnisnetzwerke vor den Schäden durch wiederholte Niedrigsauerstoffphasen schützen?
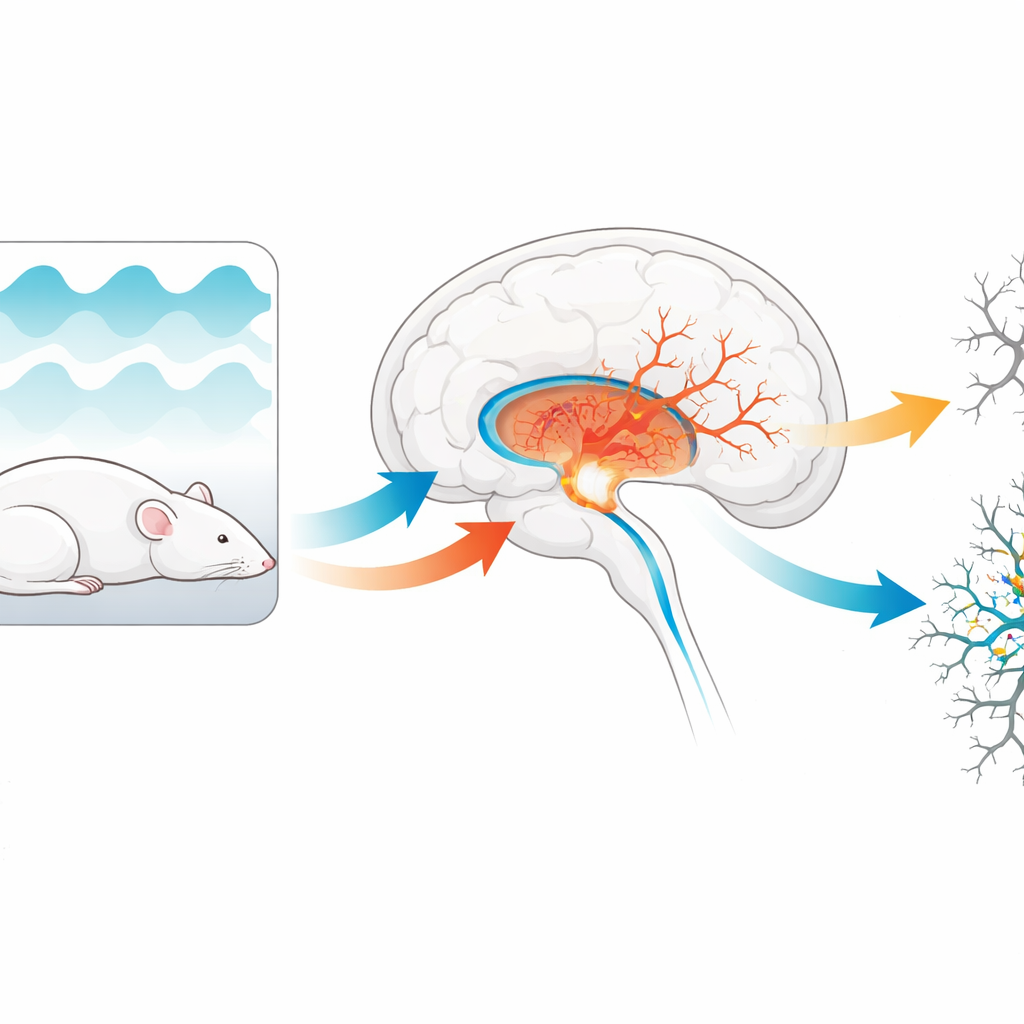
Schlaf, Sauerstoffabfälle und ein verletzliches Gedächtniszentrum
Die obstruktive Schlafapnoe ist durch chronische intermittierende Hypoxie gekennzeichnet—schnelle Zyklen von niedrigem und normalem Sauerstoff. Der Hippocampus, eine tiefliegende Hirnstruktur, die für die Bildung räumlicher und alltäglicher Erinnerungen entscheidend ist, ist für solchen Stress besonders empfindlich. Frühere Arbeiten zeigten, dass apnoeähnliche Zustände Neuronen ausdünnen und die chemische Kommunikation zwischen ihnen stören können. Zwei Signalwege stechen in diesem Zusammenhang hervor: eine Familie von Rezeptoren, die auf den Botenstoff Acetylcholin reagieren (wichtig für Aufmerksamkeit und Gedächtnis), und ein innerer Relay-Mechanismus, die JAK2/STAT3-Signalachse, die Zellen hilft, sich an Stress anzupassen und zu überleben.
Apnoeähnlichen Stress im Labor testen
Um Schlafapnoe nachzuahmen, setzten die Forschenden gesunde Ratten in eine Kammer, in der die Sauerstoffwerte täglich acht Stunden lang wiederholt absanken und anstiegen—über vier Wochen. Einige Tiere erlebten nur dieses Sauerstoffzyklisieren, andere erhielten zusätzlich Medikamente, die entweder die JAK2/STAT3-Relay blockierten oder den M1-muskarinischen Acetylcholinrezeptor aktivierten, einen wichtigen acetylcholinempfindlichen Schalter im Hippocampus. Das Team maß dann, wie gut die Ratten den Standort einer versteckten Plattform in einem Wassermaze erlernen und sich später daran erinnern konnten. Außerdem untersuchten sie Hirngewebe, um Neuronen zu zählen und zu prüfen, wie viel der Schlüsselorote M1-Rezeptor und STAT3 vorhanden waren.
Was niedriger Sauerstoff mit Lernen und Gehirnzellen machte
Ratten, die dem apnoeähnlichen Sauerstoffmuster ausgesetzt waren, hatten im Wassermaze Schwierigkeiten. Sie legten längere Wege zurück, um die Plattform zu finden, und verbrachten, als diese entfernt wurde, weniger Zeit im richtigen Bereich—Anzeichen für geschwächtes räumliches Lernen und Gedächtnis. Unter dem Mikroskop zeigten ihre Hippocampus-Neuronen eine geringere Zahl, stärkere Unordnung und Merkmale von Zellschäden. Auf molekularer Ebene waren sowohl das gesamte STAT3 als auch seine aktive, eingeschaltete Form reduziert, ebenso die Menge des M1-Rezeptors im Hippocampus. Kurz gesagt: Wiederholte Sauerstoffabfälle trübten genau jene Signalwege, die Neuronen helfen sollen, mit Stress umzugehen und Gedächtnisprozesse zu stützen.
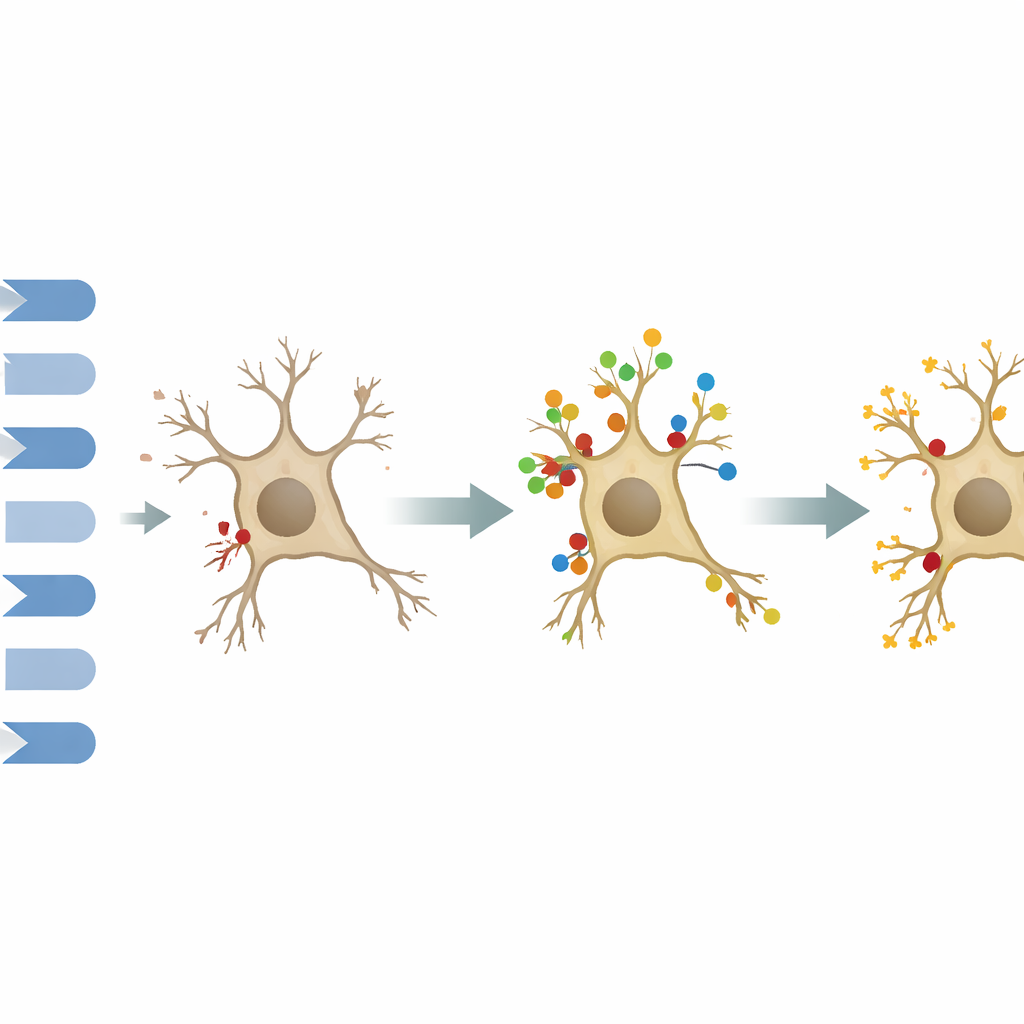
Ein schützender Schalter mit wichtiger Abhängigkeit
Das Aktivieren des M1-Rezeptors mit einem selektiven Wirkstoff, VU0364572, kehrte diese Probleme teilweise um. Behandelte Ratten lernten das Maze schneller und suchten genauer an der früheren Plattformposition, und ihr Hippocampusgewebe zeigte eine besser erhaltene Struktur und höhere M1-Rezeptorwerte. Im Gegensatz dazu verbesserte das Blockieren von JAK2—einem wichtigen upstream-Aktivator von STAT3—mit dem Wirkstoff AG490 das Verhalten nicht und löschte sogar die Vorteile der M1-Aktivierung, wenn beide Substanzen zusammen verabreicht wurden. Interessanterweise stellten weder Behandlung die STAT3-Proteinwerte unter diesen Bedingungen wieder her, was nahelegt, dass möglicherweise die Integrität des Signalwegs wichtiger ist als dessen Gesamtmenge.
Was das für Menschen bedeutet, die sich wegen Schnarchens und Gedächtnis sorgen
Für eine allgemeine Leserschaft ist die Schlussfolgerung: Die Reaktion des Gehirns auf Sauerstoffschwankungen im Schlaf ist nicht festgelegt; sie lässt sich in Richtung Verletzung oder Schutz verschieben, je nachdem, welche chemischen Schalter aktiviert werden. In dieser Rattenstudie schadete chronisch intermittierender Niedrigsauerstoff den Gedächtnisnetzwerken und reduzierte sowohl einen wichtigen Oberflächenrezeptor als auch ein internes Stressantwort‑Relay. Ein sanftes Anheben des M1-Rezeptors half den Ratten, trotz des Sauerstoffstresses klarer zu denken und sich besser zu erinnern, jedoch nur, wenn die JAK2/STAT3‑Achse intakt blieb. Obwohl diese Arbeit noch weit von einer Behandlung für Menschen entfernt ist, hebt sie eine vielversprechende Strategie hervor: wirksame Apnoeversorgung mit Medikamenten zu kombinieren, die verletzliche Gedächtnisnetzwerke stärken, statt ausschließlich den Sauerstoff zu adressieren.
Zitation: Huang, Q., Hu, C., Liu, H. et al. Activation of M1mAChR’s improves spatial learning and memory deficits in rats exposed to chronic intermittent hypoxia. Sci Rep 16, 8836 (2026). https://doi.org/10.1038/s41598-025-34689-7
Schlüsselwörter: obstruktive Schlafapnoe, intermittierende Hypoxie, Hippocampus, Lernen und Gedächtnis, Acetylcholinrezeptoren