Clear Sky Science · de
Zielgerichtete Stabilisierung von Hypoxie‑induzierbarem Faktor 1‑alpha (HIF1A) während der in vitro‑Reifung von bovinen Cumulus‑Oozyten‑Komplexen erhöht die Blastozystenraten
Warum das Feinjustieren der Sauerstoffwahrnehmung in Eizellen wichtig ist
Die moderne Rinderzucht baut stark auf im Labor hergestellten Embryonen auf, doch der Erfolg ist alles andere als sicher: Nur etwa ein Drittel der Eizellen erreicht das entscheidende Blastozystenstadium, in dem sie bereit für den Transfer in eine Kuh sind. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage für Tierzucht und assistierte Reproduktion: Wenn wir die niedrigen Sauerstoffbedingungen, denen Eizellen im Eierstock natürlicherweise ausgesetzt sind, besser nachahmen—indem wir einen zentralen Sauerstoffsensor dezent verstärken—können wir dann mehr Embryonen zu einer erfolgreichen Entwicklung verhelfen?
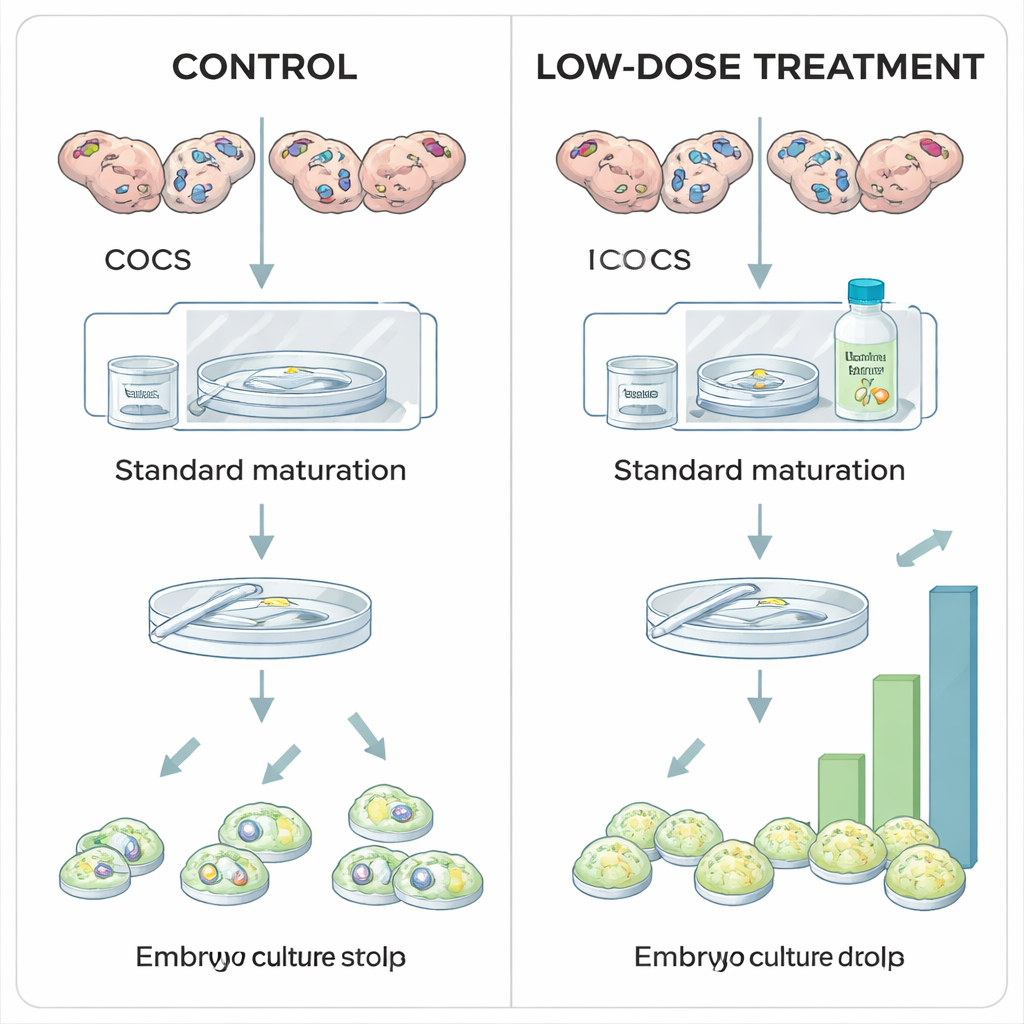
Das Leben beginnt in einer niedrig‑sauerstoff Nische
Im Eierstock ist jede sich entwickelnde Eizelle von einem unterstützenden Zellverband, dem Cumulus, umgeben; zusammen bilden sie einen Cumulus‑Oozyten‑Komplex. Obwohl der Eierstock mit dem Wachstum von Follikeln besser durchblutet wird, reichen Blutgefäße nicht bis unmittelbar an die Eizelle heran. Sauerstoff muss erst diffundieren, wodurch um die heranreifende Eizelle eine mäßig sauerstoffarme, also hypoxische, Umgebung entsteht. In dieser Nische hilft ein intrazellulärer Sensor namens HIF1A den Zellen, sich anzupassen, indem er Stoffwechsel und Hormonproduktion einstellt. Frühere Arbeiten zeigten, dass die Blockade von HIF1A die Eizellreifung beeinträchtigt und die Embryonenbildung drastisch reduziert—was dieses Protein als zentralen Koordinator der Eizellkompetenz herausstellt, also der Fähigkeit einer Eizelle, befruchtet zu werden und sich zu einem gesunden Embryo zu entwickeln.
Ein Medikament zur Feineinstellung des Sauerstoffsensors der Eizelle
Die Forschenden untersuchten, ob eine moderate Stabilisierung von HIF1A während der Laborreifung boviner Eizellen die Embryonenausbeute erhöhen könnte. In üblichen in vitro‑Protokollen werden Cumulus‑Oozyten‑Komplexe unter Normalluft‑Sauerstoffbedingungen reifen gelassen, vorwiegend aus praktischen und nicht aus biologischen Gründen. Hier wurden aus Schlachthof‑Ovarien gewonnene Eizellen in Gruppen aufgeteilt und während der 24‑stündigen Reifungsperiode verschiedenen Dosen von Roxadustat ausgesetzt, einem Medikament, das bereits in der Humanmedizin zur Behandlung von Anämie verwendet wird. Roxadustat wirkt, indem es eine Enzymfamilie namens Prolyl‑Hydroxylasen (PHDs) hemmt, die HIF1A normalerweise markieren, damit es bei hoher Sauerstoffverfügbarkeit abgebaut wird. Durch die Hemmung der PHDs kann HIF1A‑Protein sich auch bei höheren Sauerstoffwerten anreichern und so das hypoxische Signal, das die Eizelle in vivo wahrnimmt, teilweise nachbilden.
Mehr Blastozysten bei richtiger Dosis, Schaden bei höheren Konzentrationen
Bei der Untersuchung, wie Eizellen und Embryonen nach der Behandlung abschnitten, zeichnete sich ein klares Muster ab. Eine niedrige Dosis Roxadustat (25 Mikromolar) veränderte nicht die Zahl der Eizellen, die die Reifung abschlossen, noch die Anzahl befruchteter Eizellen, die mit der Zellteilung begannen, steigerte jedoch signifikant den Anteil, der das Blastozystenstadium erreichte. Anders gesagt: Die frühen Schritte blieben unverändert, doch mehr Embryonen beendeten erfolgreich den anspruchsvollen Weg zur Blastozyste—was darauf hinweist, dass eine moderate HIF1A‑Stabilisierung die intrinsische Qualität der Eizelle verbessert. Im Gegensatz dazu verringerte die höchste Dosis (100 Mikromolar) den Prozentsatz der Eizellen, die überhaupt reiften, und wenn derselbe Inhibitor später während der acht Tage dauernden Embryokultur angewandt wurde, schnitten hohe Dosen die Blastozystenbildung stark zurück, ohne die frühe Zellteilung zu verändern. Diese Befunde deuten darauf hin, dass „genau genug“ HIF1A‑Aktivität während der Reifung vorteilhaft ist, während zu viel oder zu lange Aktivierung schädlich ist.
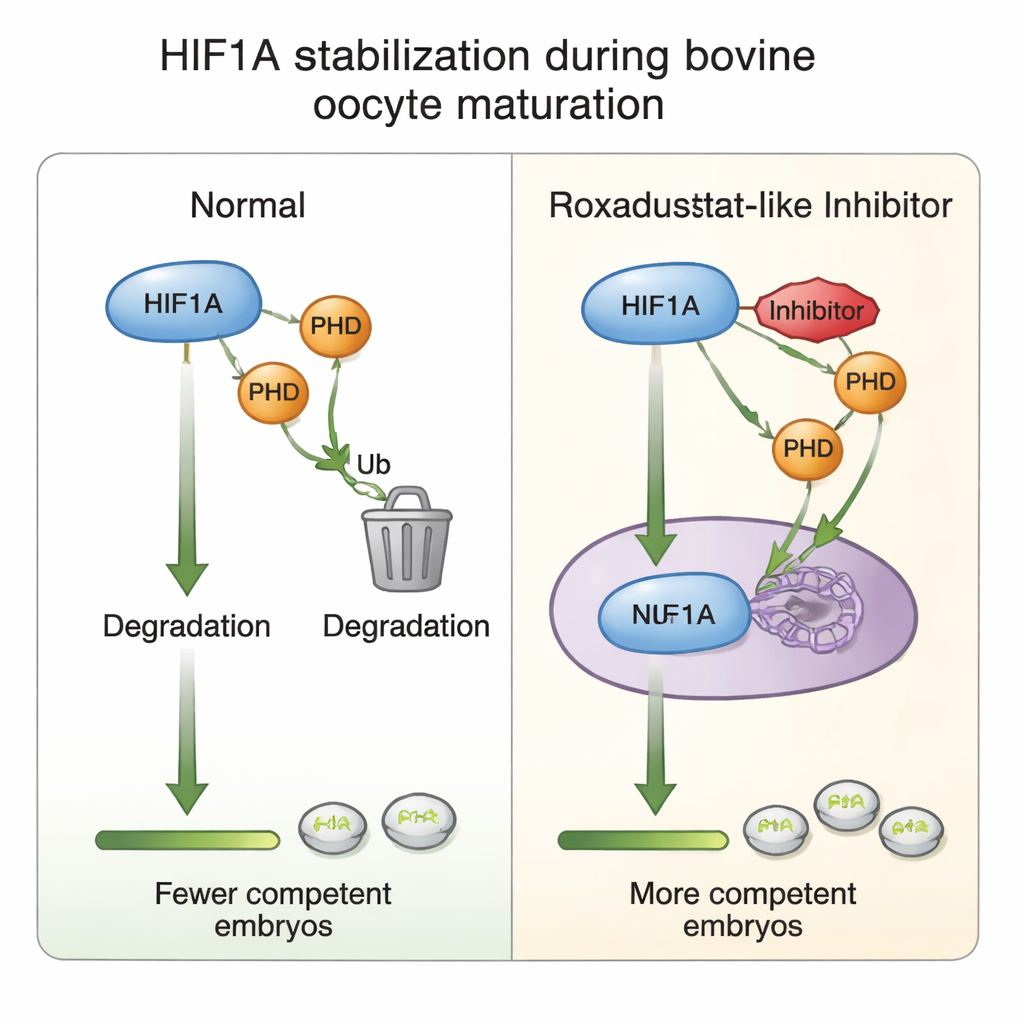
Was in den Stütz‑ (Cumulus‑)Zellen passiert
Um zu verstehen, wie diese chemische Feinabstimmung wirkt, untersuchten die Autorinnen und Autoren die Cumuluszellen, die jede Eizelle umgeben. Sie fanden heraus, dass die Reifung allgemein die HIF1A‑Genaktivität erhöht, das Hinzufügen von Roxadustat jedoch paradoxalerweise die HIF1A‑mRNA verringerte, während die HIF1A‑Proteinspiegel stabil blieben—ein Hinweis darauf, dass Zellen die Genexpression dämpfen könnten, sobald das Protein ausreichend stabilisiert ist, eine Art eingebauter Bremse gegen Überaktivierung. Die Spiegel von PHD2, der empfindlichsten der PHD‑Enzyme gegenüber Sauerstoff, stiegen als Reaktion auf das Medikament an, was seine Rolle im Sauerstoff‑Sensor‑Kreislauf unterstreicht. Bei höheren Medikamentendosen waren Marker für Zellproliferation und für die klebrige Matrix, die das Ausdehnen der Cumuluszellen um die Eizelle unterstützt, reduziert—was mit dem beobachteten Rückgang von Reifung und Embryonenbildung übereinstimmt. All dies stützt die Idee, dass sorgfältig abgestimmte HIF1A‑Aktivität den Dialog zwischen Eizelle und Cumuluszellen feinjustiert, der späteren Entwicklungserfolg ermöglicht.
Folgen für Tierzucht und darüber hinaus
Die Arbeit zeigt, dass eine behutsame Stabilisierung des Sauerstoffsensors der Eizelle während des kurzen Fensters der in vitro‑Reifung die Blastozystenausbeute bei Rindern spürbar erhöhen und stabilisieren kann, ohne Befruchtung oder frühe Furchung zu verändern. Praktisch könnte das zu verlässlicherer Embryonenproduktion für Zuchtprogramme führen, indem ein gezieltes Medikament eingesetzt wird, statt grober Änderungen der Sauerstoffkonzentration oder toxischerer Chemikalien. Die Studie betont zudem eine allgemeinere Lehre für die Humanreproduktionsmedizin: Die Nachahmung der nuancierten, sauerstoffarmen Umgebung des Eierstocks ist nicht einfach eine Frage des Hoch- oder Runterregulierens von Sauerstoff, sondern erfordert das Respektieren des empfindlichen Gleichgewichts von Signalstoffen wie HIF1A. Diese Balance feinzujustieren, statt sie in Extreme zu treiben, könnte ein Schlüssel zu gesünderen Embryonen sein.
Zitation: Gübeli, M., Bleul, U. & Kowalewski, M.P. Targeted hypoxia-inducible factor 1-alpha (HIF1A) stabilization during in vitro maturation of bovine cumulus-oocyte complexes increases blastocyst rates. Sci Rep 16, 7554 (2026). https://doi.org/10.1038/s41598-025-33894-8
Schlüsselwörter: in vitro Embryoproduktion, Oozytenreifung, Hypoxie‑Signalgebung, HIF1A‑Stabilisierung, bovine Reproduktion