Clear Sky Science · de
Konservierte Regionen und molekulares Klonieren von sauren und alkalischen Phosphatasen in Streptomyces sp. MMA-NRC
Warum Bodenphosphor für unsere Nahrung wichtig ist
Die moderne Landwirtschaft ist stark auf Phosphor angewiesen, einen Schlüsselbestandteil von Pflanzendüngern, der den Pflanzen beim Aufbau von DNA, der Energiespeicherung und der Entwicklung starker Wurzeln hilft. Vieles des auf Felder ausgebrachten Phosphors wird jedoch rasch in unlösliche Mineralien gebunden, die Pflanzen nicht nutzen können, während die weltweiten Vorkommen abbauwürdigen Phosphatgesteins begrenzt und ungleich verteilt sind. Diese Studie untersucht eine biologische Alternative: die Nutzung im Boden lebender Mikroben – und sogar gentechnisch veränderter Bakterien –, um Phosphor aus Gesteinsphosphat freizusetzen, was unsere Abhängigkeit von chemischen Düngemitteln verringern und Umweltschäden mindern könnte.
Kleine Helfer, die „feststeckende" Nährstoffe lösen
In vielen Böden ist die Gesamtmenge an Phosphor hoch, doch nur ein winziger Bruchteil liegt in einer Form vor, die Pflanzenwurzeln aufnehmen können. Überschüssiger Dünger verschwendet nicht nur Geld, sondern wird auch in Flüsse und Seen eingetragen und löst dort Algenblüten und tote Zonen aus. Die Autoren konzentrieren sich auf eine Gruppe von Bodenbakterien namens Streptomyces, die bereits für die Produktion von Antibiotika und leistungsfähigen Enzymen bekannt sind. Ein Stamm, Streptomyces sp. MMA-NRC, kann Gesteinsphosphat auflösen – ein günstiger, aber schlecht löslicher Dünger. Das Team wollte zwei seiner Schlüsselenzyme verstehen und nutzbar machen: saure Phosphatase und alkalische Phosphatase – molekulare Werkzeuge, die Phosphor-haltige Gruppen von sonst unbrauchbaren Verbindungen abspalten.
Die Baupläne der Enzyme lesen und modellieren
Zunächst isolierten die Forscher die Gene, die für diese beiden Phosphatasen im MMA-NRC-Stamm kodieren. Sie vervielfältigten und sequenzierten die Gene, die sich als Proteine mit 488 bzw. 560 Bausteinen (Aminosäuren) herausstellten, und legten die Sequenzen in öffentlichen Datenbanken ab. Mit Bioinformatik-Werkzeugen verglichen sie diese Proteine mit verwandten Enzymen anderer Bakterien und zeigten, dass die MMA-NRC-Varianten eng verwandt sind – etwa 99 % Ähnlichkeit zu einem anderen Streptomyces-Stamm. Anschließend erstellten sie detaillierte dreidimensionale Computermodelle der Enzyme und überprüften deren Qualität mit etablierten Methoden, die beurteilen, ob jede Aminosäure an einer realistischen Position sitzt. Die Modelle bestanden diese Prüfungen mit hohen Werten, was darauf hindeutet, dass die virtuellen Strukturen den realen sehr ähnlich sind.
Wie gut die Enzyme Gesteinsphosphat greifen
Mithilfe der 3D-Modelle führten die Wissenschaftler „Docking“-Simulationen durch, um zu prüfen, wie stark die Enzyme an Gesteinsphosphat, ihr Zielsubstrat, binden könnten. In diesen Simulationen werden Enzym und Mineral in vielen möglichen Orientierungen zusammengebracht, und ein Computer schätzt, welche Anordnungen am stabilsten sind. Sowohl die saure als auch die alkalische Phosphatase von MMA-NRC zeigten sehr starke vorhergesagte Bindungsenergien an Gesteinsphosphat, was bedeutet, dass sie voraussichtlich fest mit der Mineraloberfläche interagieren. Bestimmte Aminosäuren in den Enzymen bildeten Wasserstoffbrücken und hydrophobe Kontakte mit dem Gesteinsphosphat-Modell und zeichneten wahrscheinliche aktive Zentren nach, an denen chemische Reaktionen zur Freisetzung von Phosphor stattfinden würden.
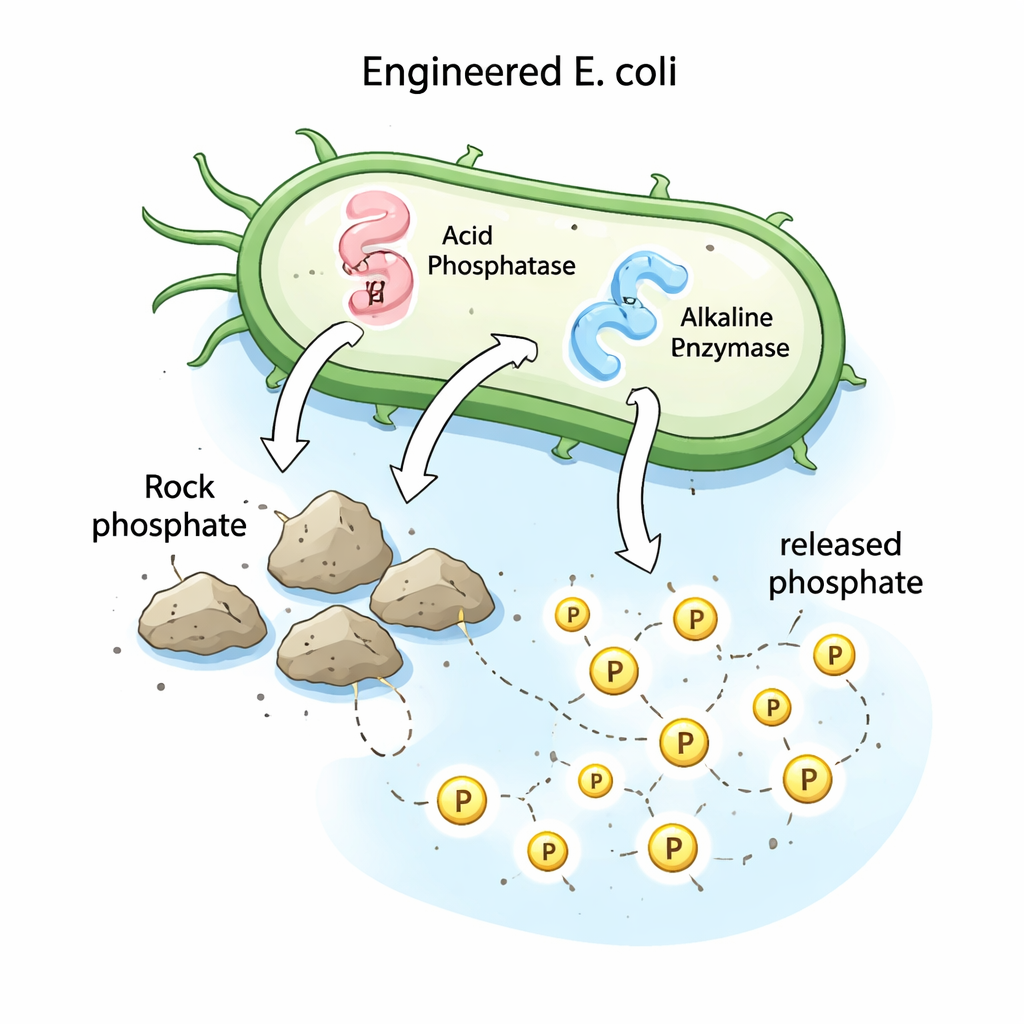
Ein Laborbakterium in einen Phosphorfrei-setzer verwandeln
Um diese Ideen experimentell zu testen und ein praktisches Werkzeug zu schaffen, überführten die Forscher die Phosphatasen-Gene von Streptomyces in ein gut untersuchtes Laborbakterium, Escherichia coli DH5α. Sie setzten jedes Gen in einen Standard-Klonierungsvektor ein und transformierten die Plasmide in E. coli, wobei sie Kolonien auswählten, die die neue DNA aufgenommen hatten. Diese gentechnisch veränderten Stämme wurden anschließend in einem Medium kultiviert, das Gesteinsphosphat als einzige Phosphorquelle enthielt. Während unverändertes E. coli keinen messbaren Phosphor freisetzen konnte, setzten die rekombinanten Stämme, die entweder saure oder alkalische Phosphatase produzierten, nach sieben Tagen etwa 53 bzw. 57 Milligramm löslichen Phosphor pro Liter frei – deutlich mehr als der ursprüngliche Streptomyces-Stamm, der unter denselben Bedingungen etwa 35 Milligramm pro Liter freisetzte.
Was das für umweltfreundlichere Landwirtschaft bedeuten könnte
Für Nicht-Expertinnen und Nicht-Experten ist das Fazit klar: Durch das Verständnis und die Nutzung der natürlichen Enzyme können Wissenschaftler preiswertes, schlecht lösliches Gesteinsphosphat in eine für Pflanzen besser verfügbare Nährstoffquelle verwandeln. Die hohe Aktivität der modellierten und geklonten Phosphatasen deutet darauf hin, dass Stämme wie Streptomyces sp. MMA-NRC oder gentechnisch veränderte Bakterien mit deren Genen Teil von Biofertilisern werden könnten, die die Abhängigkeit von konventionellen Phosphordüngern verringern. Solche biologischen Lösungen könnten Landwirten helfen, Erträge zu halten, während sie Umweltbelastungen senken und den Druck auf begrenzte globale Phosphorreserven mindern – ein Beitrag zu nachhaltigeren und widerstandsfähigeren Lebensmittelsystemen.
Zitation: Abd El-Aziz, N.M. Conserved regions and molecular cloning of Acid and Alkaline phosphatases in Streptomyces sp. MMA-NRC. Sci Rep 16, 7493 (2026). https://doi.org/10.1038/s41598-025-33881-z
Schlüsselwörter: Phosphat-solubilisierende Bakterien, Biofertilizer, Streptomyces, Phosphatase-Enzym, Gesteinsphosphat