Clear Sky Science · de
Auf dem Weg zu digitalen Zwillingen der Herz-Elektrophysiologie mit einem effizienten Open-Source-skalierten Solver für GPU-Cluster
Warum der Bau virtueller Herzen wichtig ist
Bei der Behandlung von Herzrhythmusstörungen arbeiten Ärztinnen und Ärzte oft teilweise im Dunkeln: Sie können elektrische Signale an der Körperoberfläche messen, sehen aber nicht ohne Weiteres, wie diese Signale tief im Herzen verlaufen. Diese Studie beschreibt leistungsfähige neue Rechenwerkzeuge, die das Schlagen eines individuellen Herzens detailliert simulieren können — schnell genug, um viele „Was-wäre-wenn“-Szenarien zu untersuchen. Durch die Kombination realistischer Herzgeometrie mit modernen Grafikprozessoren bringen die Autorinnen und Autoren uns näher an sichere, kostengünstige virtuelle Experimente an digitalen Kopien einzelner Patientinnen und Patienten.
Von einfachen Modellen zu digitalen Zwillingen
Moderne Herzsimulationen können Aktivität von der Ebene einzelner Zellen bis zum gesamten Organ abbilden, doch die getreue Reproduktion der elektrischen Ausbreitung im Herzen ist sowohl mathematisch komplex als auch rechenintensiv. Ein zentrales Ziel für die Medizin ist der „cardiac digital twin“: ein personalisiertes Computermodell, das das Herz eines bestimmten Patienten nachbildet und verwendet werden kann, um Medikamente, Geräte oder Stimulationsstrategien vor einem klinischen Einsatz zu testen. Damit das praktikabel wird, muss die Software für diese Simulationen sowohl schnell als auch genau sein, wichtige anatomische Strukturen enthalten und offen zugänglich sein, damit Forschende weltweit sie prüfen, verbessern und wiederverwenden können.
Das verborgene Leitungsnetz des Herzens erfassen
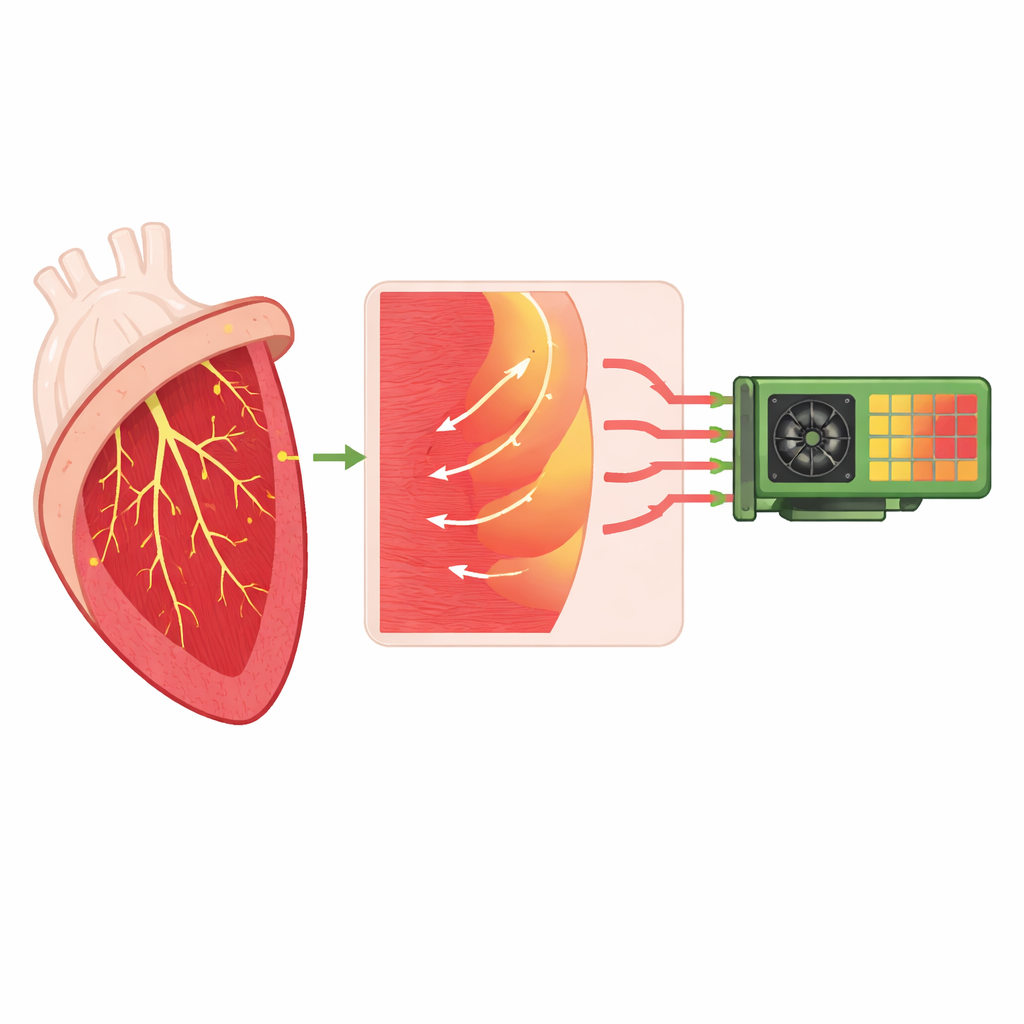
Die Arbeit konzentriert sich auf einen Open-Source-Simulator namens monoalg3d, der modelliert, wie elektrische Signale durch den Herzmuskel und sein spezialisiertes Leitungssystem laufen. Dieses System, als Purkinje-Netzwerk bekannt, überträgt das herzschlagauslösende Signal schnell von den oberen Leitungsbahnen zu vielen kleinen Anschlussstellen über die Innenseite der Ventrikel. An jedem dieser Knoten muss eine dünne Purkinje-Faser eine deutlich größere Masse an Herzmuskel erregen, wodurch eine natürliche Verzögerung entsteht und unter bestimmten Bedingungen ein Risiko für Blockaden oder abnorme Leitungen besteht. Die Autorinnen und Autoren erweitern monoalg3d so, dass es dieses Leitungssystem und seine Übergänge realistischer abbildet, einschließlich der Asymmetrie zwischen Signalen von Purkinje zum Muskel und umgekehrt.
Supercomputer und GPUs als Herzlabore nutzen
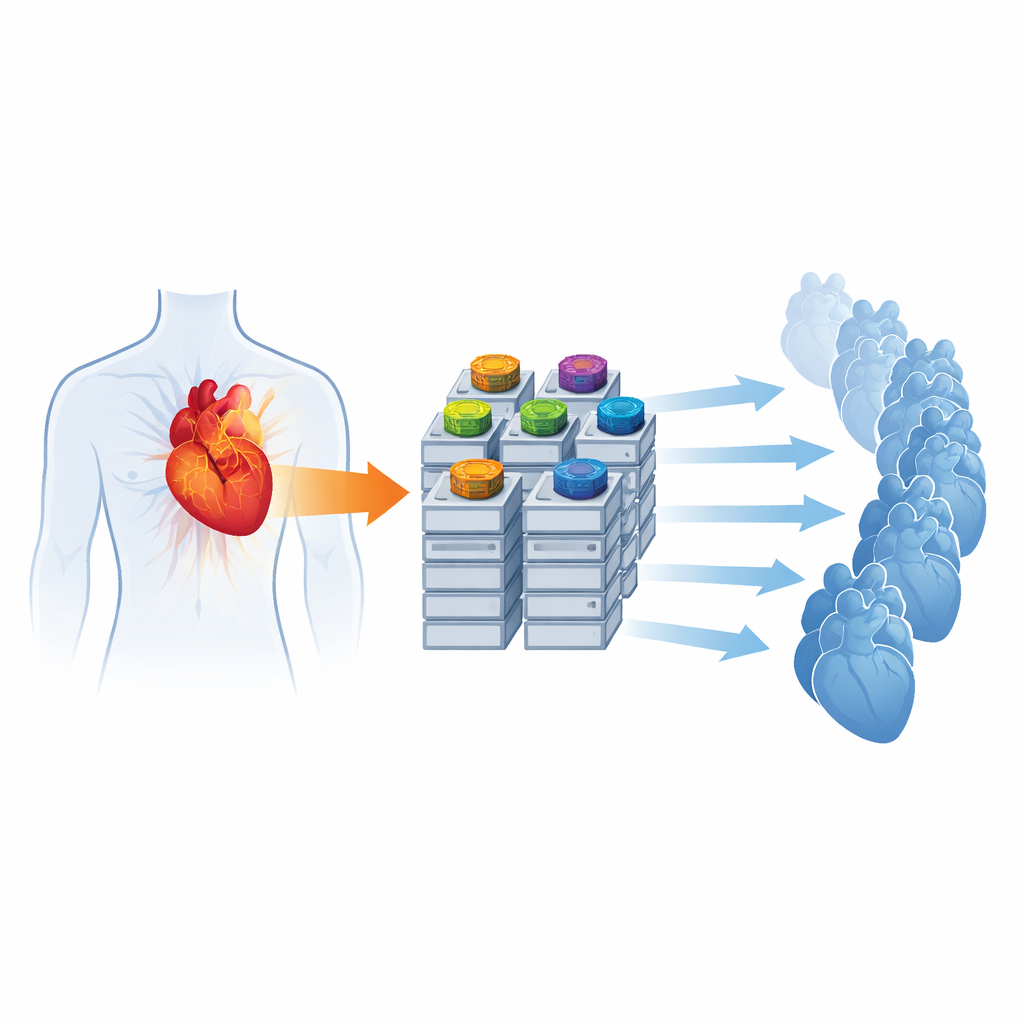
Um derart detaillierte Modelle schnell laufen zu lassen, überarbeiten die Forschenden, wie der Simulator die Hardware nutzt. Sie gestalten den numerischen Kern neu, sodass sowohl die lokalen Zelldynamiken als auch die Ausbreitung der Spannung im Herzen direkt auf Grafikprozessoren (GPUs) gelöst werden — Geräte, die ursprünglich für Bilddarstellung entwickelt wurden, heute aber weit verbreitet in der wissenschaftlichen Berechnung eingesetzt werden. Durch sorgfältige Organisation der Daten für GPU-Bibliotheken und das Vermeiden häufiger Übertragungen zwischen CPU und GPU zeigen sie, dass eine vollständig GPU-basierte Konfiguration einen Standard-Benchmark gegenüber einer herkömmlichen reinen CPU-Version nahezu elfmal beschleunigen kann. Außerdem führen sie ein neues, kompaktes Ausgabeformat ein, um den Speicherbedarf drastisch zu reduzieren, und eine Message-Passing-Funktion, mit der Hunderte von Simulationen parallel über einen Supercomputer gestartet werden können, wobei jede ein anderes Set physiologischer Parameter untersucht.
Virtuelle Herzen so trainieren, dass sie realen Patienten gleichen
Über die reine Geschwindigkeit hinaus prüfen die Autorinnen und Autoren, ob ihr verbesserter Solver realistische, patientenspezifische Simulationen unterstützt. Anhand einer drei-dimensionalen Rekonstruktion eines menschlichen Herzens aus medizinischen Bilddaten fügen sie ein synthetisches Purkinje-Netzwerk an und passen zentrale Knotenparameter an: den Widerstand an jeder Verbindung und wie viele benachbarte Muskelregionen jeder Purkinje-Terminal erregt. Automatisch durchlaufen sie Hunderte von Kombinationen dieser Werte, starten Simulationen, die von einem Stimulus im Hauptleitungsbündel ausgehen, und messen sowohl die kleinen Verzögerungen an jedem Übergang als auch die resultierenden Elektrodiagramm-(EKG-)Signale auf der Brust. Für ein fein aufgelöstes Herznetz identifizieren sie Parameterwerte, die physiologisch plausible Aktivierungszeiten und EKG-Wellenformen liefern, die gut mit den Aufzeichnungen eines echten Patienten korrelieren, während einzelne Simulationen innerhalb weniger Stunden bleiben, selbst wenn 512 Läufe gleichzeitig ausgeführt werden.
Viele mögliche Herzen, die außen gleich aussehen
Ein interessantes Ergebnis ist, dass unterschiedliche interne Leitungsstrukturen und Knotenspannungen zu sehr ähnlichen EKGs an der Körperoberfläche führen können. Mit anderen Worten: Mehrere verschiedene digitale Herzen können gleichermaßen mit denselben klinischen Daten vereinbar erscheinen. Die Autorinnen und Autoren zeigen, dass einige Purkinje-Knoten besonders einflussreich sind, wobei ihre lokalen Verzögerungen zwischen gleichermaßen gut passenden Simulationen erheblich variieren, während das Gesamtaktivierungstiming über die Ventrikel stabil bleibt. Diese Nicht-Eindeutigkeit legt nahe, dass künftige digitale-Zwilling-Frameworks zusätzliche Daten oder Einschränkungen benötigen werden — etwa detailliertere Bildgebung oder invasive Messungen — um für einen gegebenen Patienten eine einzelne, am wahrscheinlichsten zutreffende interne Konfiguration festzulegen.
Was das für die zukünftige Versorgung bedeutet
Zusammenfassend liefert diese Studie einen frei verfügbaren, GPU-beschleunigten Simulator, der detaillierte Herzgeometrie, realistisches Leitungssystem und große Chargen personalisierter Simulationen auf modernen Rechenclustern bewältigen kann. Für Nichtfachleute ist die Kernbotschaft, dass es zunehmend praktikabel wird, schnelle, hochauflösende virtuelle Herzexperimente durchzuführen, die individuellen Patienten ähneln, einschließlich subtiler Verzögerungen an den inneren Leitungsübergängen des Herzens. Zwar ist noch Arbeit nötig, um diese Modelle vollständig zu personalisieren und interne Unsicherheiten aufzulösen, doch die hier vorgestellten Werkzeuge bilden einen wichtigen Baustein für künftige Diagnose-, Risikobewertungs- und Behandlungsplanungsansätze auf Basis digitaler Zwillinge in der Kardiologie.
Zitation: Berg, L.A., Oliveira, R.S., Camps, J. et al. Toward cardiac electrophysiology digital twins with an efficient open source scalable solver on GPU clusters. Sci Rep 16, 9619 (2026). https://doi.org/10.1038/s41598-025-33709-w
Schlüsselwörter: digitaler Herzzwilling, Simulation der Herz-Elektrophysiologie, Purkinje-Leitungssystem, GPU-Computing, personalisierte Kardiologie