Clear Sky Science · de
Androgene dysregulieren die follikuläre extrazelluläre Matrix und erhöhen die pro-fibrotische Genexpression im Maus-Ovar
Warum das für die Frauengesundheit wichtig ist
Viele Frauen mit polyzystischem Ovarialsyndrom (PCOS) haben unregelmäßige Zyklen und Probleme, schwanger zu werden — doch die eigentliche Geschichte spielt sich in der Gewebearchitektur des Ovars ab. Diese Studie nutzt Maus-Ovarien, um zu untersuchen, wie männliche Hormone, sogenannte Androgene, das mikroskopische Stützgerüst um sich entwickelnde Eifollikel umgestalten. Die Arbeit hilft zu erklären, warum Ovarien bei PCOS oft faseriger und steifer erscheinen und wie diese veränderte Umgebung die normale Follikelreifung und den Eisprung beeinträchtigen könnte.
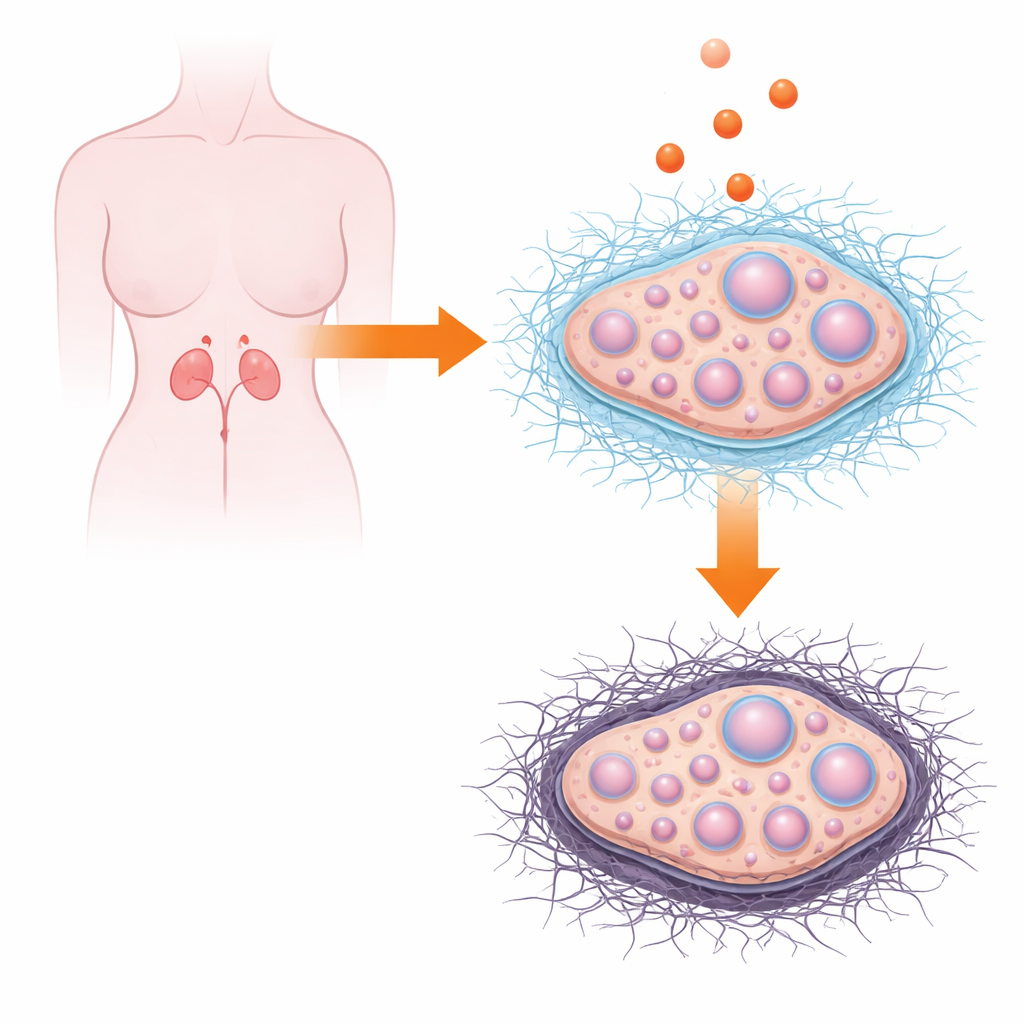
Das verborgene Stütznetz des Ovars
Jedes Organ im Körper ruht auf einem komplexen „molekularen Gerüst“, der extrazellulären Matrix. Im Ovar umgibt dieses Geflecht aus Proteinen und Zuckern die Follikel, die winzigen flüssigkeitsgefüllten Strukturen, die heranreifende Eizellen beherbergen. Die Matrix ist nicht statisch: Sie wird während jedes Zyklus umgebaut, damit Follikel wachsen, Hohlräume bilden und schließlich eine reife Eizelle freisetzen können. Frühere Arbeiten an Frauen mit PCOS zeigen, dass ihre Ovarien häufig vermehrtes Bindegewebe aufweisen und dichter erscheinen, was auf Narbenbildung bzw. Fibrose hindeutet. Die Autoren wollten herausfinden, welche matrixbezogenen Gene und Signalwege im Maus-Ovar vorhanden sind und wie sie reagieren, wenn Follikel im Labor direkt Androgenen ausgesetzt werden.
Die Bausteine im Ovar kartieren
Die Forschenden stellten zunächst ein Panel von Genen zusammen, die strukturelle Matrixproteine, Enzyme, die diese Proteine modifizieren, und Moleküle umfassen, die Zellen helfen, mechanische Kräfte zu spüren und darauf zu reagieren. In Maus-Ovarien bestätigten sie, dass viele dieser Gene in verschiedenen Follikelstadien, im umgebenden Stromagewebe und sogar in den Eizellen selbst aktiv sind. Unter dem Mikroskop bildeten mehrere Schlüsselproteine wie Kollagen, Laminin und eine Form von Aktin ringförmige Schichten um wachsende Follikel, während andere Proteine Zellen mit der Matrix verbanden und Fasern vernetzten. Dieses Muster zeigt, dass das Stütznetz des Ovars sorgfältig organisiert ist, um jeden Follikel einzuschließen, und legt nahe, dass jede Störung dieser Ringe oder des umgebenden Geflechts das Follikelwachstum und die gefühlte Steifigkeit der Umgebung verändern könnte.
Androgene verschieben das Gleichgewicht in Richtung Vernarbung
Als Nächstes isolierte das Team frühe Follikelstadien aus der Maus und kultivierte sie mit oder ohne das potente Androgen Dihydrotestosteron. Wie bereits aus früheren Studien zu erwarten war, wuchsen androgenbehandelte Follikel schneller. Unter dieser Wachstumsbeschleunigung verschob sich jedoch ihre Genaktivität in Richtungen, die auf ein fibrotischeres Ovar hindeuten. Nach einem Tag sank die Aktivität vieler strukturrelevanter Matrixgene, insbesondere von Komponenten der dünnen Basalmembran, die die äußere Begrenzung des Follikels bildet. Nach drei Tagen erholten sich einige Komponenten oder erhöhten sich sogar, darunter Elastin und alpha-glattes Muskelaktin, beides Marker für steifes, narbenähnliches Gewebe. Die Follikel steigerten zudem Gene für Enzyme, die Kollagenfasern stärken oder zuckerreiche Matrix umbauen — konsistent mit einer Verlagerung von einer flexiblen zu einer dichteren, härteren Gewebeumgebung.
Mechanische Signale werden lauter
Die Studie ging auch der Frage nach, wie Follikel mechanische Signale wahrnehmen und umsetzen, wenn ihre Umgebung steifer wird. Androgenbehandelte Follikel zeigten eine erhöhte Aktivität mehrerer zentraler Komponenten des Hippo-Wegs, eines Signalnetzwerks, das auf Gewebespannung reagiert und die Organgröße begrenzt. Abwärts gerichtete Ziele dieses Weges, darunter das connective tissue growth factor und andere matrixassoziierte Signale, waren ebenfalls erhöht, was darauf hindeutet, dass mechanische Botschaften den Zellkern erreichen und Genprogramme verändern. Parallel dazu waren zwei Mitglieder der TGF‑beta-Familie, starke Treiber fibrotischer Antworten in vielen Organen, hochreguliert. Zusammen deuten diese Veränderungen auf eine Rückkopplungsschleife hin, in der Androgene nicht nur die Matrix verändern, sondern auch pro-fibrotische und mechanosensitive Signalwege innerhalb der Follikelzellen verstärken.
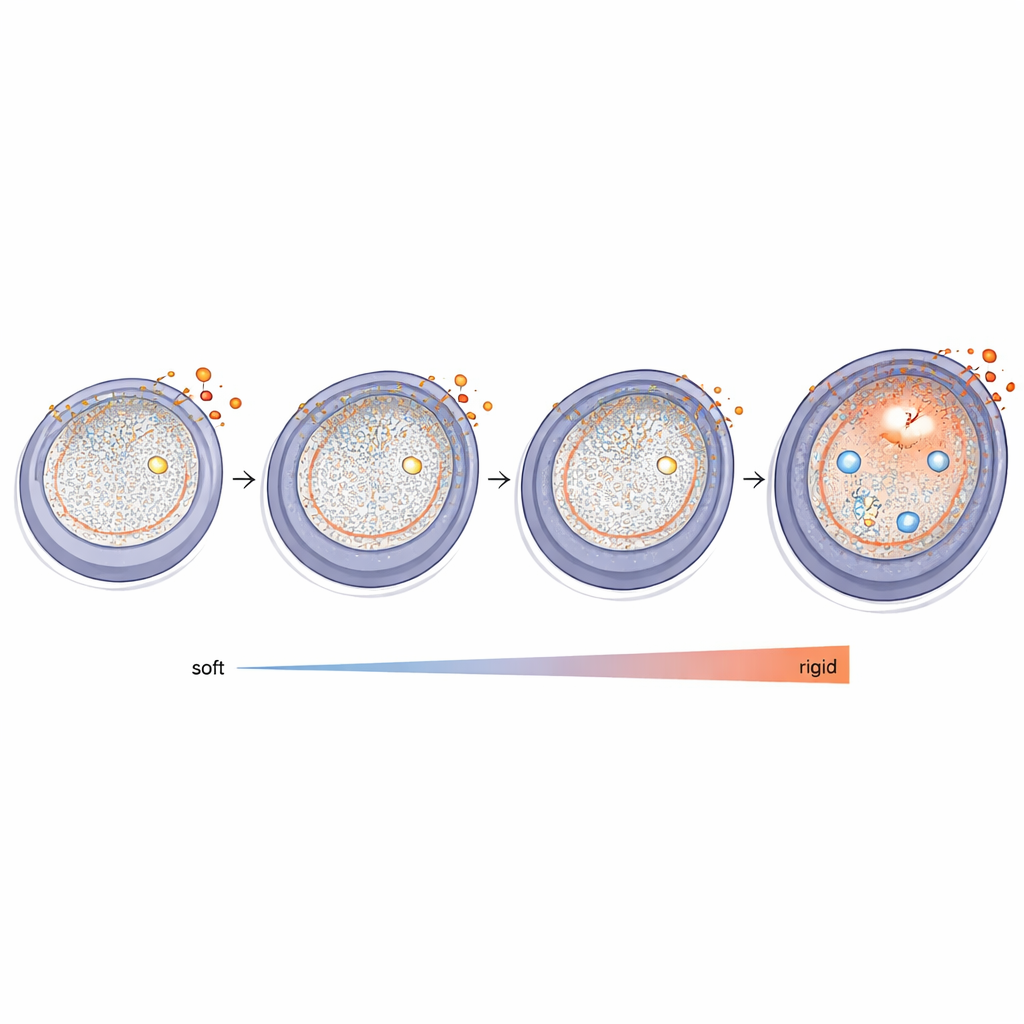
Was das für PCOS bedeutet
Für Nicht-Fachleute ist die Kernbotschaft, dass ein Übermaß an Androgenen Follikel dazu bringen kann, eine steifere, narbenähnliche Hülle aufzubauen, und zelluläre Systeme zu aktivieren, die diese Veränderung verstärken. Im Kontext von PCOS, wo erhöhte Androgenspiegel und verstärkte ovariale Fibrose häufig gemeinsam auftreten, stützen diese Befunde die Vorstellung, dass Hormone aktiv die physische Landschaft des Ovars umgestalten und nicht nur die Hormonspiegel im Blut verändern. Eine steifere Ovarumgebung kann es erschweren, dass Follikel normal heranreifen und Eizellen freigeben, was einige der bei PCOS beobachteten Fruchtbarkeitsprobleme erklären hilft. Das Verständnis dieser Gewebeveränderungen könnte neue therapeutische Ansätze eröffnen, die darauf abzielen, die ovarielle Matrix zu „erweichen“ oder mechanische Signalwege zu modulieren, und somit Behandlungen ergänzen, die sich allein auf Hormonspiegel konzentrieren.
Zitation: Hopkins, T.I.R., Lerner, A., Dunlop, I.E. et al. Androgen dysregulates the follicular extracellular matrix and increases pro-fibrotic gene expression in the mouse ovary. Sci Rep 16, 8974 (2026). https://doi.org/10.1038/s41598-025-32927-6
Schlüsselwörter: polyzystisches Ovarialsyndrom, Androgene, ovariale Fibrose, extrazelluläre Matrix, Follikelentwicklung