Clear Sky Science · de
Auf dem Weg zu tieflern‑basierten Verfahren zur Erkennung und Quantifizierung von intestinaler Metaplasie in digitalisierten Magenbiopsien: eine Vergleichsstudie mit mehreren Experten
Warum das für Ihre Gesundheit wichtig ist
Magenkrebs gehört weltweit zu den tödlichsten Krebserkrankungen, weil er oft zu spät entdeckt wird. Ärztinnen und Ärzte wissen, dass eine bestimmte präkanzeröse Veränderung der Magenschleimhaut, die intestinale Metaplasie genannt wird, Jahre bevor ein Tumor entsteht ein erhöhtes Risiko anzeigt. Heute wird dieses Warnsignal jedoch mit bloßem Auge beurteilt, sodass zwei Expertinnen oder Experten dieselbe Biopsie unterschiedlich einschätzen können. Diese Studie untersucht, ob künstliche Intelligenz diese wichtige Früherkennungsstufe konsistenter und präziser machen kann.
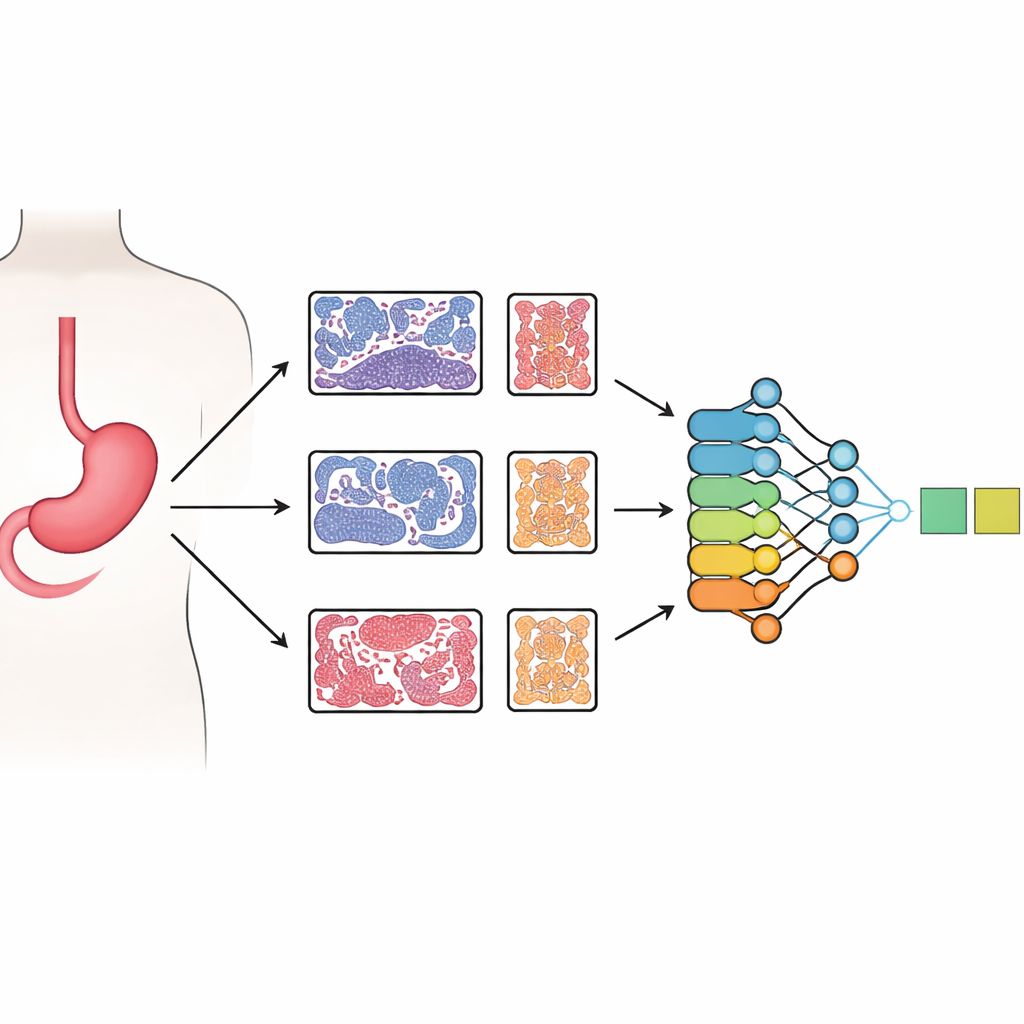
Wie Ärztinnen und Ärzte im Magen nach Auffälligkeiten suchen
Bei der Abklärung möglicher Magenkrankheiten werden aus mehreren standardisierten Stellen im Magen kleine Gewebeproben entnommen und unter dem Mikroskop untersucht. Pathologinnen und Pathologen achten auf Hinweise wie Entzündungen, den Verlust normaler Drüsen und insbesondere auf das Auftreten von darmähnlichen Zellen an Stellen, an denen sie nicht hingehören. Je weiter verbreitet diese Veränderungen sind und je mehr Bereiche des Magens sie betreffen, desto höher wird das geschätzte Risiko eingestuft, später Magenkrebs zu entwickeln. Aktuelle Scoring‑Systeme fassen diese visuellen Eindrücke zu Stadien von sehr niedrig bis sehr hoch zusammen und leiten daraus, wie engmaschig eine Patientin oder ein Patient überwacht werden sollte.
Das Problem der rein menschlichen Beurteilung
Obwohl diese Systeme in Kliniken weit verbreitet sind, basieren sie auf der besten Schätzung einer Pathologin oder eines Pathologen darüber, welcher Anteil des Gewebes verändert ist. Frühere Forschung und die tägliche Erfahrung zeigen, dass selbst gut ausgebildete Expertinnen und Experten sich deutlich in ihren Einschätzungen unterscheiden können. In dieser Studie beurteilten drei Pathologinnen/Pathologen unabhängig voneinander mehr als 200 Biopsiesätze aus dem Magen von kolumbianischen Freiwilligen und Patientinnen/Patienten. Ihre Übereinstimmung reichte nur von gering bis mäßig, was bedeutet, dass derselbe Fall je nach Gutachter unterschiedliche Risikostadien erhalten konnte. Diese Variabilität weckt die Sorge, dass einige Menschen fälschlicherweise beruhigt werden, während andere als höher gefährdet eingestuft werden, als sie tatsächlich sind.
Dem Computer beibringen, Biopsieschnitte zu lesen
Die Forschenden fragten, ob Deep Learning, eine Form künstlicher Intelligenz, die besonders gut darin ist, Muster in Bildern zu erkennen, helfen könnte. Sie digitalisierten pro Person fünf Biopsieproben bei sehr hoher Vergrößerung und nutzten zunächst einen spezialisierten Algorithmus, um glanduläre Strukturen im Gewebe zu lokalisieren, an denen die frühen Veränderungen auftreten. Aus diesen Regionen extrahierten sie Hunderttausende kleiner Bildkacheln. Eine erfahrene Pathologin hatte zuvor die Bereiche abgegrenzt, in denen intestinale Metaplasie vorlag, sodass das Team Kacheln als verändert oder normal kennzeichnen konnte. Mehrere moderne neuronale Netzwerkarchitekturen wurden dann in Etappen trainiert: zunächst durch Lernen an großen bestehenden Bilddatenbanken und anschließend feinabgestimmt an diesen Magenproben, um metaplastische von normalen Kacheln zu unterscheiden.
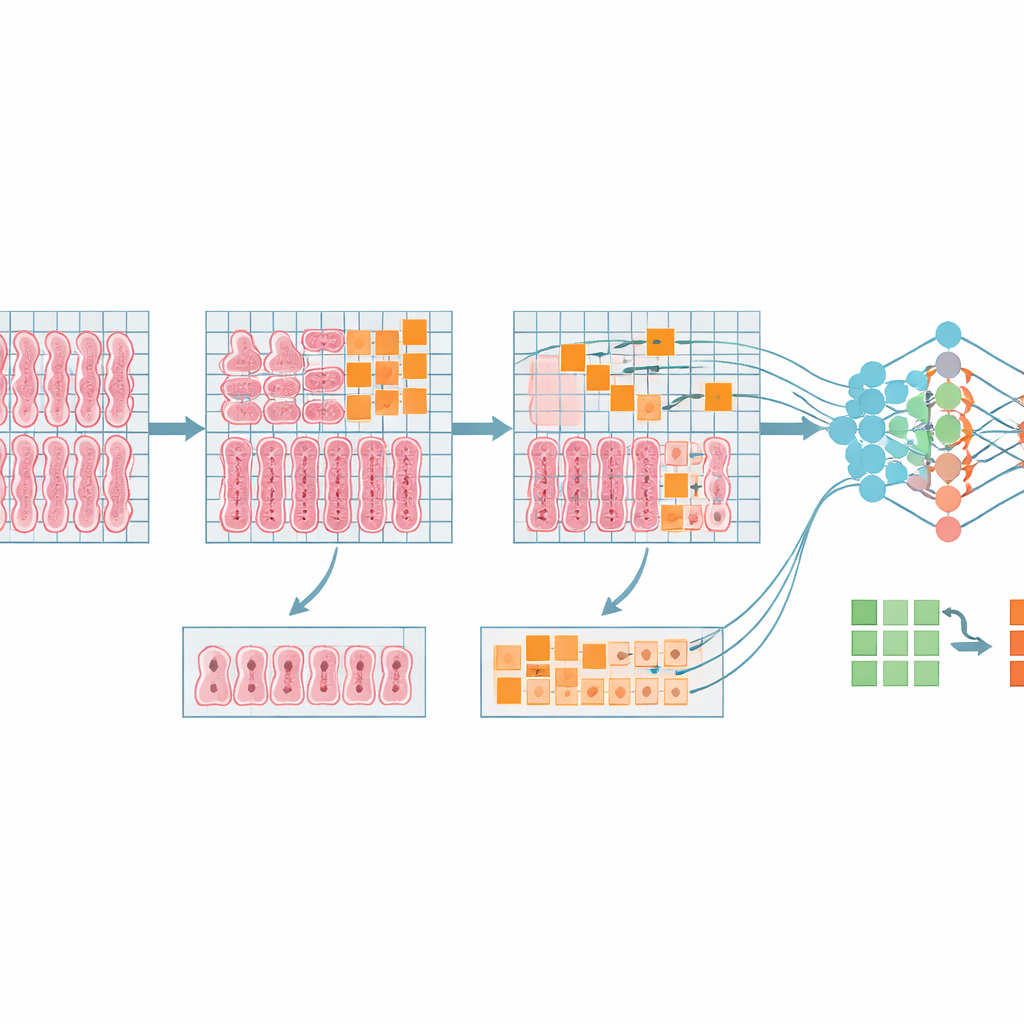
Was der Computer fand und wie das im Vergleich abschneidet
Unter den getesteten Modellen erzielte eine Architektur die besten Ergebnisse: Sie erkannte intestinale Metaplasie in den meisten Kacheln korrekt und erreichte Leistungswerte, die mit denen anderer medizinischer Bildgebungsaufgaben vergleichbar sind. Als die Vorhersagen auf Kachelebene wieder auf die Ganzschnittbilder übertragen wurden, erzeugte das Modell farblich kodierte Karten, die zeigten, wo veränderte Drüsen wahrscheinlich vorkommen. Aus diesen Karten berechnete das Programm automatisch den Prozentsatz veränderten Gewebes an jedem Biopsiestandort und übersetzte diese Prozentsätze in dieselben Risikostadien, die auch menschliche Expertinnen und Experten verwenden. Zwar entsprach das Modell nicht perfekt einer einzelnen Pathologin oder einem einzelnen Pathologen, zeigte jedoch eine starke Korrelation mit ihren Schätzungen und — wichtig — war fallübergreifend konsistenter als die Menschen untereinander.
Was das für die zukünftige Versorgung bedeuten könnte
Die Studie legt nahe, dass Deep‑Learning‑Systeme als verlässliche „zweite Leser“ für Magenbiopsien dienen können und objektive Messungen darüber liefern, wie viel des Gewebes frühe präkanzeröse Veränderungen zeigt. Solche Werkzeuge sollen Pathologinnen und Pathologen nicht ersetzen, sondern ihnen eine belastbare Ausgangsbasis geben, Schätzungen und Meinungsverschiedenheiten verringern und dazu beitragen, dass Patientinnen und Patienten mit tatsächlich höherem Risiko erkannt und angemessen überwacht werden. Mit weiteren Tests in verschiedenen Krankenhäusern und detaillierteren Beschriftungen von Gewebeuntertypen könnte dieser Ansatz schließlich individuellere und sicherere Entscheidungen darüber unterstützen, wer engmaschiger nachuntersucht werden sollte, um Magenkrebs zu verhindern.
Zitation: Cano, F., Caviedes, M., Siabatto, A. et al. Towards deep-learning based detection and quantification of intestinal metaplasia on digitized gastric biopsies: a multi-expert comparative study. Sci Rep 16, 9606 (2026). https://doi.org/10.1038/s41598-025-32737-w
Schlüsselwörter: Magenkrebs, intestinale Metaplasie, Tiefes Lernen, digitale Pathologie, Risikostratifizierung für Krebs