Clear Sky Science · de
Multifunktionale Pektin‑Derivate als Krebsbekämpfer bei kolorektalem Krebs durch Synthese, computergestützte Einsichten und Modulation der NRF2/HO‑1-, HIF‑1α‑ und VEGF/PDGF‑D‑Signalwege
Vom Fruchtfaserstoff zu krebsbekämpfenden Molekülen
Pektin ist ein natürlicher Ballaststoff, der vor allem zum Eindicken von Marmeladen und Gelees bekannt ist, doch dieser alltägliche Küchenbestandteil könnte auch ein stiller Verbündeter im Kampf gegen Krebs sein. Diese Studie untersucht, wie Wissenschaftler die Struktur von Pektin gezielt verändern können, um neue Verbindungen zu erzeugen, die im Labor das Wachstum von kolorektalen Krebszellen verlangsamen, gleichzeitig schädlichen oxidativen Stress mindern und die Blutversorgung, die Tumore zum Wachsen benötigen, unterbrechen.
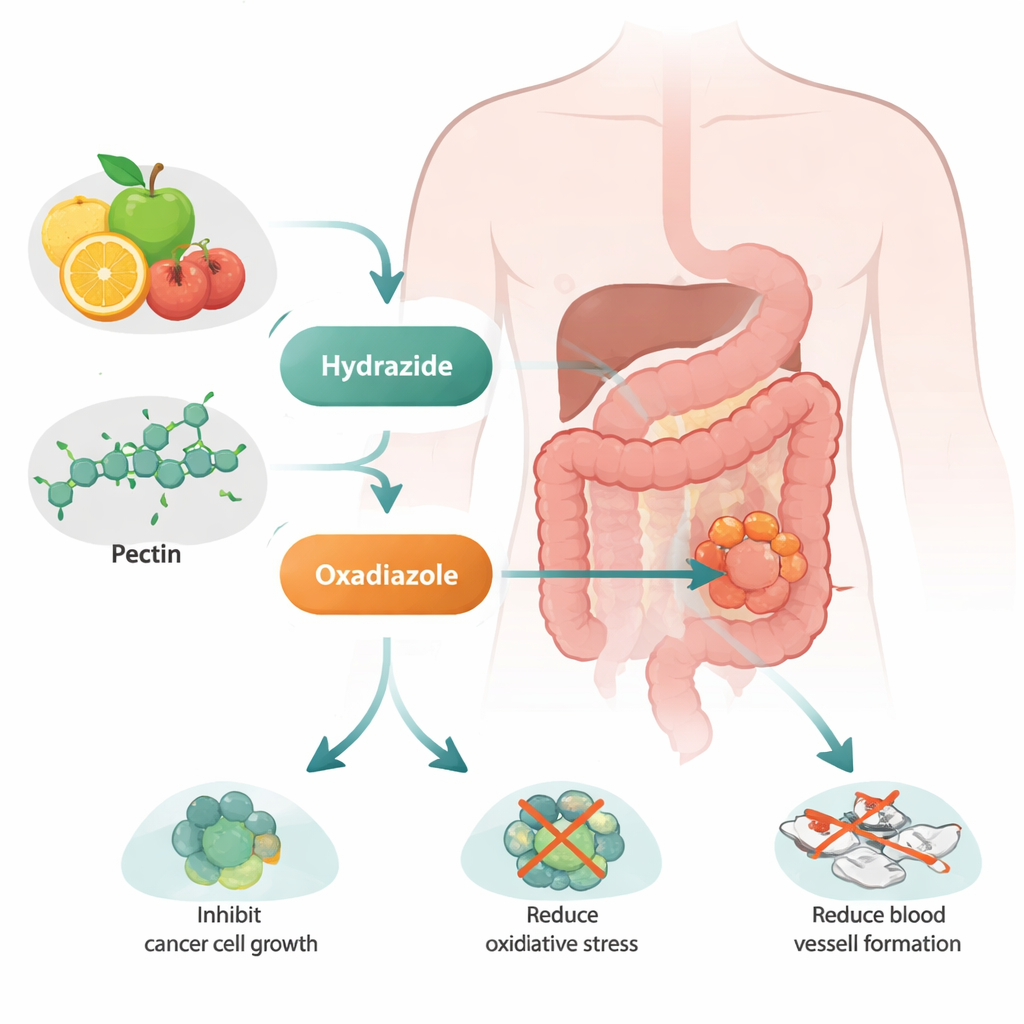
Aus einer verbreiteten Faser wird ein intelligenter Wirkstoffkandidat
Die Forschenden begannen mit gewöhnlichem Pektin, einer pflanzenbasierten Zucker‑Kette, die in vielen Früchten vorkommt. Durch eine Reihe kontrollierter chemischer Schritte verwandelten sie Pektin in zwei neue Formen, „Pektin‑Hydrazid“ und „Pektin‑Oxadiazol“. Obwohl die Namen technisch klingen, ist die Idee einfach: Durch das Anfügen kleiner, Stickstoff‑ und Schwefel‑haltiger Gruppen erhielt das Molekül neue elektronische und strukturelle Eigenschaften, die seine Aktivität gegen Krebszellen erhöhen könnten. Fortgeschrittene Methoden wie Infrarotspektroskopie, Kernspinresonanz, Elektronenmikroskopie und Thermostabilitätstests bestätigten, dass die Reaktionen klappten und dass die neuen Materialien thermisch stabiler waren als das ursprüngliche Pektin.
Erprobung der neuen Verbindungen an Krebszellen
Um zu prüfen, ob diese modifizierten Fasern Krebszellen schädigen können, setzte das Team zwei menschliche Zelllinien — eine aus Leberkrebs und eine aus kolorektalem Krebs — unterschiedlichen Dosen der neuen Verbindungen aus. Sie verwendeten einen farbstoffbasierten Test, der misst, wie viele Zellen nach der Behandlung noch leben. Sowohl Pektin‑Hydrazid als auch Pektin‑Oxadiazol waren wirksamer als unverändertes Pektin darin, das Überleben von kolorektalen Krebszellen (Caco2) zu verringern, wobei Pektin‑Oxadiazol den stärksten Effekt zeigte. Gegenüber Leberkrebszellen waren die Verbindungen weniger potent, zeigten jedoch dennoch messbare Aktivität, was darauf hindeutet, dass die neuen Strukturen besonders vielversprechend für die gezielte Behandlung kolorektaler Tumoren sind.
Reduktion von oxidativem Stress und Abschneiden der Tumorblutversorgung
Krebs entwickelt sich nicht isoliert; er wird durch chemischen Stress und abnormale Signalwege innerhalb von Zellen angetrieben. Die Forschenden konzentrierten sich auf reaktive Sauerstoffspezies (ROS) — hochreaktive Moleküle, die DNA schädigen und Tumorwachstum fördern können — sowie auf Proteine, die Tumoren helfen, sich an Stress anzupassen und neue Blutgefäße zu bilden. Als Caco2‑Zellen mit den neuen Pektin‑Derivaten in aktiven Dosen behandelt wurden, sanken die ROS‑Werte, und auch die Menge eines antioxidativen Enzyms namens HO‑1 nahm ab. Auf genetischer Ebene wurden zentrale "Schaltstellen" wie NRF2 und HIF‑1α sowie die gefäßfördernden Faktoren VEGF und PDGF‑D alle herunterreguliert. Vereinfacht gesagt schädigten die modifizierten Pektine nicht nur die Krebszellen direkt, sondern dämpften auch die inneren Stresssignale und reduzierten die Anweisungen, die Tumoren zur Bildung neuer Blutgefäße geben.
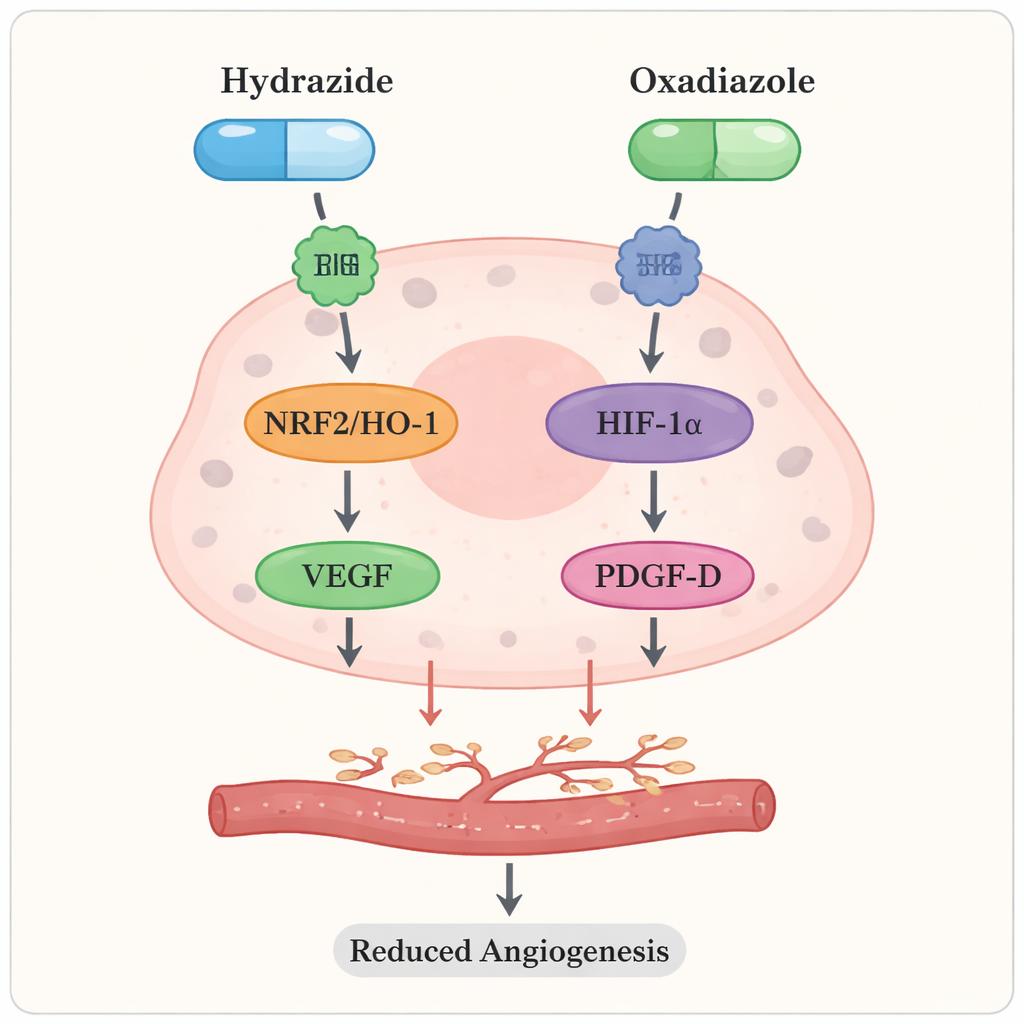
Computermodelle erklären, warum sie wirken
Um tiefer zu verstehen, wie und warum diese Moleküle so aktiv sind, nutzte das Team computergestützte Simulationen. Sie „dockten“ Pektin, Pektin‑Hydrazid und Pektin‑Oxadiazol virtuell an mehrere Proteinstrukturen an, die mit Krebswachstum, Stressantwort und Gefäßbildung verknüpft sind. Über alle diese Ziele hinweg passte Pektin‑Oxadiazol meist am besten und bildete die stärksten und stabilsten Wechselwirkungen. Lange Computersimulationen, die die atomare Bewegung über 100 Nanosekunden verfolgen, stützten dieses Bild: Die Oxadiazol‑Form hielt besonders fest an ihren Zielstrukturen und stabilisierte deren Konformationen stärker als Hydrazid oder unverändertes Pektin. Quantenchemische Berechnungen zeigten außerdem, dass das Einführen von Stickstoff‑ und Schwefelringen die Elektronenverteilung im Molekül veränderte und es reaktiver machte, was starke Bindungen an biologische Partner begünstigt.
Was das für zukünftige Krebstherapien bedeuten könnte
Zusammengefasst zeigt die Studie, dass ein vertrauter Nahrungsfaserstoff zu weit mehr als nur einer darmfreundlichen Zutat gemacht werden kann. Durch die gezielte Umgestaltung der Pektinstruktur schufen die Forschenden neue Verbindungen, die kolorektale Krebszellen auf mehreren Ebenen gleichzeitig angreifen: Sie verlangsamen das Zellwachstum, reduzieren schädlichen oxidativen Stress und schwächen die Signale, die die Bildung neuer Blutgefäße antreiben. Obwohl diese Befunde noch im Zellkultur‑ und Computermodellstadium stehen — und vor einer Anwendung am Menschen in normalen Zellen und Tierversuchen weiter geprüft werden müssen — deuten sie auf Pektin‑Hydrazid und insbesondere Pektin‑Oxadiazol als vielversprechende Ausgangspunkte für sicherere, multifunktionale Wirkstoffe gegen kolorektalen Krebs hin.
Zitation: Elsayed, G.H., Fahim, A.M. Multifunctional pectin derivatives as anticancer agents in colorectal cancer via synthesis, computational insights, and modulation of NRF2/HO-1, HIF-1α, and VEGF/PDGF-D signaling pathways. Sci Rep 16, 6542 (2026). https://doi.org/10.1038/s41598-025-32107-6
Schlüsselwörter: pektin, kolorektaler Krebs, oxidativer Stress, Angiogenese, Wirkstoffdesign