Clear Sky Science · de
Einfluss der Mediumzusammensetzung auf die In-vitro-Ovarkultur von Gurke
Schnellere Wege zu besseren Gurken
Moderne Salatbuffets und Gewürzgurkengläser verdanken Pflanzenzüchtern, die Gurken über viele Generationen hinweg schrittweise verbessern. Diese Studie untersucht eine High‑Tech-Abkürzung: das Kultivieren winziger Gurkenovaren in Glasschalen, um schnell reinlinige Zuchtlinien zu erzeugen. Die Arbeit ist bedeutsam, weil schnellere und präzisere Züchtung schmackhaftere, widerstandsfähigere Gurken bei geringerem Ressourceneinsatz liefern könnte. Gleichzeitig zeigen die Forschenden, wie hartnäckig und unvorhersehbar Pflanzen reagieren können, wenn man sie so behandelt, und offenbaren damit sowohl Chancen als auch Grenzen der aktuellen Techniken.
Warum Züchter an „reinen“ Linien interessiert sind
Pflanzenzüchter wünschen oft Pflanzen, die Merkmale zuverlässig von einer Generation zur nächsten weitergeben. Das erfordert hochgradig uniforme, „reine“ Linien, die normalerweise viele Jahre des Kreuzens und Auslesens brauchen. Eine wirksame Alternative besteht darin, von Zellen auszugehen, die nur einen einfachen Chromosomensatz tragen – sogenannte Haploide – und diesen Satz dann zu verdoppeln, um sofort völlig uniforme Linien zu erhalten. Bei Gurken ist eine der vielversprechendsten Methoden, diesen Umweg auszulösen, die Kultur unbefruchteter Ovarien, also des Blütenteils, der normalerweise zur Frucht würde. Lassen sich diese Ovarien dazu bringen, ganze Pflanzen zu bilden, gewinnen Züchter eine schnelle Pipeline zu neuen Sorten.
Die Laborrezeptur entwerfen
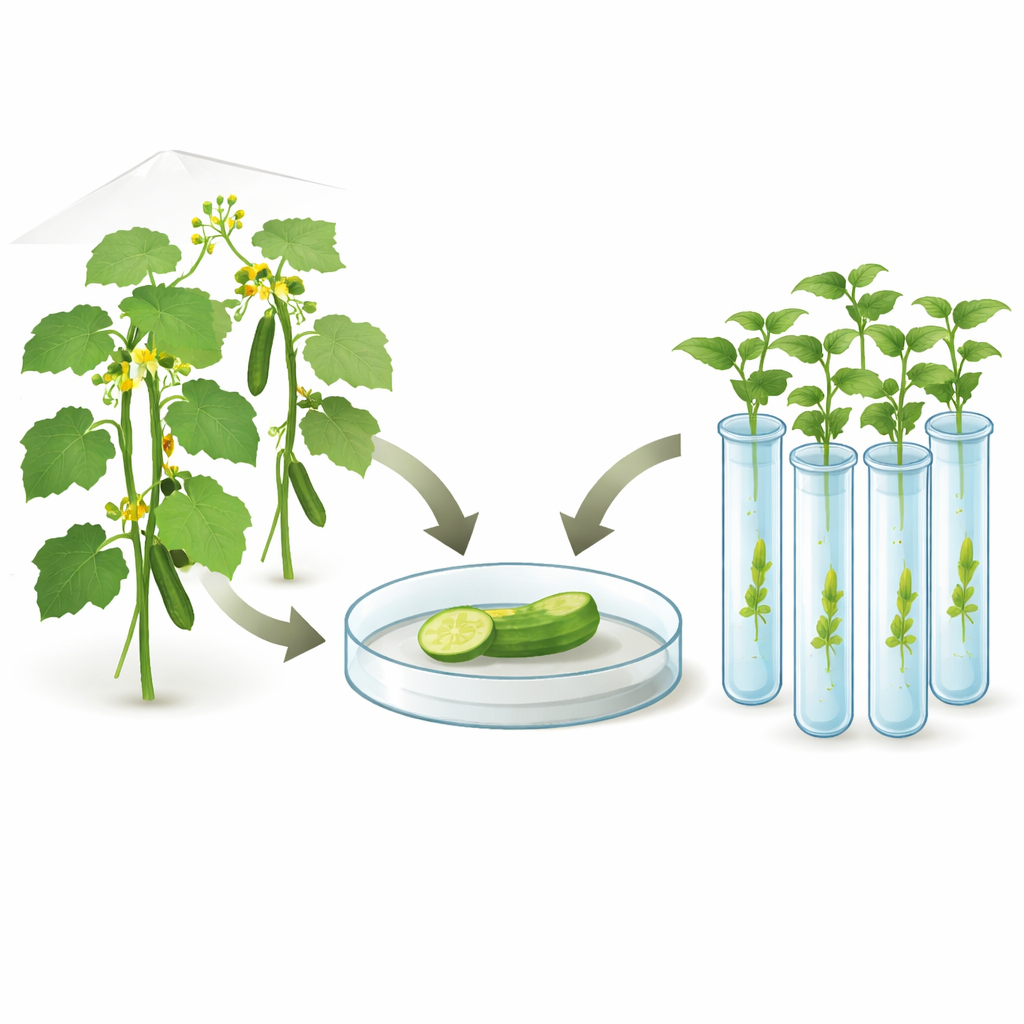
Das Team konzentrierte sich auf vier kommerziell relevante Gurkentypen – Mini-, Lange-, Einlege- und eine offen bestäubte Linie. Sie sammelten sorgfältig junge, unbefruchtete weibliche Blütenknospen und setzten sie einem kurzen Kälteschock aus, um einen Stressreiz zu imitieren, der Zellen manchmal dazu bringen kann, ihren Entwicklungsweg umzustellen. Die Ovarien wurden in dünne Stücke geschnitten und auf eines von vier Ausgangs(Induktions)medien gelegt, die sich hauptsächlich in der Zusammensetzung und Dosis wachstumssteuernder Substanzen unterschieden, und später auf eines von mehreren Folge(Regenerations)medien transferiert. Alle Kulturen wurden unter kontrollierten Licht- und Temperaturbedingungen gehalten, und die Forschenden beobachteten mehrere Schlüsselschritte: geschwollene Samenanlagen, Callus (eine weiche Zellmasse), embryoähnliche Strukturen und schließlich Pflänzchen mit Blättern und Wurzeln.
Welche Gurken und Rezepte am besten reagierten
Die Reaktionen unterschieden sich deutlich sowohl zwischen den Gurkensorten als auch zwischen den Medienrezepturen. Ein bestimmtes Induktionsmedium mit hoher Dosis eines synthetischen Auxins kombiniert mit einer Substanz namens Putrescin stach hervor. Auf diesem Medium zeigte die Einlegelinie „Botanik“ die höchste Rate frühzeitiger Entwicklungen, wobei aus 88 % der kultivierten Stücke embryoähnliche Strukturen hervorgingen. Die Langgurke „Sardes“ und der Mini‑Typ PTK40 reagierten ebenfalls gut, während die offen bestäubte Beith Alpha zurückblieb. Wenn die sich entwickelnden Strukturen auf demselben starken Medium belassen wurden, entwickelten viele weiter Embryonen und embryogenen Callus, besonders bei Botanik, das eine außergewöhnliche Regenerationsfähigkeit zeigte. Regenerationsmedien, die mit einer spezifischen Kombination zweier gängiger Wachstumsregulatoren angereichert waren, erwiesen sich als am erfolgreichsten darin, diese Embryonen und Calli in vollständige Pflänzchen zu überführen.

Ein überraschendes Ergebnis: Noch keine echten Abkürzungen
Um zu prüfen, ob die neuen Pflanzen tatsächlich die erhoffte Abkürzung ermöglichen, analysierten die Forschenden Blattproben von zwanzig regenerierten Gurken mittels Durchflusszytometrie, einer Methode zur Messung des DNA-Gehalts einzelner Zellen. Hätte der Prozess haploide Pflanzen erzeugt, hätten diese nur halb so starkes DNA-Signal gezeigt. Stattdessen erwies sich jede getestete Pflanze als diploid – der normale Chromosomensatz –, was bedeutet, dass die Kulturen sich aus gewöhnlichen Körperzellen regeneriert hatten und nicht aus gametenähnlichen, haploiden Zellen. Einige Pflanzen zeigten zudem unerwünschte Merkmale wie blasse, albinoide Entwicklung. Kurz gesagt: Das Protokoll war sehr gut darin, Pflanzen zu erzeugen, aber nicht darin, die von Züchtern meist gewünschte spezielle Art von Pflanzen für eine schnelle Linienbildung zu produzieren.
Was das für zukünftige Gurken bedeutet
Die Studie zeigt, dass Gurkenovare in viele Embryonen und neue Pflanzen überführt werden können und dass bestimmte Sorten und Medienrezepte viel reaktionsfreudiger sind als andere. Da jedoch alle regenerierten Pflanzen den normalen Chromosomensatz und nicht das reduzierte haploide Niveau hatten, wurde das zentrale Ziel – die Erstellung sofortiger reiner Zuchtlinien – nicht erreicht. Für Erzeuger und Verbraucher bedeutet das, dass der Traum von deutlich schnellerer Gurkenzüchtung über diese Methode weiterhin in Arbeit ist. Die Autoren argumentieren, dass eine bessere Auswahl elterlicher Sorten, eine feinere Abstimmung der Chemikalienmischungen und eine verbesserte Steuerung der Stressbehandlungen nötig sein werden, um das Gleichgewicht zugunsten echter haploider Pflanzen zu verschieben und das volle Potenzial dieser Technologie freizusetzen.
Zitation: Nyirahabimana, F., Erol, M.H., Kaçar, Y.A. et al. Effect of medium composition on in vitro ovary culture of cucumber. Sci Rep 16, 9924 (2026). https://doi.org/10.1038/s41598-025-31636-4
Schlüsselwörter: Gurkenzüchtung, Ovarkultur, haploide Pflanzen, Pflanzengewebekultur, doppelt haploide