Clear Sky Science · de
Umnutzung natürlicher Produkte bei spinozerebellärer Ataxie Typ 3 mittels integrierter Netzwerkpharmakologie und in silico‑Ansätzen
Warum diese Forschung für Patientinnen, Patienten und Familien wichtig ist
Die spinozerebelläre Ataxie Typ 3 (SCA3) ist eine seltene, vererbte Erkrankung des Gehirns, die Betroffenen nach und nach Gleichgewicht, Koordination und Selbstständigkeit raubt. Es gibt bislang weder Heilung noch ein zugelassenes Medikament, das den Krankheitsverlauf stoppt. Diese Studie untersucht, ob bereits in der Natur vorkommende Verbindungen – viele davon aus traditionellen Arzneimitteln – mithilfe leistungsstarker Computerwerkzeuge gezielt „wiederverwendet“ werden können, was einen schnelleren und potenziell sichereren Weg zu neuen Therapien eröffnen könnte.
Suche nach hilfreichen Molekülen in der Natur
Die Forschenden konzentrierten sich auf natürliche Produkte: chemische Verbindungen aus Pflanzen und anderen Organismen, die seit langem eine Quelle moderner Arzneimittel sind. Sie sammelten 15 vielversprechende Naturstoffe, die zuvor in Zell‑ oder Tiermodellen zur Linderung von SCA3‑Merkmalen berichtet worden waren. Über spezialisierte Datenbanken sagten sie voraus, mit welchen menschlichen Proteinen jede Verbindung möglicherweise interagiert, und stellten separat Tausende von Genen zusammen, die mit SCA3 in Verbindung stehen. Durch den Vergleich beider Mengen konzentrierten sie sich auf 239 überlappende Ziele – Proteine, die sowohl an der Erkrankung beteiligt sind als auch potenziell von diesen Naturstoffen beeinflusst werden können. 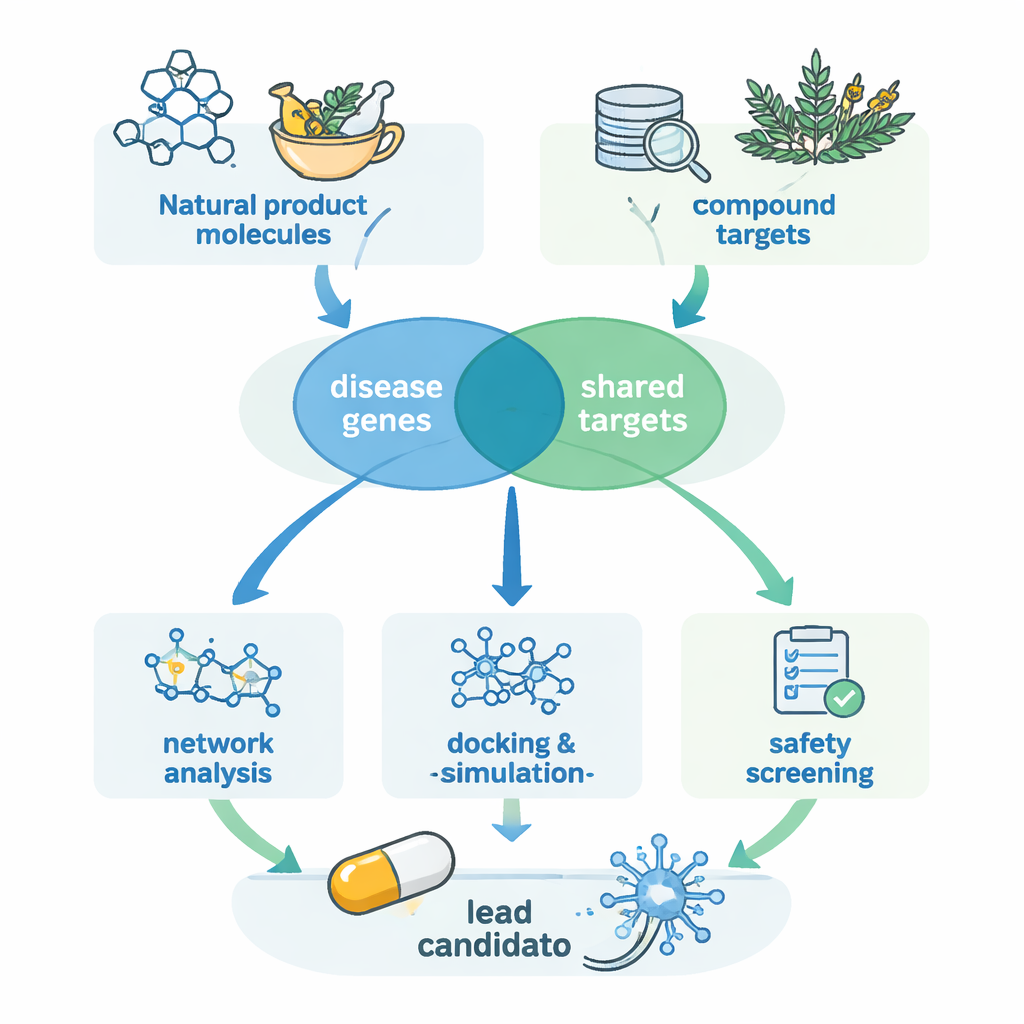
Die Schwachstellen der Krankheit kartieren
Als Nächstes erstellte das Team große „Interaktionskarten“, die zeigen, wie diese 239 Proteine innerhalb der Zelle miteinander kommunizieren. In diesen Karten fungieren einige Proteine wie viel frequentierte Knotenpunkte in einem Verkehrsnetz und verbinden viele Wege gleichzeitig. Zwei solcher Hubs, AKT1 und TP53, stachen als besonders zentral hervor. Die Forschenden untersuchten daraufhin, welche zellulären Signalwege – also verknüpfte biochemische Reaktionsketten – am stärksten betroffen sind. Ein Signalweg, bekannt als MAPK‑Signalgebung, erwies sich als besonders wichtig und ist bereits für seine Rolle beim Überleben von Nervenzellen, Stressreaktionen und Degeneration anerkannt. Viele der natürlichen Verbindungen schienen diesen Weg zu beeinflussen, was auf eine gemeinsame Route hindeutet, über die sie Neuronen in SCA3 schützen könnten.
Crocin wird (virtuell) genau unter die Lupe genommen
Unter den untersuchten Molekülen zeigte Crocin – ein leuchtend orangefarbener Farbstoff aus Safran – die stärkste vorhergesagte Bindung an sowohl AKT1 als auch TP53. Um dies genauer zu verstehen, nutzte das Team computergestützte Docking‑Verfahren, bei dem eine virtuelle Kopie jeder Verbindung in ein 3D‑Modell des Proteins eingefügt wird, ähnlich wie das Ausprobieren von Schlüsseln in einem Schloss. Crocin „passte“ zu AKT1 und TP53 besser als ein Referenz‑Versuchsmedikament namens Troriluzol, bildete stabilere Kontakte und stärkere Wechselwirkungen. Die Wissenschaftler führten anschließend lange Molekulardynamik‑Simulationen durch, die nachahmen, wie sich Atome im Laufe der Zeit in einer wässrigen, körperähnlichen Umgebung bewegen. Diese Simulationen zeigten, dass Protein–Crocin‑Komplexe stabil blieben, viele Wasserstoffbrücken bildeten und in energiefreundliche, gleichgewichtsnahe Konformationen übergingen – Eigenschaften, die auf eine starke und verlässliche Interaktion hindeuten.
Wie das Nervenzellen schützen könnte
AKT1 und TP53 entscheiden mit darüber, ob eine gestresste Nervenzelle sich erholt oder stirbt. Bei SCA3 stören fehlerhafte Formen des Ataxin‑3‑Proteins Signalnetzwerke, an denen beide dieser Schlüsselregulatoren beteiligt sind, und verschieben so das Gleichgewicht in Richtung Zellschädigung und -verlust. Die Computermodelle legen nahe, dass Crocin an AKT1 in Regionen bindet, die für dessen Aktivität wichtig sind, und an TP53 im DNA‑Bindungsbereich, wodurch das Verhalten dieser Proteine subtil verändert werden könnte. Frühere Laborstudien in anderen Modellen von Hirnerkrankungen zeigen, dass Crocin oxidativen Stress reduzieren, Entzündungen dämpfen, Mitochondrien stabilisieren (die Energiezentralen der Zelle) und den programmierten Zelltod modulieren kann. Zusammengenommen stützen die neuen Simulationen die Idee, dass Crocin dazu beitragen könnte, das Gleichgewicht zwischen Überleben und Tod in von SCA3 betroffenen Neuronen wiederherzustellen.
Von Computer‑Vorhersagen zu realen Therapien
Obwohl das vorhergesagte Sicherheitsprofil von Crocin günstig erscheint und sein Verhalten in Simulationen ermutigend ist, befindet sich diese Arbeit weiterhin auf der Ebene von Computermodellen. Die Studie testet Crocin nicht direkt bei Menschen mit SCA3. Vielmehr liefert sie eine detaillierte Roadmap, die Crocin als starken Kandidaten für weiterführende Labor‑ und Tierstudien und schließlich sorgfältig geplante klinische Studien ausweist. 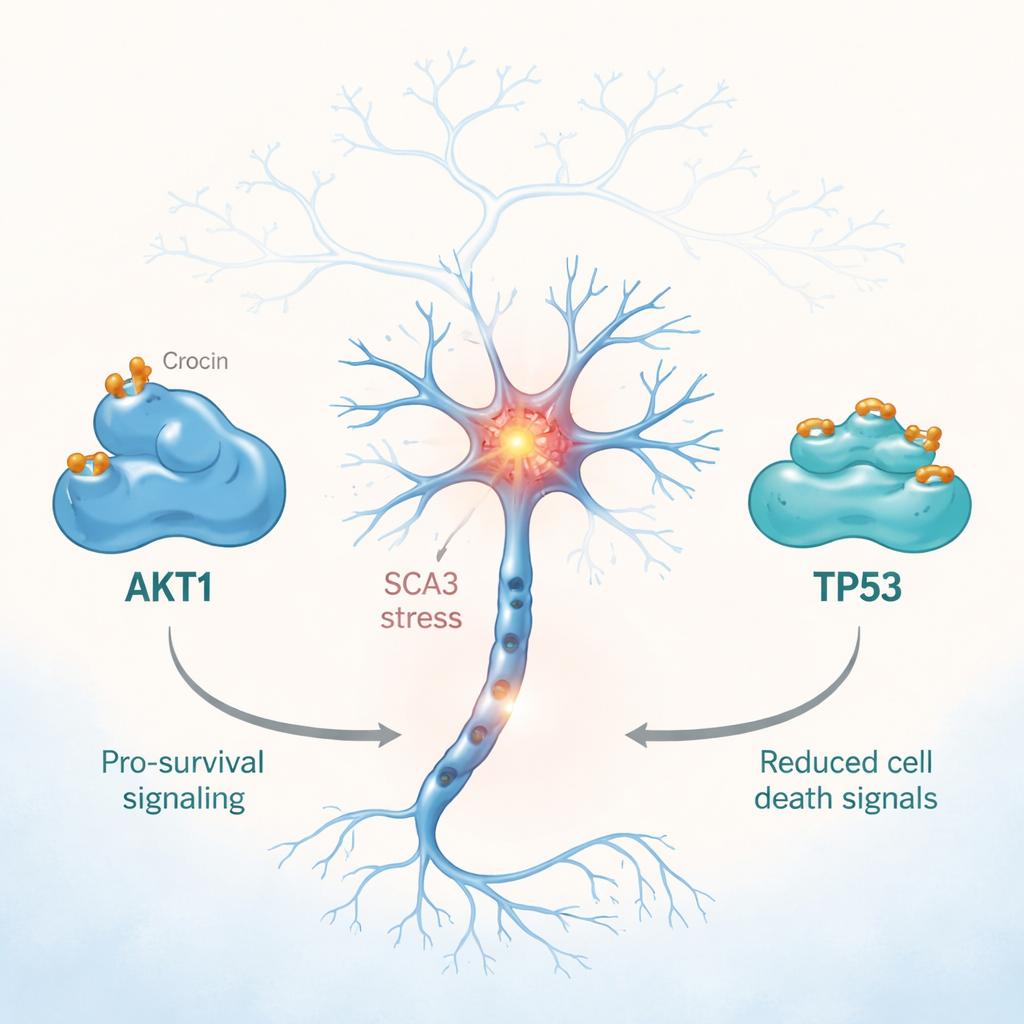
Zitation: Roney, M., Mohd Hisam, N.S., Uddin, M. et al. Repurposing of natural products for spinocerebellar ataxia type 3 using integrated network pharmacology and in silico approaches. Sci Rep 16, 7332 (2026). https://doi.org/10.1038/s41598-025-30652-8
Schlüsselwörter: spinozerebelläre Ataxie Typ 3, natürliche Produkte, Drug‑Repurposing, Crocin, Neurodegeneration