Clear Sky Science · de
In vivo-Visualisierung der extrazellulären Adenosindynamik im Herzen und deren pharmakologische Modulation in Zebrafisch-Modellen von Herzinsuffizienz
Warum diese Geschichte vom Fischherz wichtig ist
Herzinsuffizienz bleibt eine der häufigsten Todesursachen weltweit, und viele Patientinnen und Patienten verschlechtern sich trotz der besten verfügbaren Medikamente. Forschende wissen, dass gestresste Herzmuskelzellen chemische „Alarm‑Signale“ in ihre Umgebung abgeben, doch war es schwierig, diese Signale in einem schlagenden Herzen direkt zu beobachten. Diese Studie nutzt transparente Zebrafische, deren winzige Herzen zentrale Merkmale menschlicher Herzen nachbilden, um diese Gefahrensignale in Echtzeit zu beobachten und eine neue Methode zu testen, sie zu dämpfen.
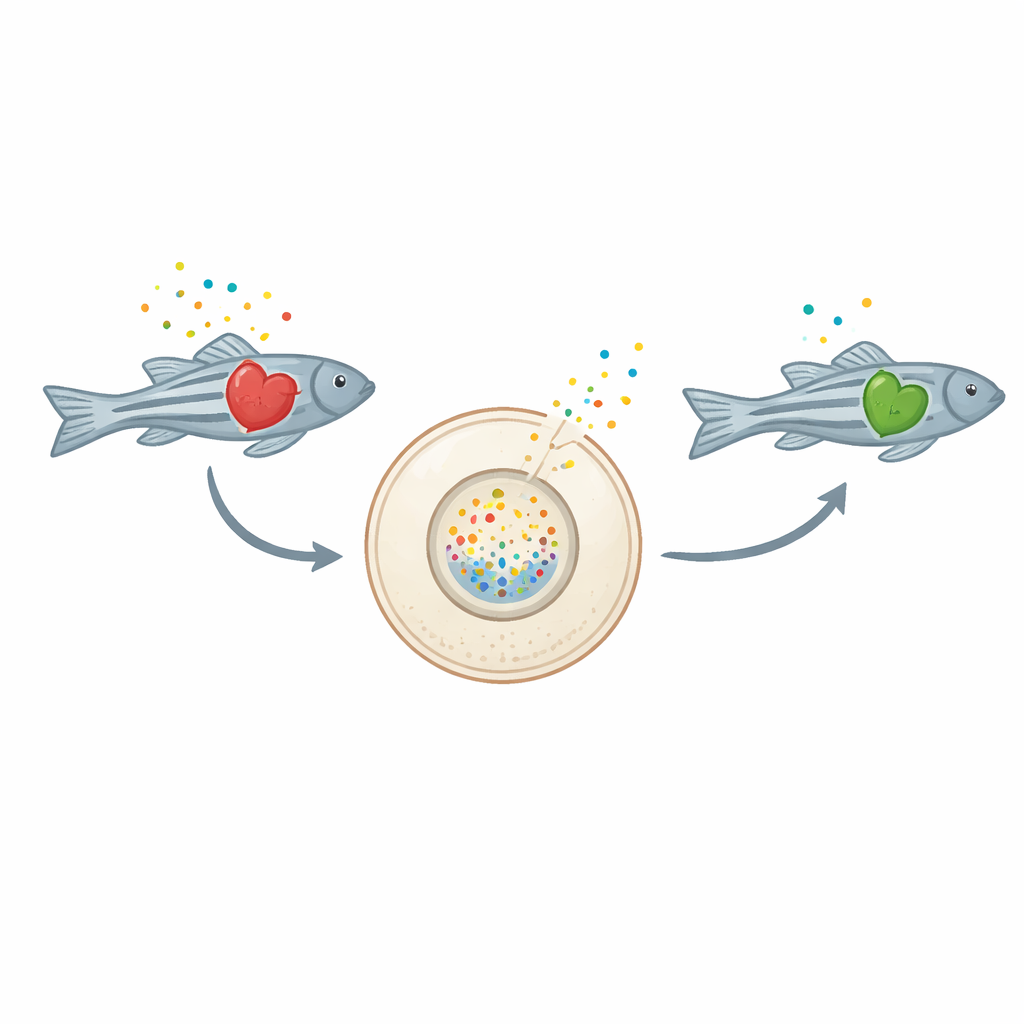
Signale aus einem kämpfenden Herzen
Wenn Herzmuskelzellen verletzt sind, geben sie energietragende Moleküle wie ATP und dessen Abbauprodukt Adenosin in den extrazellulären Raum frei. Außerhalb der Zelle wirken diese Moleküle nicht mehr als Brennstoff, sondern wie dringliche Botschaften, die Entzündungsreaktionen anheizen können. Bei chronischer Herzinsuffizienz kann diese Entzündungsantwort überaktiv werden und das Herz weiter schädigen. Bislang fehlten jedoch direkte in vivo‑Nachweise dafür, wie sich diese Moleküle über die Zeit in einem versagenden Herzen verhalten.
Zebrafische als lebende chemische Kameras
Das Team erzeugte Zebrafische, deren Herzmuskelzellen an ihrer Oberfläche ein spezielles fluoreszierendes Sensorprotein namens GRABAdo produzieren. Wenn sich Adenosin außerhalb der Zellen anreichert, leuchtet dieser Sensor heller grün und verwandelt damit jedes winzige Herz in eine eigene Live‑Chemiekamera. Die Forschenden lösten Herzinsuffizienz in den Zebrafischen mit Terfenadin aus, einem Medikament, das den Herzrhythmus stört und die Pumpleistung schwächt. Während die Tiere deutliche Anzeichen von Herzinsuffizienz entwickelten — langsamere Herzschläge, vergrößerte und schwächere Ventrikel, Flüssigkeitsansammlungen um das Herz und reduzierte Schwimmleistung — hellten die Herzsensoren auf und zeigten einen ausgeprägten Anstieg des extrazellulären Adenosins. Chemische Messungen ganzer Larven bestätigten, dass die Gesamtadenosinspiegel in den versagenden Herzen erhöht waren.
Das Auslassventil blockieren
Die Forschenden fragten als Nächstes, ob das Abschwächen dieser Gefahrensignale das Herz schützen kann. Sie konzentrierten sich auf VNUT, einen Transporter, der ATP in kleine zelluläre Vesikel verpackt, um es außerhalb der Zelle freizusetzen. Durch den Einsatz von Clodronat, einem Wirkstoff, der VNUT blockiert, reduzierten sie die ATP‑Freisetzung und indirekt die Adenosinakkumulation um Herzmuskelzellen. In zebrafischbasierten Modellen mit medikamentös ausgelöster Herzinsuffizienz bewahrte die VNUT‑Hemmung die Herzform, verringerte die Kammervergrößerung, verbesserte Herzfrequenz und Pumpleistung und hielt den Blutfluss besser aufrecht. Der aufleuchtende Adenosinsensor wurde schwächer, was zeigte, dass weniger des Gefahrensignals außerhalb der Zellen vorhanden war. Ähnliche schützende Effekte traten auch bei erwachsenen Zebrafischen mit einer akut schnell verlaufenden Form der Herzinsuffizienz auf.
Mehrere schützende Hebel greifen ineinander
Herzinsuffizienz betrifft mehr als einen Signalweg, daher prüften die Forschenden, wie VNUT‑Blockade mit anderen bekannten Akteuren interagiert. Medikamente, die bestimmte Adenosin‑ und ATP‑Rezeptoren blockieren, sowie eine Verbindung, die passive ATP‑Leckage durch Membrankanäle einschränkt, halfen jeweils den Zebrafischherzen. In Kombination mit VNUT‑Hemmung ergaben viele dieser Behandlungen additive Vorteile, was darauf hindeutet, dass das Absenken der Purinsignalgebung an mehreren Stellen besonders wirksam sein kann. VNUT‑Hemmung half außerdem, das Kalziumgleichgewicht in Herzmuskelzellen wiederherzustellen — essenziell für einen normalen Herzschlag — und verringerte sowohl den Zelltod als auch die Aktivität von Genen, die mit Entzündungen verbunden sind. Zusammengenommen zeichnen diese Ergebnisse VNUT als einen zentralen Schalter, der ATP‑Freisetzung, Entzündung, gestörtes Kalziumhandling und fortschreitende Herzschädigung verknüpft.
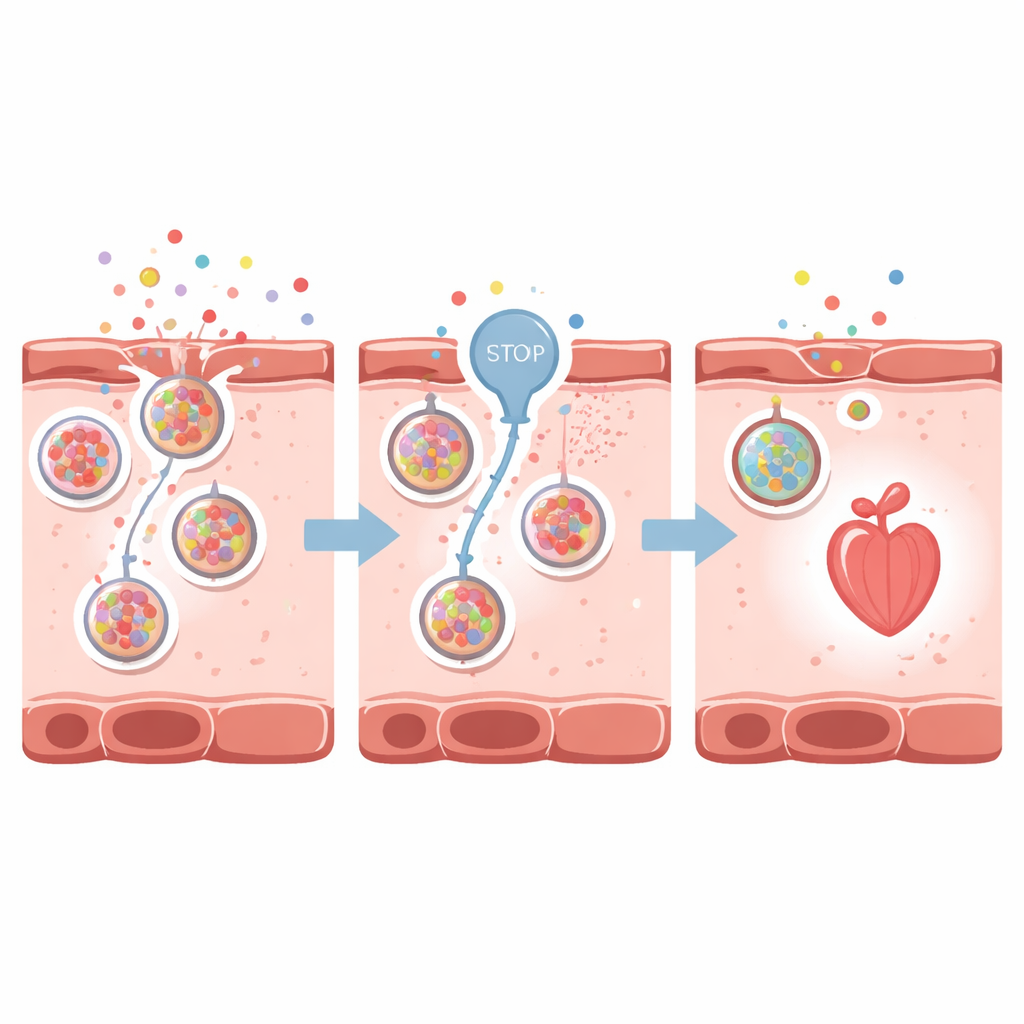
Aus dem Fischbecken zu künftigen Therapien
Für Nicht‑Spezialisten ist die Kernbotschaft, dass die Studie ein chemisches Stresssignal sichtbar macht, das in versagenden Herzen ansteigt, und zeigt, dass das Blockieren seiner Freisetzung die Herzfunktion in einem lebenden Tier schützen kann. Auch wenn Zebrafischherzen einfacher aufgebaut sind als menschliche Herzen, teilen sie genügend biologische Gemeinsamkeiten, um als leistungsfähige Testplattform für neue Ideen zu dienen. Indem VNUT als vielversprechendes Ziel an der Schnittstelle von Entzündung und elektrischer Instabilität aufgezeigt wird, legt diese Arbeit nahe, dass künftige Therapien der Herzinsuffizienz mehr leisten könnten als nur die Durchblutung zu unterstützen — sie könnten aktiv schädliche zelluläre Kommunikationsprozesse beruhigen, die das Herz in Richtung Versagen treiben.
Zitation: Phurpa, P., Apolinario, M.E.C., Umeda, R. et al. In vivo visualization of cardiac extracellular adenosine dynamics and its pharmacological modulation in zebrafish heart failure models. Sci Rep 16, 8220 (2026). https://doi.org/10.1038/s41598-025-30303-y
Schlüsselwörter: Herzinsuffizienz, Adenosin-Signalgebung, Zebrafisch-Modell, Entzündung, kardialer Schutz