Clear Sky Science · de
Telomerische G‑Quadruplex‑Zwischenstufen aufgedeckt durch komplexe Markov‑Netzwerkanalyse
Verborgene Knoten an den Enden unserer DNA
An den Spitzen unserer Chromosomen sitzen Schutzkappen, die Telomere genannt werden und oft mit den Kunststoffenden von Schnürsenkeln verglichen werden. In diesen Bereichen kann sich die DNA zu ungewöhnlichen viersträngigen Knoten zusammenfalten, den sogenannten G‑Quadruplexen. Diese winzigen Strukturen können beeinflussen, wie Gene reguliert werden und wie Zellen altern oder krebsartig werden. Diese Studie gewährt einen Blick hinter die Kulissen, wie ein solcher Knoten schrittweise aufgeht: mithilfe detaillierter Computersimulationen und fortschrittlicher Datenanalyse werden kurzlebige Formen sichtbar, die in Experimenten kaum zu fassen sind.
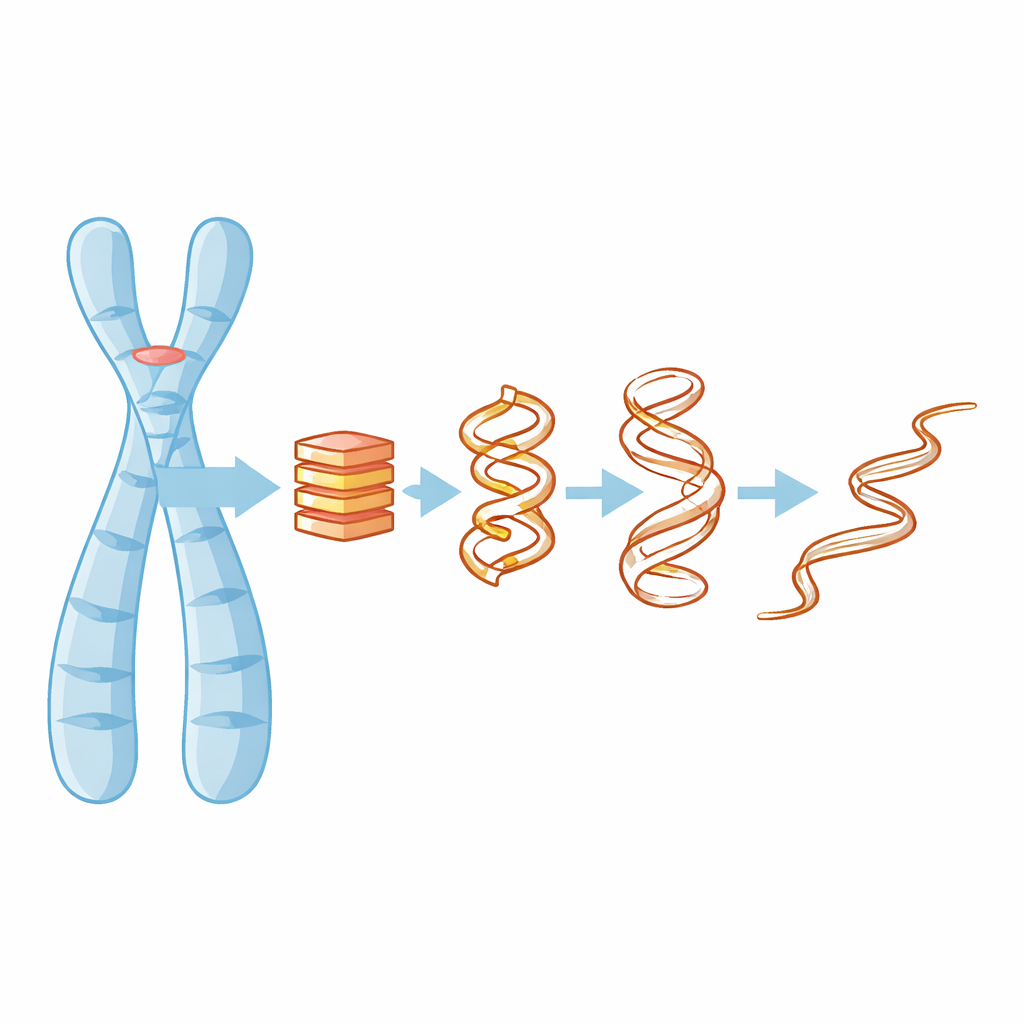
Warum viersträngige DNA‑Knoten wichtig sind
Die meisten von uns lernen, dass DNA eine Doppelhelix ist, doch in guaninreichen Abschnitten — etwa in Telomeren — kann sich das Molekül zu kompakten viersträngigen Stapeln falten, den G‑Quadruplexen. Diese Stapel werden von planaren Schichten aus Guaninbasen zusammengehalten und von kleineren positiv geladenen Ionen, wie Kalium, stabilisiert, die in der Mitte sitzen und alles zusammenkleben. Wenn ein G‑Quadruplex entsteht oder zerfällt, kann er Teile des Genoms blockieren oder freilegen, was Genaktivität, DNA‑Replikation und sogar die Art und Weise beeinflusst, wie Krebszellen ihre Telomere erhalten. Zu verstehen, wie diese Strukturen ihre Form verlieren, ist daher entscheidend, um sie gezielt mit Wirkstoffen anzugreifen oder vorherzusagen, wann sie versagen könnten.
Beobachtung, wie ein molekularer Knoten sich löst
Die Forscher konzentrierten sich auf einen menschlichen telomerischen G‑Quadruplex, bei dem vier Segmente eines einzelnen DNA‑Strangs parallel aneinandergereiht sind und zu einer kompakten Säule gestapelt werden. Sie verwendeten all‑atom Molekulardynamik‑Simulationen — virtuelle Experimente, die die Bewegung jedes einzelnen Atoms verfolgen — und erhitzten acht Kopien dieser Struktur bis in die Nähe ihres Schmelzpunktes. Um das System an verschiedene Konformationen heranzuführen, nutzten sie eine Strategie namens Replica Exchange, bei der Simulationen bei unterschiedlichen Temperaturen gelegentlich Konfigurationen tauschen. In sieben der acht Fälle blieb der G‑Quadruplex zusammen; in einem faltete er sich vollständig auf. Dieses seltene Entfaltungsereignis wurde zur detaillierten Fallstudie und zeigte nicht nur Vorher und Nachher, sondern eine ganze Abfolge von Zwischenformen auf dem Weg.
Die entscheidende Rolle winziger Ionen
Ein zentrales Ergebnis ist, dass die kleinen Ionen im Inneren des G‑Quadruplex wie Schlüsselpunkte wirken. Solange mindestens ein Ion zwischen den Guaninlagen verbleibt, bleibt die Struktur weitgehend intakt — vielleicht etwas gelockert, aber dennoch erkennbar. Wenn jedoch beide Ionen den zentralen Kanal verlassen, destabilisiert der Stapel sich rasch. Die Guaninlagen verformen sich, einzelne Stränge lösen sich ab und die gesamte DNA wird länger und flexibler. Andere simulierte Moleküle, die nur ein Ion verloren hatten, gelangten in wackelige, aber teilweise geordnete Zustände, was darauf hindeutet, dass ein vollständiges Auflösen den Verlust beider stabilisierender Ionen erfordert — ein Hinweis darauf, warum manche G‑Quadruplexe in der Zelle so hartnäckig stabil sind.
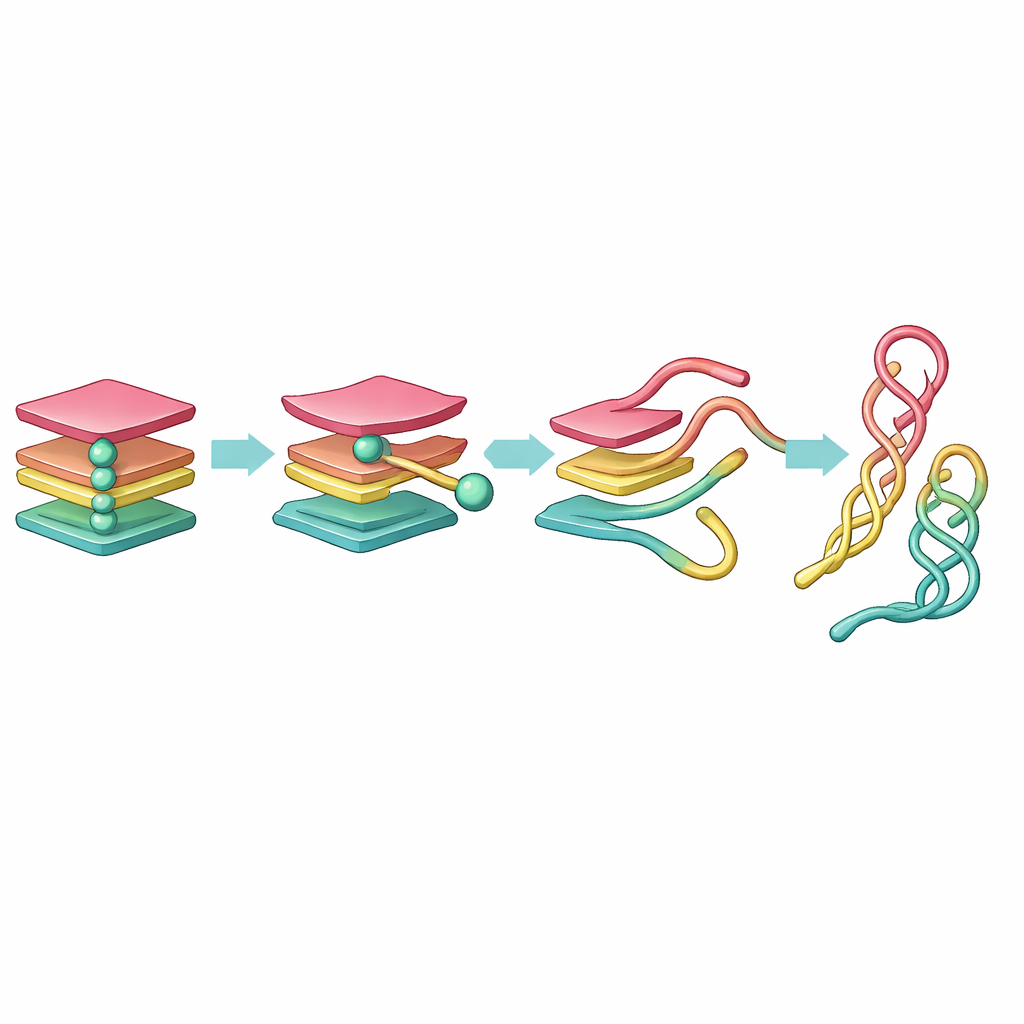
Verborgene Wegmarken auf der Reise entdecken
Die Rohdaten der Simulation lieferten eine enorme Datenmenge, die mit bloßem Auge viel zu komplex war, um interpretiert zu werden. Um das zu bändigen, vereinfachtet das Team zunächst die DNA, indem jede Base als einzelne Kugel repräsentiert wurde, und nutzte dann mathematische Werkzeuge, um die Bewegung auf nur wenige Schlüsselkoordinaten zu reduzieren. Sie wandten zwei Methoden an: Principal Component Analysis (PCA), die Richtungen größter Bewegung hervorhebt, und time‑independent Component Analysis (tICA), die langsame, langlebige Veränderungen filtert, die echte strukturelle Umstellungen kennzeichnen. Aus diesen reduzierten Koordinaten bauten sie sogenannte konformationelle Markov‑Netzwerke, in denen jeder Knoten eine typische DNA‑Gestalt darstellt und Verbindungen zeigen, wie das Molekül von einer Form zur nächsten springt.
Eine bevorzugte Route vom Knoten zum losen Strang
Diese Netzwerkansicht enthüllte einen klaren Entfaltungsweg. Ausgehend von einem vollständig gefalteten G‑Quadruplex löst sich zunächst ein Strang und bildet einen dreisträngigen „Triplex“‑Zustand. Dieser Triplex reorganisiert sich dann zu einem zweisträngigen „Haarnadel“‑(hairpin) und einer Reihe benachbarter loser Stränge. Die Haarnadel und eine verwandte „Kreuz‑Haarnadel“‑Anordnung erweisen sich als überraschend langlebig und fungieren als stabile Wegmarken auf dem Weg von einem engen Knoten zu einer entspannteren DNA‑Konfiguration. Während PCA diesen Verlauf in viele ähnlich aussehende Zustände zerlegte, destillierte tICA ihn in eine kleine Anzahl eindeutiger, kinetisch bedeutender Schritte und zeigte, dass triplexähnliche Formen kurzlebig sind, während hairpinähnliche Formen viel länger verweilen.
Was das für Biologie und Medizin bedeutet
Für Nichtfachleute lautet die Kernbotschaft: Telomerische G‑Quadruplexe springen nicht einfach von gefaltet zu entfaltet. Stattdessen schmelzen sie durch eine Folge kurzlebiger und längerlebiger Formen, wobei winzige Ionen als Torwächter der Stabilität agieren. Die Simulationen deuten darauf hin, dass dreisträngige Zwischenstufen flüchtig sind, während zweisträngige Haarnadeln und kreuzförmige Formen stabilere Ruhepunkte darstellen. Da diese Zwischenzustände auch in umgekehrter, faltender Richtung auftreten können, dürften sie eine Schlüsselrolle dabei spielen, wie G‑Quadruplexe entstehen, sich verändern und mit potenziellen Wirkstoffen interagieren. Die Kartierung dieser verborgenen Gestaltenlandschaft bringt Wissenschaftler dem Entwurf von Molekülen näher, die diese DNA‑Knoten gezielt stabilisieren oder destabilisieren — ein möglicher Schritt im Kampf gegen Krebs und andere Krankheiten.
Zitation: Sáinz-Agost, A., Falo, F. & Fiasconaro, A. Telomeric G-quadruplex intermediates unveiled by complex Markov network analysis. Sci Rep 16, 8308 (2026). https://doi.org/10.1038/s41598-025-29993-1
Schlüsselwörter: G‑Quadruplex, Telomer‑DNA, Molekulardynamik, Proteinfrei‑DNA‑Faltung, Krebstherapeutika