Clear Sky Science · de
Identifikation und Bewertung tumor-pyroptose-assoziierter Antigene zur Gestaltung eines Impfstoffkandidaten gegen Lungenkrebs
Warum diese Forschung für Menschen mit Lungenkrebs wichtig ist
Lungenkrebs bleibt die tödlichste Krebsform weltweit, und die aktuellen Behandlungen — Operation, Chemotherapie, Strahlentherapie und Immuntherapie — lassen viele Patientinnen und Patienten weiterhin ohne langfristige Optionen. Diese Studie verfolgt eine ganz andere Idee: einen therapeutischen Impfstoff, der nicht der Infektionsprävention dient, sondern das Immunsystem trainieren soll, Lungen Tumore besser zu erkennen und anzugreifen. Mithilfe fortschrittlicher Computermodelle entwerfen und prüfen die Autorinnen und Autoren vollständig in silico ein proteinbasiertes Vakzin, das Moleküle anvisiert, die mit einer feurigen Form des Tumorzelltods, der Pyroptose, verbunden sind, und eröffnet damit einen neuen Weg für präzisere und langlebigere Lungenkrebsbehandlungen.
Schalten des Zelltods als Krebsziel nutzen
Anstatt klassische Krebsmarker in den Mittelpunkt zu stellen, wählten die Forschenden vier Proteine — CARD8, NAIP, NLRP1 und NLRP3 — die an der Pyroptose beteiligt sind, einer explosionsartigen Form des programmierten Zelltods, die das Immunsystem alarmieren kann. Diese Proteine sind an der Immunregulation aktiv und wurden mit besserem Überleben bei Lungenadenokarzinom in Verbindung gebracht, was sie zu attraktiven Zielen macht. Das Team argumentierte, dass, wenn das Immunsystem gezielt darauf trainiert werden könnte, kleine Abschnitte dieser Proteine auf Tumorzellen zu erkennen, dies nicht nur direkt krebserregende Zellen zerstören, sondern auch breitere Immunantworten gegen den Tumor verstärken könnte.
Ein maßgeschneidertes Impfstoffmolekül Stück für Stück aufbauen
Mit Hilfe von Immunoinformatik-Tools durchforsteten die Autorinnen und Autoren die vier Proteine, um kurze Abschnitte, sogenannte Epitope, zu identifizieren, die voraussichtlich sowohl von T- als auch von B-Zellen erkannt werden. Aus Hunderten von Kandidaten wählten sie 15 Epitope aus, die in der Erkennbarkeit durch Immunzellen besonders hoch bewertet wurden und gleichzeitig als nicht-toxisch und nicht-allergen vorhergesagt waren. Diese Bestandteile wurden anschließend zu einem einzigen langen Protein verknüpft, verbunden durch sorgfältig ausgewählte molekulare "Spacer", damit jedes Epitop zugänglich bleibt. Um die Immunantwort zu verstärken, fügten sie drei bekannte immunstimulierende Komponenten bakterieller Proteine als Adjuvantien hinzu. Das resultierende Konstrukt, 678 Aminosäuren lang, wurde als stabil, löslich und stark antigen prädiziert — Eigenschaften, die für einen realen Impfstoff wichtig sind.
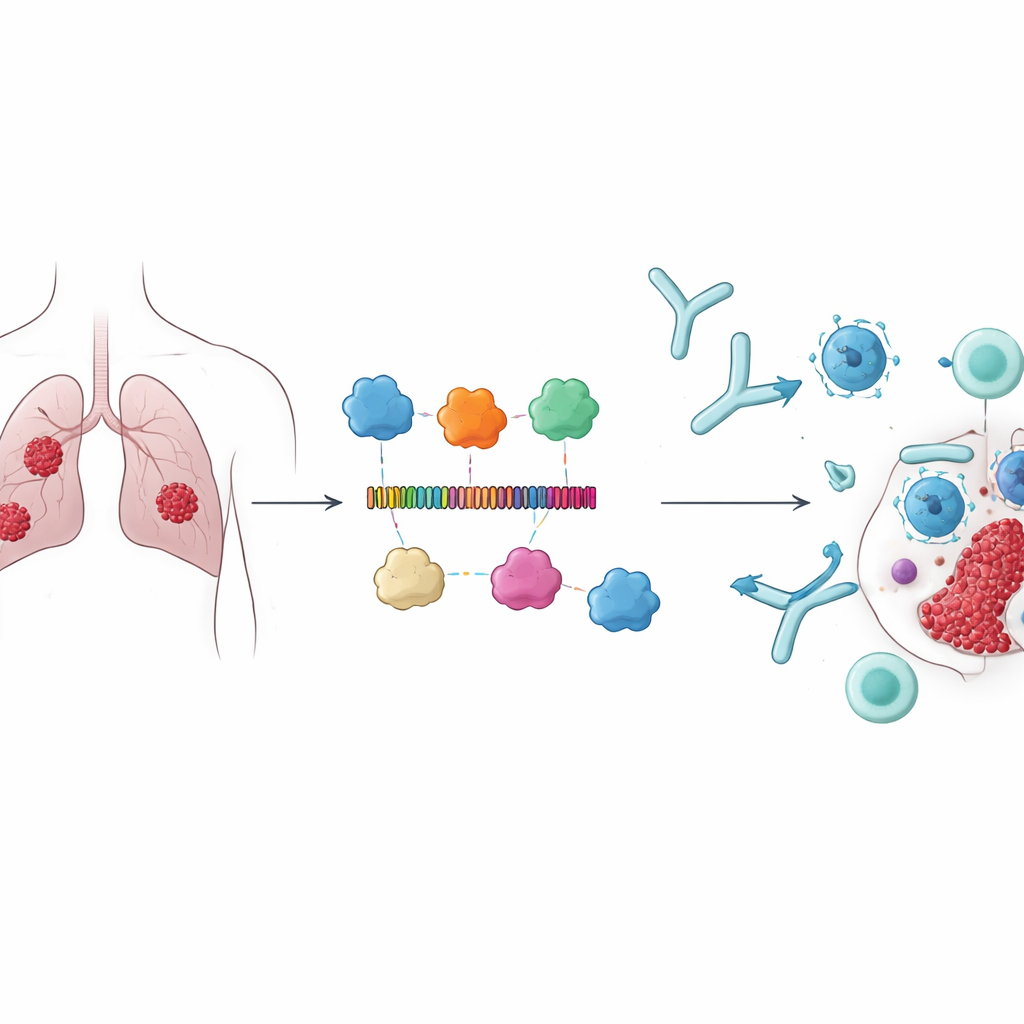
Form und Robustheit des Designs am Computer prüfen
Da die Wirksamkeit eines Impfstoffs stark von seiner dreidimensionalen Form abhängt, erstellte das Team 3D-Modelle des neuen Proteins mit mehreren modernen Strukturvorhersageprogrammen. Sie verfeinerten diese Modelle wiederholt und überprüften deren Qualität mit gängigen strukturellen Benchmarks und entschieden sich für eine finale Version, die strenge Kriterien für realistische Proteingeometrie und Stabilität erfüllte. Außerdem kartierten sie die Oberflächenbereiche, die für Antikörper am leichtesten zugänglich wären, und entwarfen neue interne "Brücken" in Form von Disulfid-Bindungen, die das Protein weiter versteifen und stabilisieren sollen. Um zu simulieren, wie sich der Impfstoff in der wässrigen Umgebung des Körpers verhalten würde, führten sie detaillierte Molekulardynamik-Simulationen über 100 Nanosekunden in zehn unabhängigen Läufen durch. Während dieser Simulationen blieb das Modellprotein kompakt und strukturell stabil, was darauf hindeutet, dass es seine beabsichtigte Form unter realen Bedingungen beibehalten würde.
Simulation der Immunantwort
Die Forschenden fragten anschließend, ob ihr Impfstoffprinzip mit den zentralen "Alarm"-Sensoren des Immunsystems kommunizieren könnte — den Toll-like-Rezeptoren (TLRs), die auf oder in Immunzellen sitzen. Computerbasiertes Docking zeigte starke, stabile Interaktionen zwischen dem Impfstoff und sechs verschiedenen menschlichen TLRs, insbesondere TLR5 und TLR8, die dafür bekannt sind, mächtige Immunreaktionen einzuleiten. Danach simulierten sie einen gesamten Impfplan mithilfe von Immunsystem-Modellierungssoftware. In diesen virtuellen Tests führten drei Impfstoffdosen zu einer raschen Beseitigung des simulierten Antigens, starken Antikörperwellen (insbesondere IgM und IgG1) und einem Anstieg langlebiger Gedächtnis-B- und T-Helferzellen. Wichtige Signalstoffe wie Interferon-Gamma und Interleukine stiegen ebenfalls an, was auf die Aktivierung sowohl der angeborenen als auch der adaptiven Immunantwort hindeutet — genau die ausgewogene Reaktion, die für einen Tumorschutz gewünscht ist.
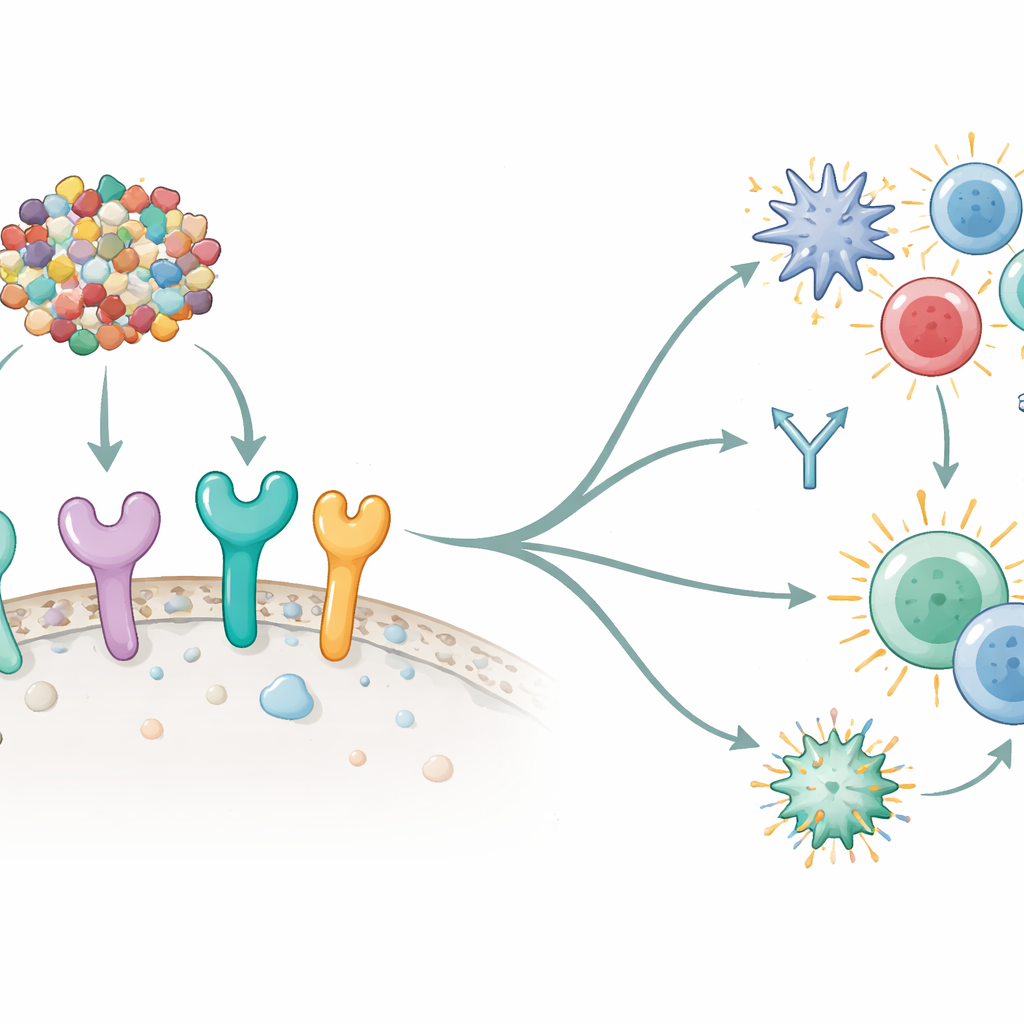
Vorbereitung für die Produktion in der realen Welt
Um vom Konzept zur Laborprüfung zu gelangen, prüfte das Team, ob der Impfstoff effizient in einem gängigen bakteriellen Produktionsorganismus, Escherichia coli, hergestellt werden könnte. Durch Anpassung des genetischen Codes für den Impfstoff, ohne das Protein selbst zu verändern, erreichten sie ein ideales Muster für bakterielle Proteinproduktion und eine ausgewogene chemische Zusammensetzung der DNA. Anschließend führten sie einen virtuellen Klonierschritt durch und setzten das optimierte Gen in ein standardmäßiges Laborplasimid ein, das für die Proteinexpression verwendet wird. Diese Schritte deuten darauf hin, dass der Impfstoff bei Überführung ins Labor voraussichtlich in großem Maßstab für experimentelle Studien produziert werden könnte.
Was das für die künftige Krebsbehandlung bedeuten könnte
Kurz gesagt liefert diese Arbeit einen umfassend computergeprüften Entwurf für einen Lungenkrebs-Impfstoff, der Proteine anvisiert, die mit einer besonders entzündlichen Form des Tumorzelltods verbunden sind. Das Design erscheint in Simulationen sicher, stabil und in der Lage, die Immunabwehr stark zu aktivieren, mit einer breiten prognostizierten Abdeckung in menschlichen Populationen. Da es sich derzeit noch um einen digitalen Prototyp handelt, der erst in Zell-, Tier- und schließlich Humanstudien validiert werden muss, zeigt die Studie dennoch, wie moderne rechnergestützte Werkzeuge Jahre von Versuchsreihen in ein integriertes Design bündeln können. Wenn zukünftige Experimente diese Vorhersagen bestätigen, könnte ein solcher Impfstoff eines Tages bestehende Behandlungen ergänzen und dabei helfen, das körpereigene Immunsystem von Patientinnen und Patienten zuverlässiger Tumoren erkennen und bekämpfen zu lassen.
Zitation: Nguyen, T.L., Kim, H. Identification and evaluation of tumor pyroptosis-associated antigens for design a vaccine candidate against lung cancer. Sci Rep 16, 9559 (2026). https://doi.org/10.1038/s41598-024-84792-4
Schlüsselwörter: Lungenkrebs-Impfstoff, Pyroptose, Multi-Epitop-Immuntherapie, Computergestützte Impfstoffentwicklung, tumorbedingte Immunantwort