Clear Sky Science · de
Ein Einzelzell-Transkriptomdatensatz zur Darstellung von traumatischer Hirnverletzung und NeuroD1-basierter Gentherapie bei Mäusen
Warum Hirnverletzungen uns alle betreffen
Jedes Jahr erleiden Millionen Menschen Kopfverletzungen durch Stürze, Unfälle, Sport oder Kampfhandlungen. Diese traumatischen Hirnverletzungen können bleibende Probleme mit Gedächtnis, Bewegung und Stimmung verursachen, und die heutigen Behandlungen dämpfen meist nur Symptome, statt das Gehirn wirklich zu reparieren. Diese Studie untersucht einen vielversprechenden genetischen Ansatz bei Mäusen, der darauf abzielt, nicht nur den Schaden zu begrenzen, sondern dem Gehirn zu helfen, sich von innen heraus wiederaufzubauen. Die Veränderungen werden Zelle für Zelle kartiert, um eine öffentliche Ressource für künftige Therapien zu schaffen.
Blick ins verletzte Gehirn
Bei einer Gehirnverletzung handelt es sich nicht einfach um eine Blutergussbildung wie bei einem Muskel. Eine komplexe Kaskade entfaltet sich: Nervenzellen sterben, der Blutfluss wird gestört und Stützzellen wie Astrozyten sowie Immunzellen strömen herbei. Astrozyten versorgen normalerweise Neuronen und halten die neuronale Kommunikation im Gleichgewicht, können nach einem Trauma jedoch eine dichte Narbe bilden und lang anhaltende Entzündungen antreiben. Die Autoren verwendeten eine kontrollierte Stichwunde im Kortex von Mäusen, um bestimmte Formen eindringender Hirnverletzungen zu simulieren, und untersuchten dann, wie sich jede wichtige Zellart im betroffenen Gewebe im Zeitverlauf verhielt. Sie nutzten eine Methode namens Einzelzell-RNA-Sequenzierung, die abliest, welche Gene in Zehntausenden einzelner Zellen aktiv sind, und so eine detaillierte Bestandsaufnahme der Veränderungen der zellulären Gemeinschaft im Gehirn nach der Verletzung erlaubt.
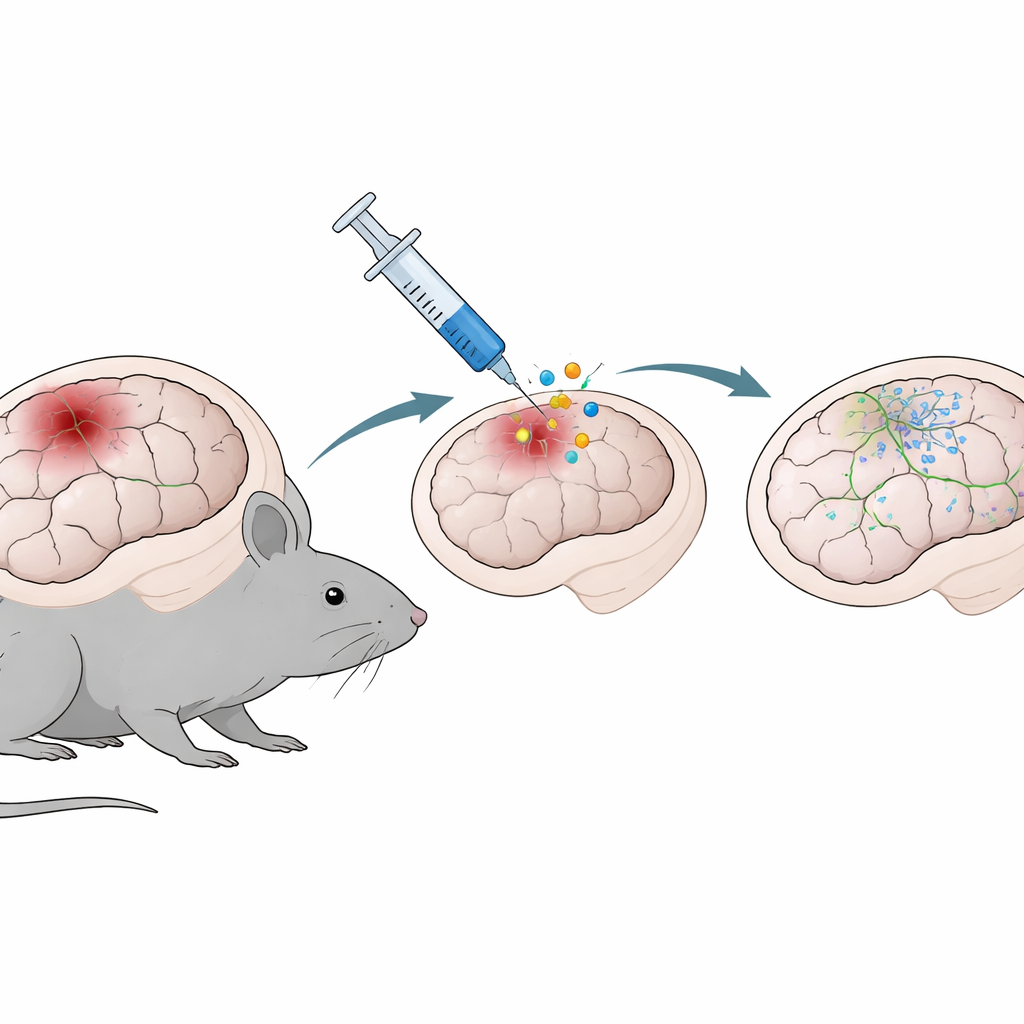
Eine Gentherapie, die Stützzellen im Gehirn rekrutiert
Da Astrozyten zahlreich sind und direkt an der Verletzungsstelle vorhanden sind, sind sie attraktive Ziele für Reparaturstrategien. Das Team testete eine auf NeuroD1 basierende Gentherapie — ein Gen, das Zellen in Richtung eines neuronähnlichen Zustands treiben kann. Mithilfe eines harmlosen viralen Vektors, drei Tage nach der Verletzung in das beschädigte kortikale Areal injiziert, brachten sie entweder ein neutrales Markergen (GFP) oder NeuroD1 in Astrozyten ein. Bei Untersuchungen eine und zwei Wochen später zeigten Mäuse, die NeuroD1 erhalten hatten, kleinere Gewebshöhlen an den Schadensstellen und weniger aktivierte Immunzellen, sogenannte Mikroglia, rund um die Läsion. Mit anderen Worten: Die Therapie verringerte nicht nur sichtbaren Strukturverlust, sondern beruhigte auch die lokale Entzündungsreaktion.
Zelltypen einzeln nachverfolgen
Um zu verstehen, was diesen Verbesserungen zugrunde lag, verglichen die Forschenden drei Gruppen kortikaler Proben: gesunde Mäuse, verletzte Mäuse mit dem Kontrollvirus und verletzte Mäuse mit dem NeuroD1-Virus. Sie sequenzierten insgesamt mehr als 97.000 einzelne Zellen und gruppierten sie anhand ihrer Genaktivitätsmuster in vertraute Gehirnbewohner, darunter Neuronen, Astrozyten, Oligodendrozyten (die Nervenfasern isolieren), Mikroglia sowie Zellen, die Blutgefäße und Hirnhöhlen auskleiden. Allein die Verletzung verschob dieses Gleichgewicht hin zu mehr Astrozyten und Mikroglia sowie zu weniger Neuronen und myelinisierenden Zellen — ein Spiegelbild von Narbenbildung und Entzündung. Unter NeuroD1-Behandlung begann sich diese Verzerrung umzukehren: Anteile von Neuronen, Oligodendrozyten und Plexus-choroideus-Epithelzellen stiegen, während Astrozyten und Mikroglia im verletzten Bereich weniger dominant wurden.
Die verborgene Arbeit der Astrozyten-Subtypen
Astrozyten erwiesen sich nicht als eine einheitliche Population. Durch eine separate Nachanalyse identifizierte das Team sieben unterschiedliche Astrozyten-Subcluster, jeweils mit eigenen Gen-Signaturen und Verhaltensmustern in den drei Bedingungen. Einige Subcluster waren im gesunden Gewebe häufig, verschwanden aber nach der Verletzung nahezu, während andere erst nach dem Trauma auftauchten. In verletzten Gehirnen, die mit dem Kontrollvirus behandelt wurden, schalteten mehrere Astrozytengruppen Programme ein, die am Aufbau und Umbau von Synapsen — den Verbindungsstellen zwischen Neuronen — beteiligt sind, während Gene, die mit der Energieproduktion in Mitochondrien verbunden sind, herunterreguliert wurden. Dieses Muster deutet darauf hin, dass Astrozyten nach der Verletzung an ungewöhnlichen Verbindungsumbauten arbeiteten, dabei aber mit verringerter metabolischer Leistung auskommen mussten.
Wie NeuroD1 Zellenergie und Verschaltungen wieder ausbalanciert
Die NeuroD1-Behandlung formte diese Astrozyten-Subcluster in eine andere Richtung. In mehreren verletzungsassoziierten Astrozytengruppen wurden Gene, die mit mitochondrialer Aktivität, zellulärer Atmung und allgemeinem Energiestoffwechsel zusammenhängen, wieder hochgefahren, während Gene, die mit übermäßiger Synapsenbildung und Myelinumbau verbunden sind, abgeschwächt wurden. Anders gesagt schien NeuroD1 die Energiemaschinen dieser Zellen wiederherzustellen und überstürzte Umbauversuche zu dämpfen, die sonst zur Funktionsstörung beitragen könnten. Manche Astrozyten-Subtypen, die nach der Verletzung stark zugenommen hatten, schrumpften unter NeuroD1, während andere, die mit gesünderen Funktionen assoziiert sind, zunahmen. Diese feingliedrigen Verschiebungen liefern Hinweise darauf, welche Astrozytenzustände schädlich sind und welche die Reparatur unterstützen könnten.
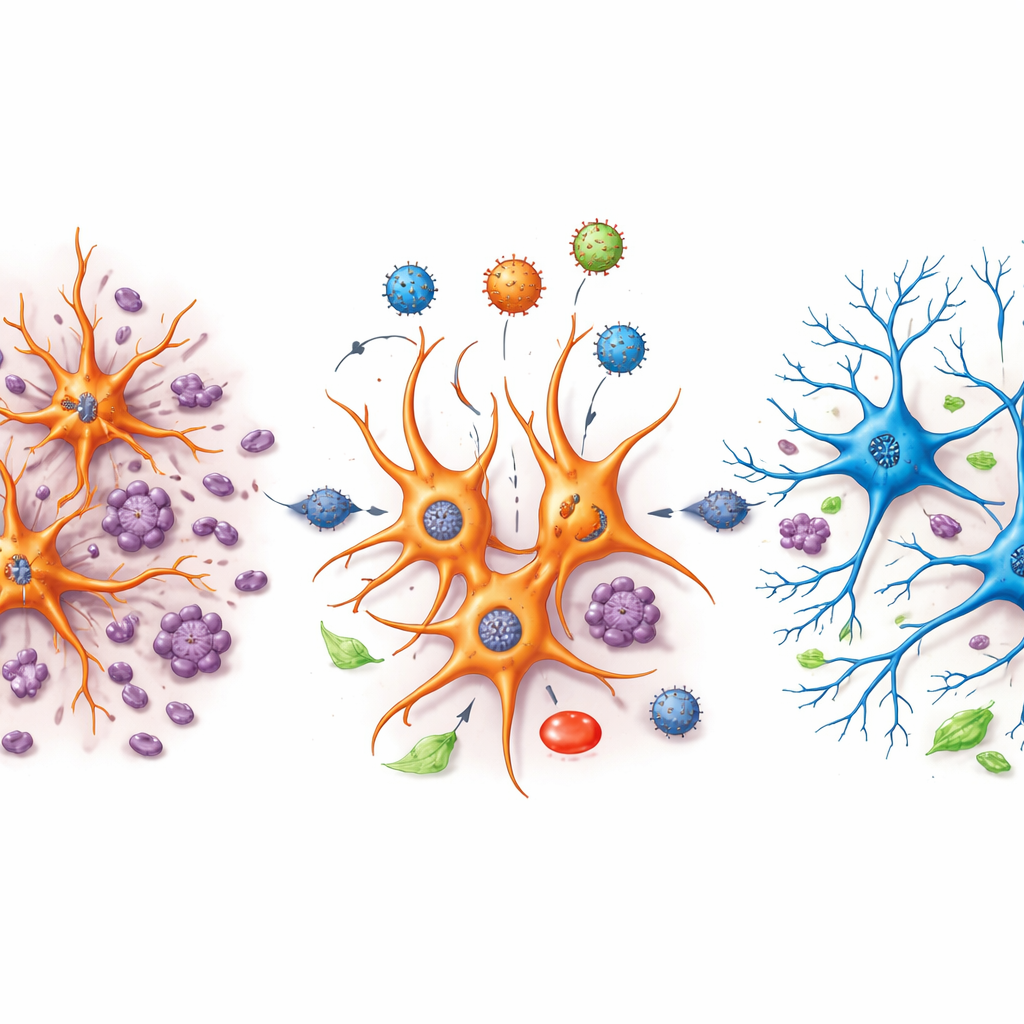
Was das für künftige Hirnreparaturen bedeutet
Diese Arbeit bietet noch keine fertige Heilung für menschliche Hirnverletzungen, aber sie liefert zwei wichtige Fortschritte. Erstens zeigt sie in einem lebenden Säugetiergehirn, dass eine gezielte Gentherapie Gewebeverlust und Entzündung verringern kann, während sie Zellpopulationen und Energieverbrauch wieder in einen gesünderen Zustand lenkt. Zweitens stellt sie einen umfangreichen, öffentlichen Einzelzell-Datensatz bereit, den andere Forschende nutzen können, um spezifische Zelltypen, Gene und Signalwege zu identifizieren, die Schaden oder Erholung nach einem Trauma antreiben. Für Leser außerhalb des Labors lautet die Kernbotschaft: Die eigenen Stützzellen des Gehirns können potenziell rekrutiert und umprogrammiert werden, um verletzte Schaltkreise beim Wiederaufbau zu unterstützen — ein Schritt näher an Therapien, die das Gehirn wiederherstellen, statt es nur zu stabilisieren, nach einem traumatischen Schlag.
Zitation: Chen, R., Zhang, S., Liu, S. et al. A single-cell transcriptomic dataset profiling traumatic brain injury and NeuroD1-based gene therapy in mice. Sci Data 13, 406 (2026). https://doi.org/10.1038/s41597-026-06788-1
Schlüsselwörter: traumatische Hirnverletzung, Gentherapie, Astrozyten, Einzelzellsequenzierung, NeuroD1