Clear Sky Science · de
HMI-LUSC: Ein histologisches Hyperspektral‑Bildgebungs‑Datenset für Plattenepithelkarzinom der Lunge
Krebs in neuen Farben sehen
Lungenkrebs bleibt eine der tödlichsten Krankheiten weltweit, unter anderem weil es schwierig und zeitaufwändig ist, jede einzelne Krebszelle auf einem Objektträger zu erkennen. Pathologen verlassen sich meist auf pink‑violett gefärbtes Gewebe unter dem Mikroskop, eine Methode, die Struktur erfasst, aber subtile chemische Hinweise verpasst. Dieses Paper stellt HMI‑LUSC vor, die erste offen verfügbare Sammlung von Mikroskopaufnahmen von Plattenepithelkarzinomen der Lunge, die nicht nur in drei Farben, sondern in dutzenden schmaler Farbbänder aufgenommen wurden und Computern sowie Klinikern einen weitaus reichhaltigeren Blick darauf geben, was Tumorzellen von gesunden Nachbarn unterscheidet.
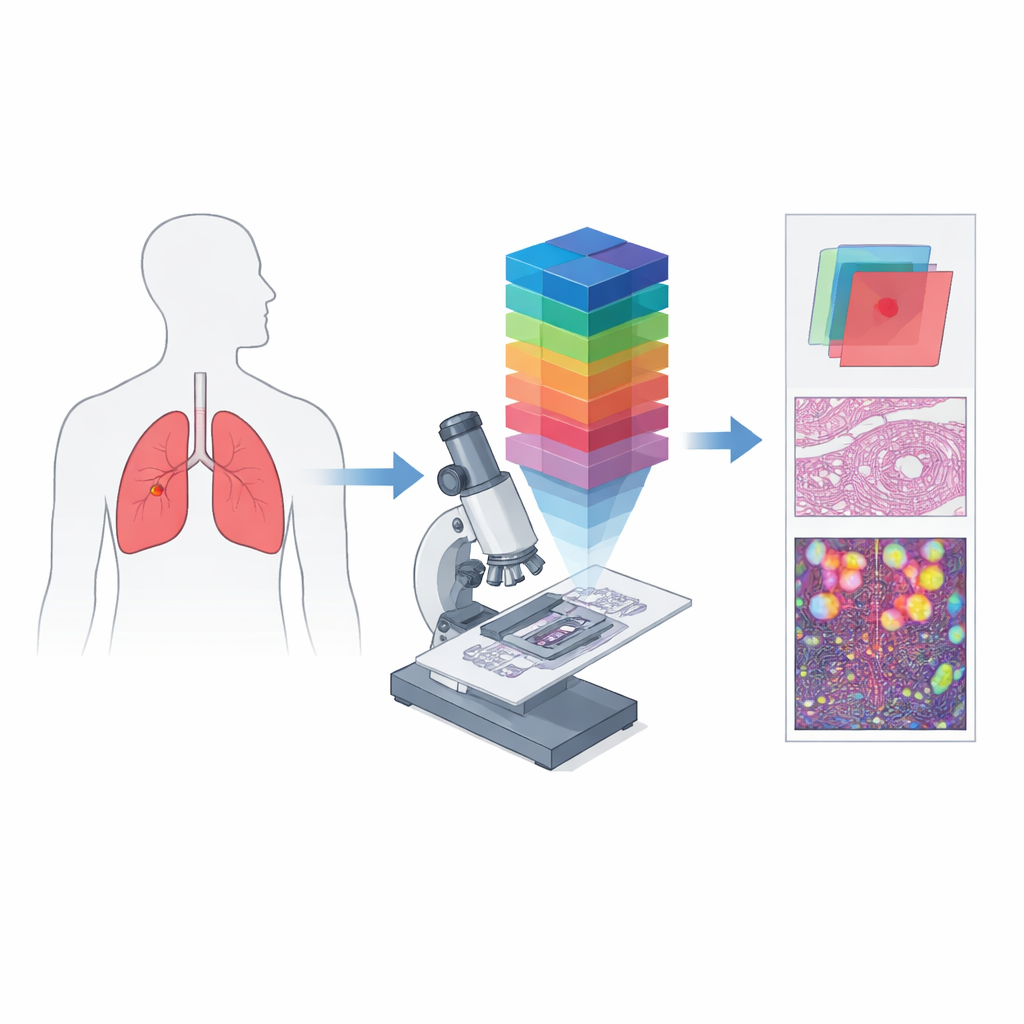
Von einfachen Farbaufnahmen zu spektralen Fingerabdrücken
Konventionelle digitale Pathologie funktioniert ähnlich wie eine Handykamera: Sie zeichnet Rot-, Grün- und Blaukanäle auf, um das Auge zu approximieren. Hyperspektralbildgebung geht mehrere Schritte weiter, indem sie Licht in viele eng benachbarte Wellenlängen aufspaltet und einen dreidimensionalen „Datenwürfel“ erzeugt, in dem jeder winzige Gewebebereich sein eigenes detailliertes Farbspektrum hat. In Kombination mit einem Mikroskop wird daraus hyperspektrale mikroskopische Bildgebung, die sowohl feine Struktur als auch reichhaltige spektrale Informationen auf Zellebene erfassen kann. Solche Daten können Unterschiede in der Absorption und Reflexion von Licht zeigen, die in Standardbildern unsichtbar sind, und so einzigartige spektrale „Signaturen“ für krebsartige und nicht‑krebsartige Bereiche schaffen.
Aufbau einer neuen Bibliothek zur Lungenkrebsforschung
Die Autorinnen und Autoren schufen HMI‑LUSC, um eine klare Lücke zu schließen: Vor dieser Arbeit gab es kein öffentliches Hyperspektral‑Datenset für Lungenkrebsobjektträger, was Tests und Vergleiche computerbasierter Diagnosemethoden erschwerte. Sie sammelten Gewebe von zehn Patientinnen und Patienten, die sich einer Lungentumoroperation unterzogen, bereiteten Standard‑Hämatoxylin‑Eosin‑Schnitte vor und scannten diese in hoher Auflösung. Erfahrene Pathologen markierten Tumor‑ und Normalbereiche, und repräsentative Regionen wurden mit einem eigens entwickelten hyperspektralen Mikroskop erneut abgebildet. Jedes resultierende Bild deckt einen kleinen Gewebefleck ab, umfasst aber 61 Wellenlängen zwischen 450 und 750 Nanometern bei einer Auflösung von 3088 × 2064 Pixeln. Für jede Region enthält das Datenset den rohen spektralen Würfel, eine konventionelle RGB‑Darstellung und Masken, die die Lage des Tumorgewebes abgrenzen.
Aus groben Umrissen werden Karten auf Zellebene
Während Markierungen auf Objektträger‑Ebene nützlich sind, erfordern moderne Algorithmen oft Informationen auf Ebene einzelner Zellen. Jede Zelle manuell nachzuzeichnen ist unpraktisch, daher entwickelte das Team einen semi‑automatischen Arbeitsablauf. Zuerst gruppierten sie Pixel basierend auf spektraler Ähnlichkeit mithilfe einer Standardmethode der Computer Vision. Anschließend inspizierten Pathologen diese Cluster, überlagert auf dem Gewebebild, und ordneten sie vier Kategorien zu: Tumorzellen, Nicht‑Tumorzellen, nicht‑zelluläres Gewebe wie Stroma oder Blut, und leerer Hintergrund. Ein zweiter Pathologe überprüfte und passte die Ergebnisse an; Uneinigkeiten wurden im Konsens gelöst. Das Ergebnis ist ein Satz detaillierter pixelgenauer Masken, die subtile Mischungen von Zelltypen und verwirrende Übergangsbereiche erfassen und so deutlich reichhaltigeres Lehrmaterial für maschinelle Lernsysteme liefern.
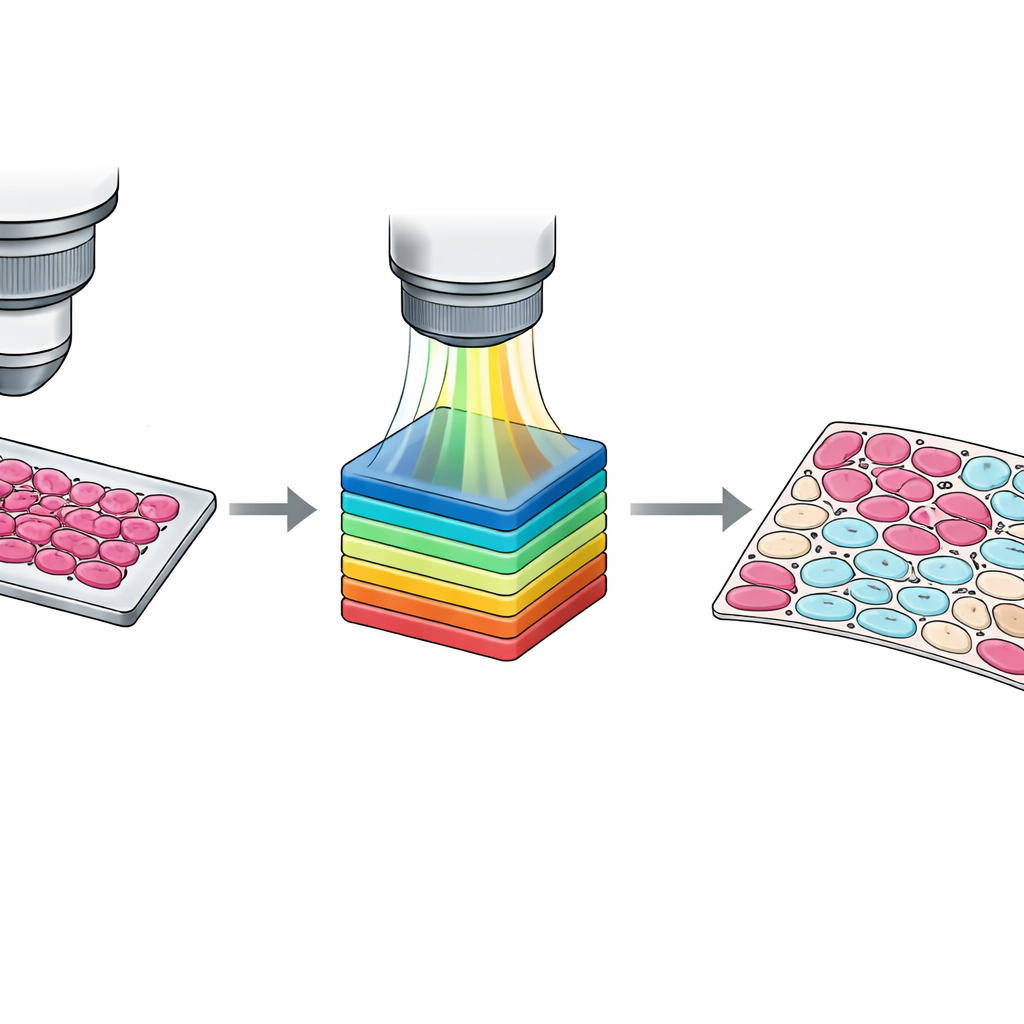
Scharfe und verlässliche Daten sicherstellen
Um das Datenset vertrauenswürdig zu machen, testeten die Autorinnen und Autoren ihr Bildgebungssystem gründlich. Sie verifizierten, dass das Mikroskop feine Muster bis etwa ein Mikrometer auflösen kann — klein genug, um einzelne Zellen zu unterscheiden — und dass das Bildrauschen über die meisten Wellenlängen gering ist. Sie verglichen außerdem das gemessene Spektrum einer Standardlichtquelle mit Referenzkurven und mit einer kommerziellen hyperspektralen Kamera und fanden ausgezeichnete Übereinstimmung. Schließlich zeigten sie, wie die Daten genutzt werden können, indem sie Basis‑Computermodelle laufen ließen, von klassischen Methoden des maschinellen Lernens bis hin zu einfachen Deep‑Learning‑Netzen, um Tumorbereiche zu segmentieren. Selbst ohne umfangreiche Optimierung erreichten diese Modelle solide Genauigkeit, was zeigt, dass das Datenset sich gut als Benchmark für zukünftige Methoden eignet.
Was das für die zukünftige Lungenkrebsversorgung bedeutet
HMI‑LUSC ersetzt keine großen Sammlungen standardisierter Schnitte und ist noch kein klinisches Werkzeug für sich. Stattdessen bietet es Forschenden ein sorgfältig kuratiertes Fenster in die Frage, wie sich Lungen-tumorzellen über viele Lichtwellenlängen von umliegendem Gewebe unterscheiden. Indem diese Daten, Labels und der Code offen verfügbar gemacht werden, stellen die Autorinnen und Autoren eine gemeinsame Testumgebung für die Entwicklung und den Vergleich von Algorithmen bereit, die spektrale Informationen nutzen — von einfachen Klassifikatoren bis hin zu fortgeschrittenen neuronalen Netzen. Langfristig könnte solche Arbeit Computern helfen, Pathologinnen und Pathologen genauer und schneller bei der Tumorerkennung zu unterstützen und spektrale Muster aufzudecken, die mit Tumortypen oder Therapieansprechen verknüpft sind und die gewöhnliche Bilder nicht zeigen können.
Zitation: Yan, Z., Huang, H., Guo, Y. et al. HMI-LUSC: A Histological Hyperspectral Imaging Dataset for Lung Squamous Cell Carcinoma. Sci Data 13, 415 (2026). https://doi.org/10.1038/s41597-026-06766-7
Schlüsselwörter: Hyperspektralbildgebung, Lungenkrebs, digitale Pathologie, Tumorsegmentierung, medizinisches Bildgebungs‑Datenset