Clear Sky Science · de
Ein hochaufgelöstes Histopathologie‑Bilddatensatz für Diagnose und Prognose des Plattenepithelkarzinoms im Mund
Warum diese Forschung wichtig ist
Mundkrebs kann leicht übersehen werden: er beginnt oft als kleine Wunde im Mund und kann sich zu einer lebensbedrohlichen Erkrankung entwickeln. Ärztinnen und Ärzte verlassen sich auf mikroskopische Gewebebilder, um das Ausmaß eines Tumors und seine Wahrscheinlichkeit für Rückfall oder Ausbreitung zu beurteilen, doch das Auswerten dieser Bilder ist zeitaufwendig und anspruchsvoll. In dieser Studie wird eine umfangreiche neue Bildsammlung vorgestellt, die KI‑Systeme dabei unterstützen soll, diese Präparate zusammen mit Pathologinnen und Pathologen zu lesen, mit dem langfristigen Ziel, Patientinnen und Patienten schnellere und genauere Informationen über ihre Erkrankung und Behandlungsoptionen zu bieten.
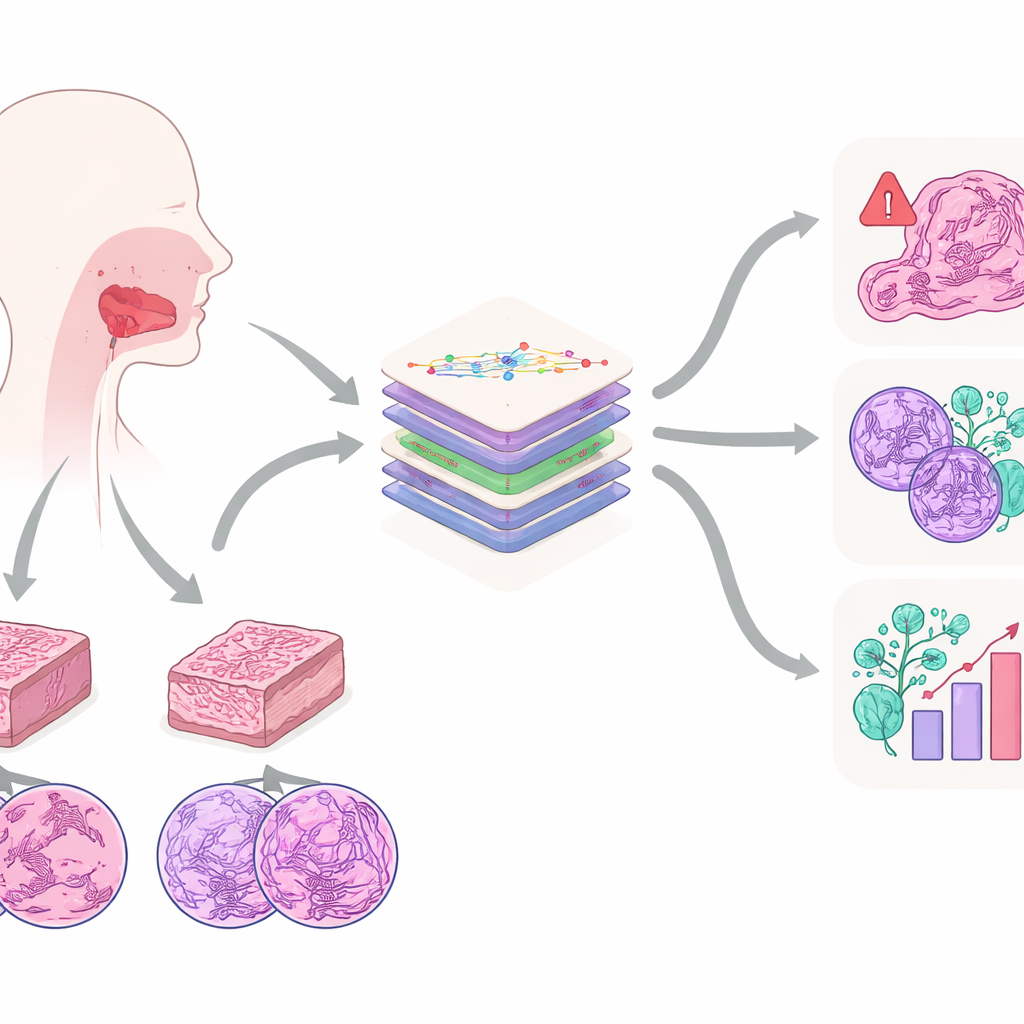
Ein genauerer Blick auf einen häufigen Mundkrebs
Die Arbeit konzentriert sich auf das orale Plattenepithelkarzinom, einen der häufigsten und aggressivsten Mundkrebse. Es tritt häufig bei Personen mit Nikotin‑ oder Alkoholanamnese auf und kann in umliegendes Gewebe und die Lymphknoten im Hals streuen. Bis heute ist der Goldstandard der Diagnose weiterhin das pathologische Auge auf gefärbte Schnittpräparate unter dem Mikroskop. Aus diesen Schnitten beurteilen Expertinnen und Experten, wie abnormal die Zellen aussehen, wie tief der Tumor gewachsen ist, ob er Nerven oder Blutgefäße infiltriert hat und viele weitere Merkmale, die das Überleben beeinflussen. Die Autorinnen und Autoren argumentieren, dass diese mikroskopischen Muster weit mehr Informationen enthalten, als sich ein Mensch leicht merken kann, und sie damit ein ideales Ziel für moderne KI darstellen.
Ein reichhaltigeres Bild aus Gewebebildern aufbauen
Um diese Informationen zu erschließen, erstellte das Team den Multi‑OSCC‑Datensatz: Mikroskopbilder von 1.325 Patientinnen und Patienten, die zwischen 2015 und 2022 an einem einzigen Krankenhaus wegen Mundkrebs behandelt wurden. Für jede Person bereiteten Pathologinnen und Pathologen zwei Gewebeproben vor—eine aus dem Zentrum des Tumors und eine aus dessen invasivem Rand—und fertigten hochaufgelöste Bilder in drei Vergrößerungsstufen an, vergleichbar mit der Sicht auf eine Stadt aus dem Flugzeug, von einem Dach und an einer Straßenecke. Dadurch entstanden pro Patient sechs sorgfältig ausgewählte Bilder, die jeweils wichtige Strukturen wie Tumorzellnester, Keratinwirbel und stark auffällige Zellkerne zeigten. Neben den Bildern sammelten die Forschenden detaillierte Krankengeschichten und Langzeit‑Follow‑up‑Daten, um zu verfolgen, welche Tumoren zurückkehrten oder metastasierten.
Sechs Fragen, die Ärztinnen und Ärzte wirklich interessieren
Was Multi‑OSCC auszeichnet, ist, dass der Datensatz reale klinische Fragestellungen widerspiegelt, statt sich auf ein einziges Label zu beschränken. Jede Patientin und jeder Patient im Datensatz ist für sechs wichtige Ergebnisse annotiert. Eines davon ist, ob der Tumor innerhalb von zwei Jahren nach der Operation rezidivierte, ein kritisches Zeitfenster, in dem die meisten Rückfälle auftreten. Ein weiteres ist, ob Krebszellen bereits die Lymphknoten im Hals erreicht hatten, was Entscheidungen über ausgedehnte Halsoperationen beeinflusst. Vier zusätzliche Labels erfassen, wie gut differenziert die Tumorzellen sind, wie tief der Tumor einwächst und ob er in Blutgefäße eingedrungen oder entlang von Nerven gewachsen ist—feine, aber aussagekräftige Hinweise auf die Gefährlichkeit des Krebses. Dieses Design erlaubt es KI‑Modellen, nicht nur „Tumor versus normal“ zu lernen, sondern ein umfassenderes Bild von Risiko und Schweregrad zu entwickeln.
KI beibringen, komplexe Präparate zu lesen
Die Forschenden verglichen anschließend, wie verschiedene KI‑Strategien mit diesem anspruchsvollen Datensatz umgehen. Sie setzten mehrere moderne Bild‑Erkennungs‑Backbones ein, darunter klassische Faltungsnetzwerke und neuere transformerbasierte Modelle, und fanden heraus, dass Transformer, die speziell auf Pathologie‑Bildern vortrainiert wurden, insgesamt am besten performten. Sie testeten Wege, Informationen aus den sechs Bildern pro Patientin bzw. Patient zu kombinieren, und entdeckten, dass eine einfache Strategie—Merkmale aus jedem Bild extrahieren und anschließend aneinanderfügen—komplexere Fusionsverfahren übertraf. Außerdem untersuchten sie, wie sich Farbstandardisierung der Färbungen auf die Leistung auswirkt: Die Beibehaltung der Originalfarbe war wichtig für die Vorhersage von Rezidiven, während eine schonende Farbnormalisierung bei den anderen diagnostischen Aufgaben hilfreich war.
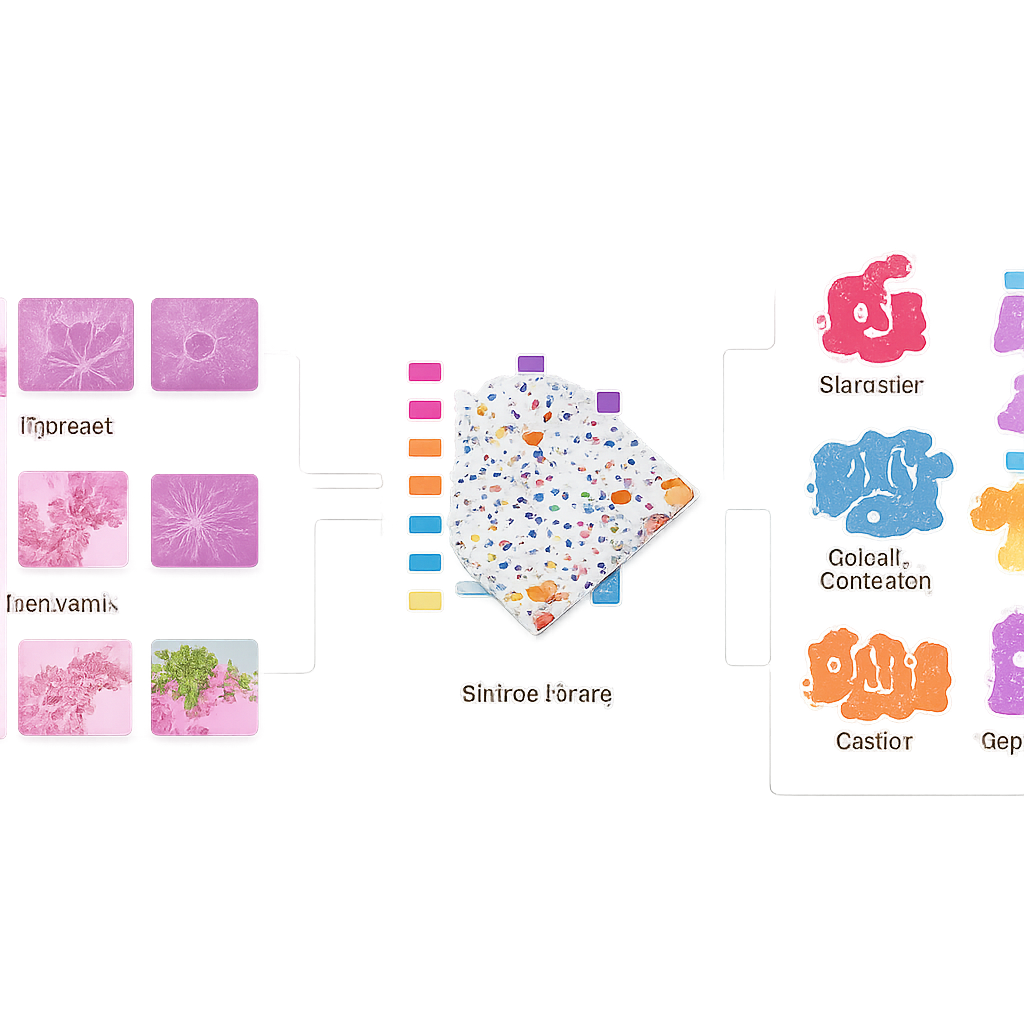
Grenzen, Überraschungen und Ausblick
Eine Überraschung war, dass das Training eines einzelnen KI‑Modells für alle sechs Fragen gleichzeitig noch nicht besser abschnitt als separat für jede Aufgabe trainierte Modelle. Eine weitere Erkenntnis: Detaillierte Mikroskoppatches, obwohl reich an zellulären Details, fehlen oft die weiträumige Architekturperspektive, die ganze Schnittpräparate bieten. Dennoch übertrafen Modelle, die auf den Multi‑OSCC‑Bildern trainiert wurden, klar Modelle, die nur klinische Daten wie Alter, Gewohnheiten und Krankengeschichte nutzten, insbesondere bei der Vorhersage von Tumorrezidiven. Die Autorinnen und Autoren verstehen Multi‑OSCC als Ausgangspunkt: ein öffentlich verfügbares, gut dokumentiertes Datenset, das andere zur Entwicklung und zum Vergleich von Methoden nutzen können. Für Patientinnen und Patienten besteht das langfristige Versprechen darin, dass künftige Werkzeuge, die auf dieser Ressource aufbauen, Ärztinnen und Ärzten dabei helfen könnten, zuverlässiger zu erkennen, welche oralen Karzinome wahrscheinlich zurückkehren oder streuen—was zu gezielteren Behandlungen und letztlich besseren Überlebenschancen führen kann.
Zitation: Guan, J., Guo, J., Chen, Q. et al. A High Magnifications Histopathology Image Dataset for Oral Squamous Cell Carcinoma Diagnosis and Prognosis. Sci Data 13, 371 (2026). https://doi.org/10.1038/s41597-026-06736-z
Schlüsselwörter: Mundkrebs, histopathologische Bilder, künstliche Intelligenz, deep learning, medizinische Bilddatensätze