Clear Sky Science · de
Groß angelegter histologischer Bilddatensatz mit Metadaten für das kolorektale Krebs-Mikroumfeld
Warum die Kartierung von Krebs’ verborgener Nachbarschaft wichtig ist
Wenn Ärztinnen und Ärzte einen Tumor im Dickdarm unter dem Mikroskop betrachten, sehen sie nicht nur Krebszellen; sie sehen eine lebhafte Nachbarschaft aus Fett, Immunzellen, Bindegewebe und mehr. Diese Mischung aus Zelltypen, das sogenannte Tumor-Mikroumfeld, beeinflusst stark, wie ein Patient auf Therapien reagiert und wie lange er lebt. Computer, die Ärztinnen und Ärzten helfen könnten, diese komplexen Szenen zu verstehen, wurden jedoch durch ein einfaches Problem ausgebremst: Es gab nicht genug gut annotierte Bilder, von denen sie lernen könnten. Diese Studie stellt eine der größten und sorgfältigsten Bildsammlungen von kolorektalem Tumorgewebe vor, die je zusammengestellt wurde, und die speziell dafür ausgelegt ist, moderne KI-Systeme zu trainieren und zu prüfen.
Aufbau einer umfangreichen Bildbibliothek von Darmtumoren
Die Forschenden schufen eine Ressource namens HMU-CRC-Hist550K, basierend auf Gewebeproben von 500 Patientinnen und Patienten, die an einem großen Krebszentrum in China behandelt wurden. Der Tumor jedes Patienten wurde konserviert, wie üblich in der Pathologie gefärbt und als hochauflösende digitale Folie gescannt. Aus diesen Folien schnitt das Team automatisch kleine quadratische Bildkacheln aus, jeweils ungefähr so groß wie das, was eine Pathologin oder ein Pathologe bei einer Mikroskopbetrachtung gleichzeitig sieht. Insgesamt entstanden so etwa 550.000 Kacheln, wodurch KI-Modelle eine enorme und vielfältige Menge an Beispielen erhalten, um zu lernen, wie verschiedene Gewebe aussehen.
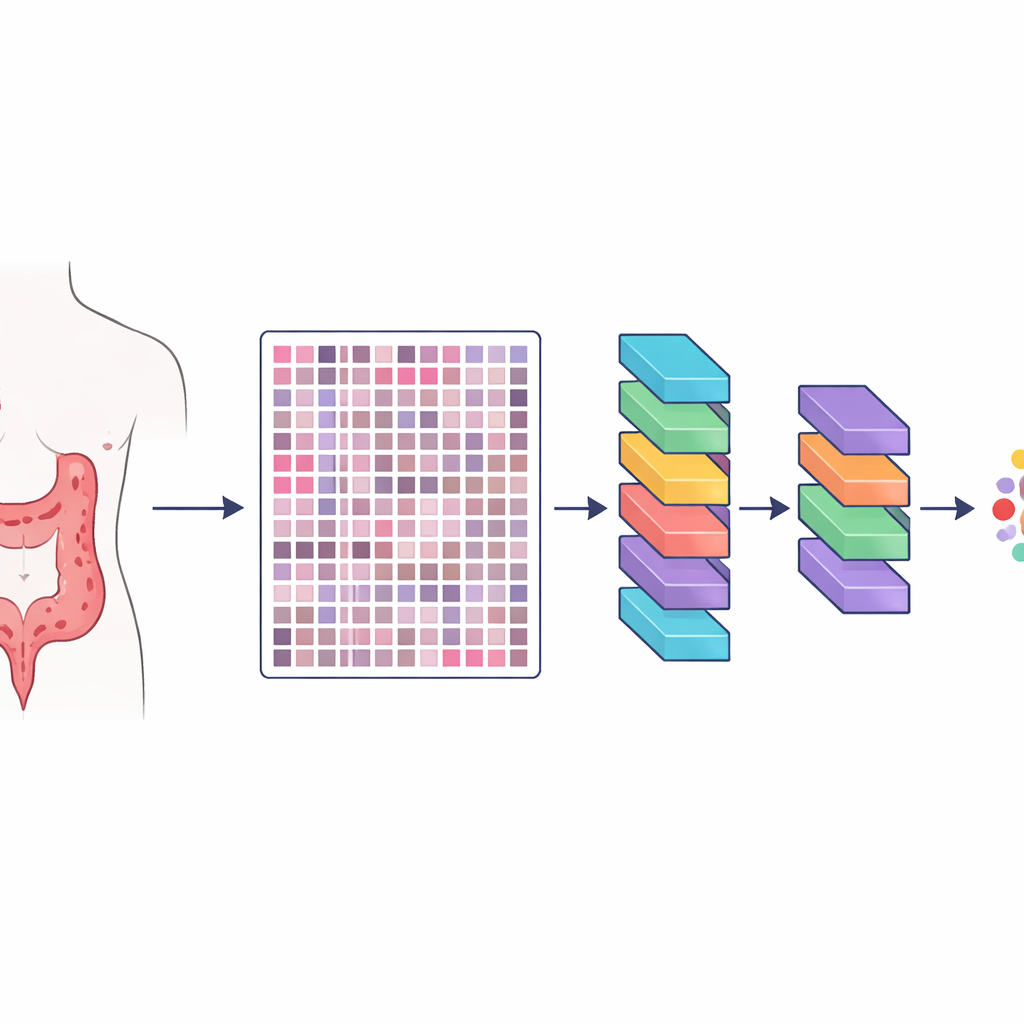
Sorgfältige menschliche Annotationsarbeit in der Krebslandschaft
Eine große Bildbibliothek allein reicht nicht aus; die Bilder müssen auch genau beschriftet sein. Drei erfahrene Pathologinnen und Pathologen arbeiteten in einem dreistufigen Verfahren zusammen, um acht wichtige Komponenten der Tumorumgebung zu markieren: Fettgewebe, Zelltrümmer, Immunzellen namens Lymphozyten, Schleim, glatte Muskulatur, normales Kolonepithel, das stützende Bindegewebe um den Tumor und die Krebszellen selbst. Zwei Pathologinnen oder Pathologen zeichneten zunächst unabhängig voneinander Regionen auf den großen Folien und überprüften anschließend gegenseitig ihre Arbeit. Ein leitender Spezialist führte eine abschließende Durchsicht durch, löste Uneinigkeiten und schloss unklare Bereiche aus. Diese Überprüfung reduzierte persönliche Verzerrungen erheblich und erzeugte sehr konsistente Labels in feiner Auflösung, sodass jede Kachel einem spezifischen Gewebetyp innerhalb der Tumornachbarschaft zugeordnet ist.
Verknüpfung von Mikroskopansichten mit Patientengeschichten
Was diesen Datensatz besonders mächtig macht, ist, dass die Bilder mit umfangreichen klinischen Informationen zu jedem Patienten verknüpft sind. Für jeden Fall sammelte das Team Basisdaten wie Alter und Geschlecht sowie Tumorstadium, Tumorlage entlang von Darm und Rektum, das Ausmaß der zellulären Atypien, ob Nerven oder Lymphknoten befallen waren, und die Überlebensdauer nach der Behandlung. Ebenso wurden Ergebnisse gängiger Labortests erfasst, die auf die genetische und proteomische Beschaffenheit des Tumors hinweisen. Alle persönlichen Identifikatoren wurden entfernt, sodass Patientinnen und Patienten nicht rückverfolgbar sind. Durch die Kombination von Gewebemustern mit diesen klinischen Merkmalen können Forschende untersuchen, wie spezifische Mikroumfeld-Layouts mit realen Ergebnissen zusammenhängen, etwa welche Patienten besser oder schlechter abschneiden.
KI-Testläufe mit dem neuen Datensatz
Um zu zeigen, dass der Datensatz wirklich nützlich ist, trainierten die Wissenschaftlerinnen und Wissenschaftler drei verschiedene Deep-Learning-Modelle — moderne Mustererkennungssysteme, die bei Bildaufgaben hervorragend sind — um die acht Gewebetypen in den Kacheln zu identifizieren. Sie verwendeten strikte Regeln, um Patienten zwischen Trainings- und Testgruppen aufzuteilen, sodass die Modelle an Patienten gemessen wurden, die sie nie zuvor gesehen hatten. Die Modelle, darunter klassische Bildnetzwerke und ein neueres „Vision Transformer“-Design, erreichten alle sehr hohe Genauigkeiten, mit Leistungsergebnissen, die in mehreren Testsets nahe an der Perfektion lagen. Das Team verglich die Resultate auch mit anderen fortgeschrittenen Segmentierungsmethoden und fand ähnlich starke Leistungen. Visuelle Werkzeuge wurden eingesetzt, um hervorzuheben, auf welche Gewebeabschnitte sich die Modelle stützten, was bestätigte, dass sie sich auf medizinisch sinnvolle Regionen konzentrierten und nicht auf zufällige Muster.
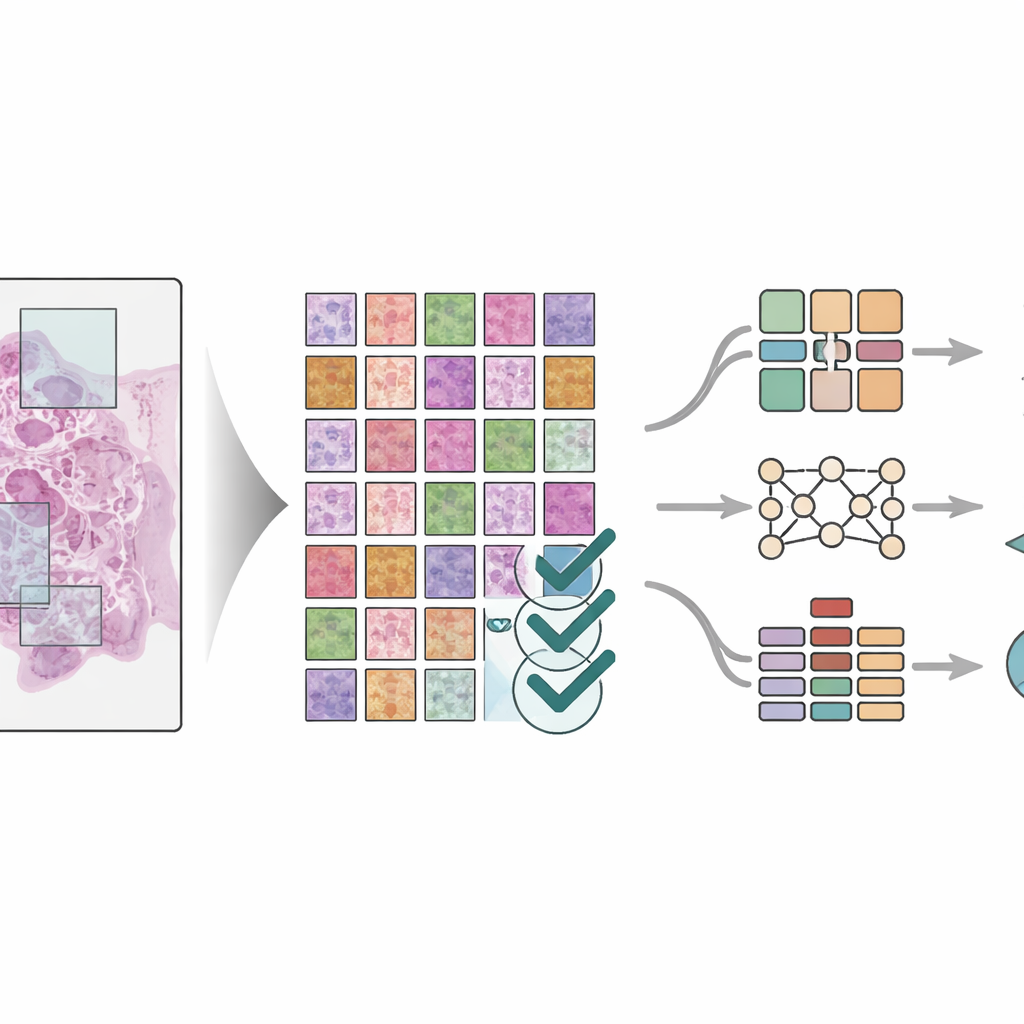
Was das für die zukünftige Krebsversorgung bedeutet
Für Nichtfachleute lautet die zentrale Botschaft: Diese Arbeit führt keine neue Therapie ein, sondern legt ein starkes Fundament für eine intelligentere Diagnostik und Prognose. Durch das Teilen einer großen, gut organisierten und offen verfügbaren Bildbibliothek, die mit detaillierten Patientenakten verknüpft ist, ermöglichen die Autorinnen und Autoren Forschenden weltweit, KI-Werkzeuge auf derselben soliden Grundlage zu entwickeln und zu vergleichen. Solche Werkzeuge könnten Pathologinnen und Pathologen schließlich dabei helfen, die Tumornachbarschaft schneller und konsistenter zu kartieren, vorherzusagen, welche Patienten ein höheres Risiko haben, und personalisiertere Behandlungsstrategien vorzuschlagen. Zwar erfassen die aktuellen Daten nur einzelne Zeitpunkte statt Veränderungen über Monate oder Jahre, doch stellt diese Ressource einen wichtigen Schritt dar, digitale Pathologie und KI zu nutzen, um das kolorektale Krebsverständnis zu verbessern und letztlich besser zu behandeln.
Zitation: Wang, H., Li, H., Xue, J. et al. Large-Scale Histological Image Dataset with Metadata for Colorectal Cancer Microenvironment. Sci Data 13, 431 (2026). https://doi.org/10.1038/s41597-026-06675-9
Schlüsselwörter: kolorektales Karzinom, Tumor-Mikroumfeld, digitale Pathologie, Deep Learning, medizinischer Bilddatensatz