Clear Sky Science · de
Umfassende Transkriptomprofilierung sporadischer medullärer Schilddrüsenkarzinome
Warum diese seltene Schilddrüsenkrebserkrankung wichtig ist
Das medulläre Schilddrüsenkarzinom ist eine seltene Form von Schilddrüsenkrebs, die tendenziell aggressiver verläuft als die meisten Schilddrüsentumoren und häufig erst in fortgeschrittenem Stadium diagnostiziert wird. Weil die Erkrankung ungewöhnlich ist, standen Ärztinnen, Ärzte und Forschende nur begrenzte Daten zur Verfügung, um zu verstehen, warum einige Tumoren schneller wachsen und metastasieren oder warum bestimmte Patientinnen und Patienten besser auf Therapien ansprechen. Diese Studie schließt diese Lücke, indem sie einen tiefgehenden, genomweiten Blick auf die Aktivität von Tausenden von Genen in 72 Tumoren wirft und damit einen der bislang vollständigsten molekularen Schnappschüsse dieser Krankheit liefert.
Ein Blick in Tumorzellen
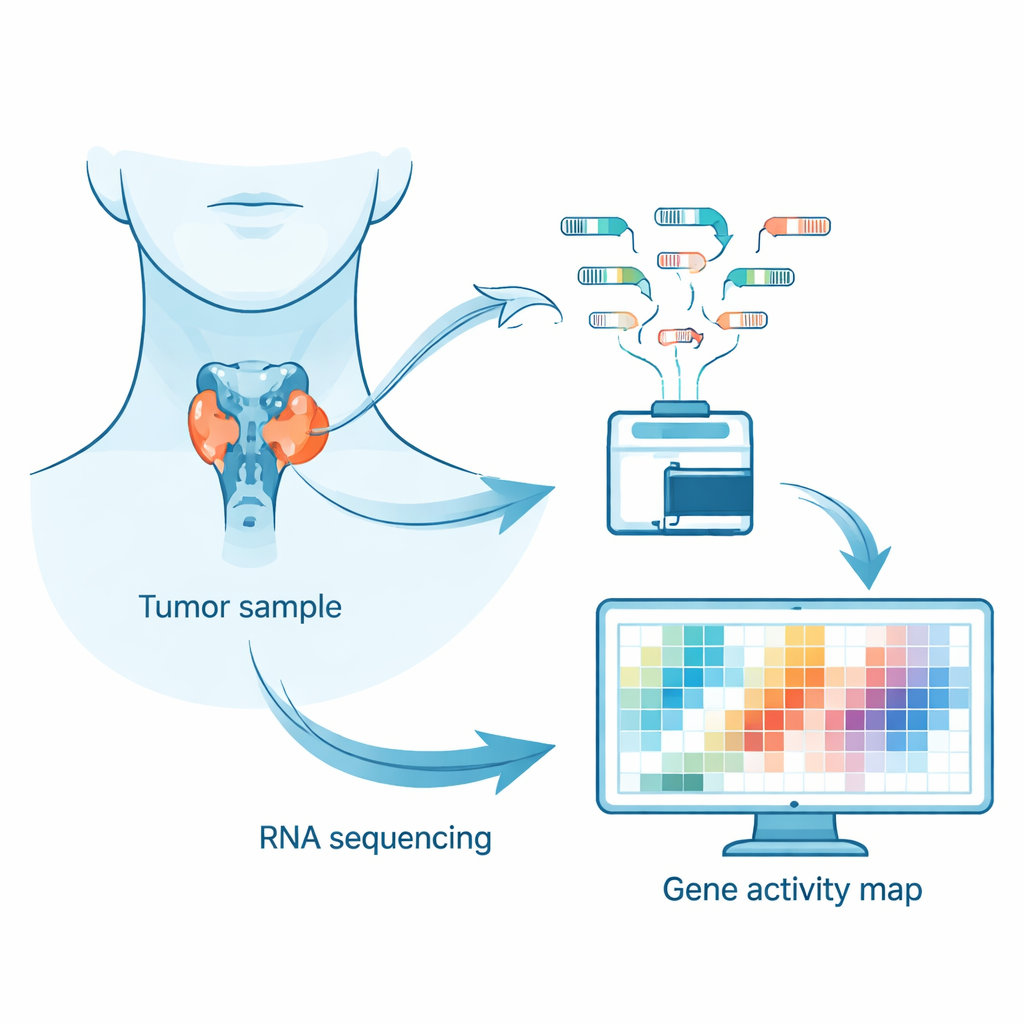
Anstatt sich nur auf DNA-Mutationen zu konzentrieren, untersuchten die Forschenden das Tumor‑„Transkriptom“ – die Gesamtheit der RNA‑Botschaften, die von aktiven Genen in Krebszellen produziert werden. Diese RNA‑Botschaften fungieren wie Echtzeit‑Statusberichte darüber, was die Zelle gerade tut. Durch die Sequenzierung von RNA aus frisch eingefrorenen Tumorproben konnte das Team sehen, welche Gene hochreguliert, welche herunterreguliert waren und wie Genbotschaften zusammengesetzt wurden. Dieser Ansatz hilft, verborgene Muster aufzudecken, die klassische Gentests möglicherweise übersehen, etwa Änderungen in der Genregulation oder in der Kombination von Genabschnitten.
Wer untersucht wurde und was gemessen wurde
Das Team analysierte Tumoren von 72 Personen mit sporadischem (nicht familiärem) medullärem Schilddrüsenkarzinom. Etwas mehr als die Hälfte waren Frauen, und das Medianalter zum Zeitpunkt der Operation betrug 61 Jahre. Etwa 58 % der Tumoren wiesen Veränderungen im Gen RET auf und rund 24 % Träger von Mutationen in RAS‑Familiengenen, beides bekannte Treiber dieser Krebsart. Die Wissenschaftlerinnen und Wissenschaftler prüften zunächst, dass die Tumorproben von hoher Qualität und relativ frei von normalem Schilddrüsengewebe oder Immunzellkontamination waren, indem sie Schlüsselmarker wie Calcitonin – das in diesen Tumoren hoch ist – und Thyreoglobulin – typisch für normales Schilddrüsengewebe und niedrig blieb – betrachteten. Anschließend nutzten sie bewährte rechnerische Werkzeuge, um die RNA‑Reads am menschlichen Genom auszurichten, Genaktivität zu zählen und Unterschiede zwischen klinischen und genetischen Gruppen zu suchen.
Genaktivität verknüpft mit Stadium und Mutation
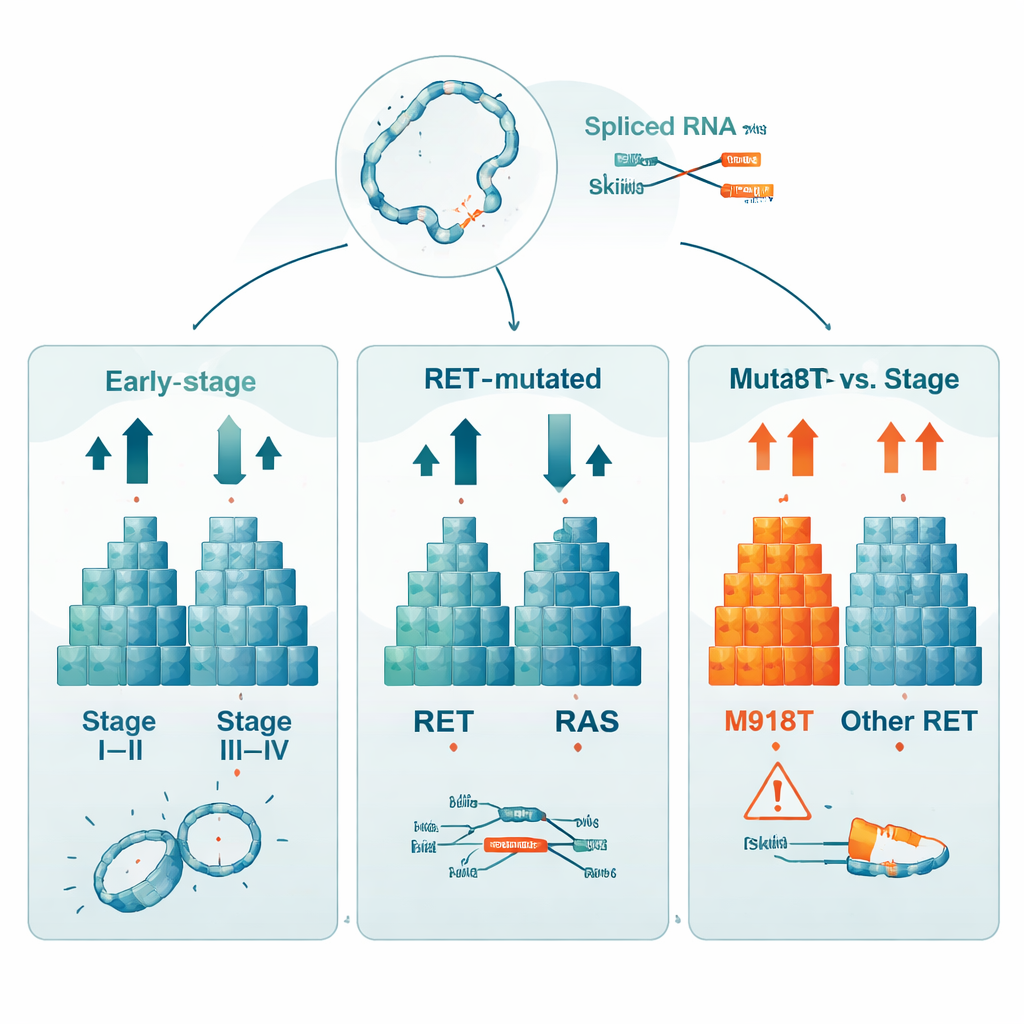
Beim Vergleich frühstadialer Tumoren (Stadium I–II) mit weiter fortgeschrittenen (Stadium III–IV) identifizierten die Forschenden 760 Gene, deren Aktivitätsniveaus sich deutlich zwischen den beiden Gruppen unterschieden. Das bedeutet, dass Expressionsmuster starke Hinweise darauf geben, wie weit der Krebs fortgeschritten ist. Sie verglichen außerdem Tumoren mit RET‑ oder RAS‑Mutationen mit solchen ohne diese Veränderungen und fanden über 1.200 Gene mit veränderter Aktivität. Eine separate Analyse fokussierte auf Tumoren mit einer spezifischen RET‑Veränderung, genannt M918T, die seit Langem mit besonders ungünstiger Prognose verbunden ist. In diesen Tumoren zeigten 529 Gene differenzielle Aktivität im Vergleich zu RET‑normalen Krebsen, und das RET‑Gen selbst war stärker exprimiert, was unterstreicht, wie stark diese einzelne Veränderung das Verhalten der Zelle umformt.
Verborgene Umschaltungen und Umprogrammierung der Botschaften
Über einfache An‑/Ab‑Regulationen von Genen hinaus suchte die Studie nach tiefergehenden Formen der RNA‑Störung. Das Team entdeckte 59 verschiedene Genfusions‑Transkripte, bei denen Teile unterschiedlicher Gene auf RNA‑Ebene ungewöhnlich miteinander verbunden sind. Die meisten waren selten, und die häufigste Fusion könnte ein technischer Artefakt widerspiegeln, doch der Katalog zeigt, dass solche Umordnungen systematisch aus diesen Daten gewonnen werden können. Die Forschenden kartierten außerdem Tausende alternativer Spleißereignisse, bei denen Abschnitte von Genbotschaften ausgelassen, vertauscht oder beibehalten werden. Während jede klinische Vergleichsgruppe (nach Stadium, Mutationstyp oder M918T‑Status) ähnliche Gesamtzahlen solcher Spleißveränderungen zeigte, unterschieden sich die konkreten Ereignisse weitgehend, was auf mehrere, teilweise unabhängige Wege hindeutet, auf denen Tumorzellen ihre Genbotschaften umprogrammieren.
Was diese Ressource Patientinnen und Wissenschaftlern bietet
Für Patientinnen und Patienten führt diese Arbeit noch nicht unmittelbar zu einem neuen Medikament oder Test, aber sie legt essenzielle Grundlagen. Indem die Autorinnen und Autoren alle aufbereiteten RNA‑Sequenzierungsdaten öffentlich zugänglich machen, bieten sie eine wertvolle Ressource, die andere Forschende nutzen können, um neue Biomarker zur Prognosevorhersage zu entdecken, die Klassifizierung medullärer Schilddrüsenkarzinome zu verfeinern oder Schwachstellen zu identifizieren, die künftige Therapien — einschließlich der neuen Generation selektiver RET‑Inhibitoren — angreifbar machen könnten. Einfach ausgedrückt liefert diese Studie eine detaillierte „Aktivitätskarte“ der Tumor‑Gene über viele reale Fälle hinweg und gibt Forschenden die Werkzeuge an die Hand, besser zu verstehen, warum dieser seltene Krebs von Person zu Person so unterschiedlich verläuft und wie die Versorgung eines Tages gezielter gestaltet werden könnte.
Zitation: Palumbo, D., Melone, V., Palo, L. et al. Comprehensive Transcriptome Profiling of Sporadic Medullary Thyroid Carcinomas. Sci Data 13, 234 (2026). https://doi.org/10.1038/s41597-026-06550-7
Schlüsselwörter: medulläres Schilddrüsenkarzinom, Krebsgenomik, RNA-Sequenzierung, RET-Mutation, personalisierte Onkologie