Clear Sky Science · de
Der Vitamin‑B2‑Stoffwechsel fördert die Stabilität von FSP1, um Ferroptose zu verhindern
Wie ein übliches Vitamin Zellen bei der Entscheidung zwischen Leben und Tod hilft
Unsere Zellen balancieren ständig auf einem Drahtseil zwischen Überleben und Selbstzerstörung. Eine dramatische Form des Zellsterbens, die Ferroptose genannt wird, ist ins Blickfeld gerückt, weil sie gezielt Krebszellen töten kann, die gegen andere Behandlungen resistent sind. Diese Studie zeigt, dass ein alltäglicher Nährstoff — Vitamin B2, auch Riboflavin genannt — das Gleichgewicht heimlich verschiebt, indem er ein wichtiges Schutzprotein stabilisiert. Das Verständnis dieser verborgenen Verbindung zwischen Ernährung, Zellstoffwechsel und Tumorzelltod könnte Forschern helfen, intelligentere Therapien zu entwickeln und künftige Ernährungsempfehlungen zu verfeinern.
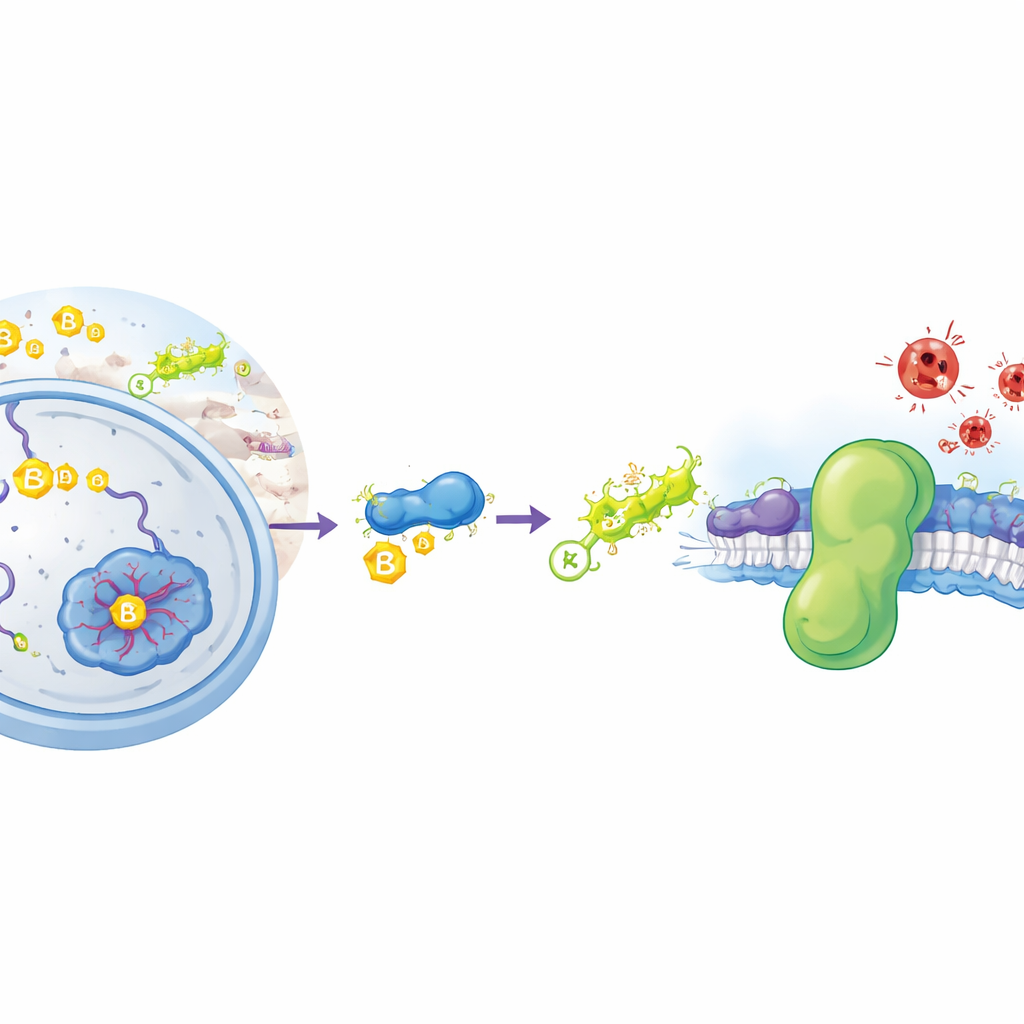
Eine besondere Art von Rost in den Zellen
Ferroptose ist eine Form des Zellsterbens, die durch einen chemischen Vorgang angetrieben wird, der dem Rosten von Metallen ähnelt: die unkontrollierte Oxidation von Fetten in den Zellmembranen. Wenn diese Fette zerfallen, verlieren Membranen ihre Integrität und Zellen platzen. Unsere Zellen setzen normalerweise mehrere Abwehrmechanismen dagegen ein. Ein wichtiges Schutzsystem ist das Enzym GPX4, das ein kleines Molekül, Glutathion, nutzt, um schädliche Lipidperoxide zu entgiften. Ein zweiter, paralleler Schutz ist das Protein FSP1, das an Zellmembranen sitzt und mit fettähnlichen Molekülen schädliche Radikale abfängt, bevor sie sich ausbreiten. Krebszellen steigern oft FSP1, um Ferroptose zu entgehen, weshalb dieses Protein ein vielversprechendes Ziel für neue Krebsmedikamente ist. Bislang war jedoch unklar, wie Zellen steuern, wie viel FSP1 hergestellt wird und wie lange es überlebt.
Aufbau einer zellulären „Tankanzeige“ für einen Todesblocker
Um die verborgenen Regulatoren von FSP1 zu entdecken, statteten die Forscher zuerst menschliche Knochenkrebszellen mit einem fluoreszenten Reporter aus. Sie markierten das natürliche FSP1‑Protein mit einem grünen Signal und kombinierten es mit einem blauen Signal, das anzeigt, wie viel FSP1‑Botschaft die Zelle produziert. Dieses clevere Design erlaubte es ihnen, Änderungen in der Genaktivität (blau) von Änderungen in der Proteinstabilität (grün) zu unterscheiden. Mit diesem Zwei‑Farb‑System setzten sie CRISPR–Cas9 ein, um systematisch nahezu jedes Gen im Genom zu stören, und sortierten dann Zellen mit hohen bzw. niedrigen FSP1‑Spiegeln. Durch den Vergleich, welche Guide‑RNAs in den Gruppen angereichert waren, kartierten sie Hunderte von Genen, die FSP1 entweder fördern oder vermindern, sei es auf Ebene der Genkontrolle oder des Proteinabbaus.
Die verborgene Aufgabe von Vitamin B2: einen stabilisierenden Griff schaffen
Zu den auffälligsten Treffern gehörten zwei Enzyme, Riboflavinkinase (RFK) und FAD‑Synthase (FLAD1), die Vitamin B2 in einen Cofaktor namens FAD umwandeln. FSP1 ist ein Flavoprotein, das normalerweise FAD fest bindet, um seine chemischen Reaktionen auszuführen. Wenn RFK oder FLAD1 entfernt wurden oder wenn Zellen in vitamin‑B2‑armem Medium kultiviert wurden, sanken die FSP1‑Proteinspiegel stark, obwohl die Genaktivität ähnlich blieb. Das Team zeigte, dass dieser Verlust die Zellen deutlich anfälliger für Ferroptose machte, wenn GPX4 blockiert war. Wichtig ist, dass Vitamin B2 selbst nicht als klassisches Antioxidans wirkte: In einem empfindlichen Reagenzglas‑Test konnte es die Lipidoxidation nicht stoppen, anders als Vitamin E. Stattdessen stellten die Zugabe von FAD (und teilweise seines Vorläufers FMN) in defiziente Zellen sowohl die FSP1‑Spiegel als auch die Resistenz gegen ferroptotischen Tod wieder her, während zusätzliches Vitamin B2 allein nicht half, wenn die verarbeitenden Enzyme fehlten.
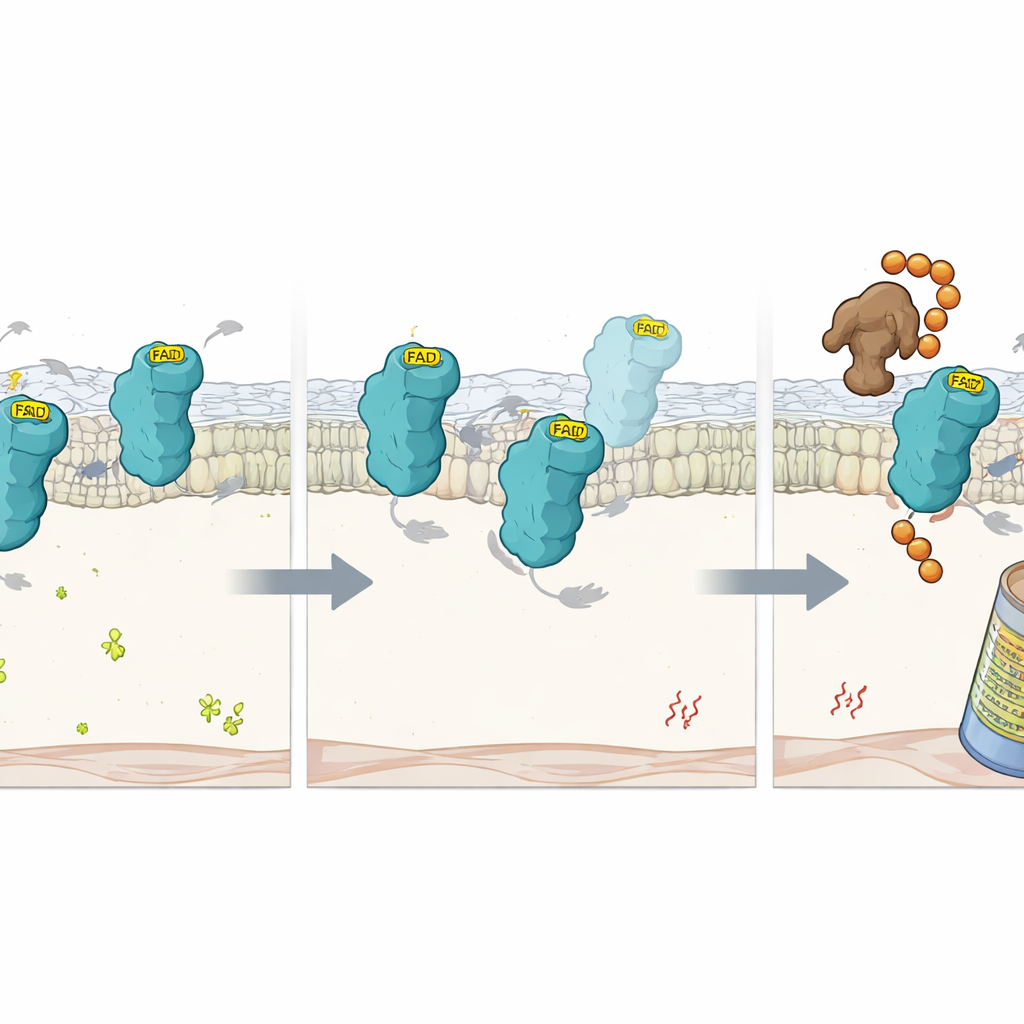
Was passiert, wenn der Cofaktor fehlt
Um näher hinzusehen, untersuchten die Wissenschaftler präzise Mutationen in FSP1, die seine Fähigkeit, FAD zu halten, schwächen. Diese mutierten Proteine falteten sich weitgehend normal, verloren jedoch ihr FAD und ihre katalytische Aktivität. In Zellen bauten sie sich deutlich schneller ab als normales FSP1, es sei denn, das Proteasom — die proteinzerkleinernde Maschinerie der Zelle — wurde blockiert. Das deutete darauf hin, dass die FAD‑Bindung selbst wie ein stabilisierender Griff wirkt, der FSP1 davor schützt, als defekt markiert zu werden. Mithilfe eines weiteren fokussierten CRISPR‑Screens unter FAD‑armen Bedingungen identifizierte das Team eine E3‑Ligase namens RNF8 als Schlüsselfaktor, der FAD‑freies FSP1 erkennt. Als RFK gelöscht wurde, hängte RNF8 Ketten von Ubiquitin‑Markern an das leere Protein und markierte es so zur Zerstörung durch das Proteasom. Die Entfernung von RNF8 verlangsamte den FSP1‑Abbau in FAD‑armen Zellen, konnte dessen verlorene Schutzfunktion jedoch ohne den Cofaktor nicht wiederherstellen.
Von molekularen Schaltkreisen zu Ideen für Krebstherapien
Setzt man diese Erkenntnisse zusammen, schlagen die Autoren ein einfaches, aber wirkungsvolles Modell vor. Vitamin B2 wird von RFK und FLAD1 in FAD umgewandelt, bindet an FSP1 und ist sowohl für seine biochemische Aktivität als auch für seine Langlebigkeit unerlässlich. Fällt die Versorgung mit Vitamin B2 oder seine Verarbeitung aus, kann neu synthetisiertes FSP1 kein FAD sichern, wird von RNF8 markiert und rasch vom Proteasom abgebaut, wodurch die Zellen anfälliger für ferroptotische Schäden werden. Tumordaten legen nahe, dass Tumoren mit höherer RFK‑Expression resistenter gegenüber ferroptoseauslösenden Medikamenten sind, was die Relevanz dieses Weges in realen Bedingungen unterstreicht. Für Nicht‑Spezialisten lautet die Kernbotschaft: Ein vertrautes Vitamin tut weit mehr, als nur als einfaches Antioxidans zu wirken — es entscheidet mit darüber, ob ein kraftvolles Anti‑Todes‑Protein Wächter spielt oder entsorgt wird. Durch das Tuning des Vitamin‑B2‑Stoffwechsels oder der Stabilität von FSP1 könnten künftige Behandlungen Ferroptose gezielter nutzen, um Krebszellen zu eliminieren und gleichzeitig gesundes Gewebe zu schonen.
Zitation: Deol, K.K., Harris, C.A., Tomlinson, S.J. et al. Vitamin B2 metabolism promotes FSP1 stability to prevent ferroptosis. Nat Struct Mol Biol 33, 525–536 (2026). https://doi.org/10.1038/s41594-026-01759-x
Schlüsselwörter: Ferroptose, Vitamin B2, FSP1, Tumorzelltod, Zellstoffwechsel